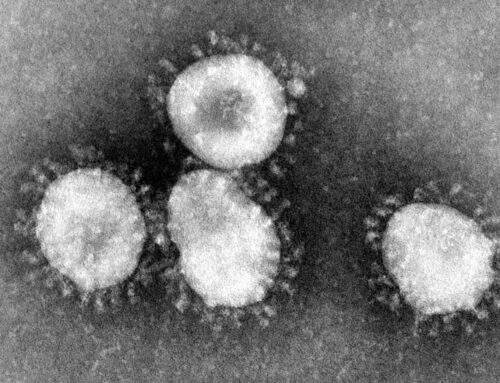
« Pendant qu’ils échangeaient ces paroles entre eux, un chien couché leva la tête et les oreilles ; c’était Argos, le chien que le vaillant Ulysse achevait d’élever, quand il fallut partir vers la sainte Ilion (…). Négligé maintenant, en l’absence du maître, il gisait, étendu au-devant du portail, sur le tas de fumier des mulets et des bœufs (…). C’est là qu’Argos était couché, tout couvert de tiques ».
Ce triste passage décrivant la condition d’Argos, qui aura attendu vingt ans (tout de même !) le retour de son maître, est dans le chant XVII de l’Odyssée. Rappelons qu’après, le chien entend la voix d’Ulysse, lève la tête et les oreilles, reconnaît son maître, remue la queue, couche les deux oreilles, et puis (désolé de spoiler), il meurt. Bon, en dehors de son côté romanesque et déchirant, ce passage présente l’intérêt de montrer que les problèmes de tiques, ça ne date pas d’hier. On en a même trouvé quelques-unes en Birmanie, encore accrochées à une plume d’un dinosaure du Crétacé, le tout conservé dans de l’ambre fossile et remontant à quelque 99 millions d’années ; autant dire qu’Argos, à côté, il fait un peu petit joueur – mais pour le sujet qui nous intéresse aujourd’hui, une tique de chien dans une île grecque, c’est tout de même plus pertinent qu’une tique de dinosaure volant en Birmanie. On va même restreindre encore plus le sujet, en limitant cet article aux tiques que l’on trouve aujourd’hui, en France, chez le chien – et beaucoup plus rarement chez le Chat, c’est pour ça qu’on a mis cette espèce entre parenthèses dans le titre. Allez, c’est parti.
Qui sont les tiques du chien (et du chat) ?
Pour prendre les choses dans l’ordre, une tique, qu’est-ce que c’est ? Il s’agit d’un Arthropode, appartenant à la classe des Arachnides (comme les araignées, donc), et à la sous-classes des Acariens. Il ne s’agit donc pas d’insectes, à la différence, par exemple, des puces. (Un moyen simple de faire la différence : les insectes ont trois paires de pattes, tandis que les arthropodes en ont quatre). Les tiques appartiennent à l’ordre des Ixodida, du grec ancien ixôdês qui signifie gluant – autant dire que ce n’est pas d’aujourd’hui que l’on trouve ces bestioles répugnantes !
On dénombre plus ou moins neuf-cents espèces de tiques dans le monde, dont (seulement !) une quarantaine en France. Alors on ne va pas parler des quarante espèces dans cet article, parce que sans vouloir vexer nos amis pigeons et chauves-souris, l’étude d’Argas reflexus et d’Argas vespertilionis, qui parasitent respectivement ces deux groupes de volatiles, présenterait peu d’intérêt dans un article consacré aux tiques du chien et du chat. On se limitera donc à l’étude des trois principales espèces de tiques qui parasitent nos carnivores domestiques en France métropolitaine, à savoir la « tique brune du chien » Rhipicephalus sanguineus, Ixodes ricinus et Dermacentor reticulatus.
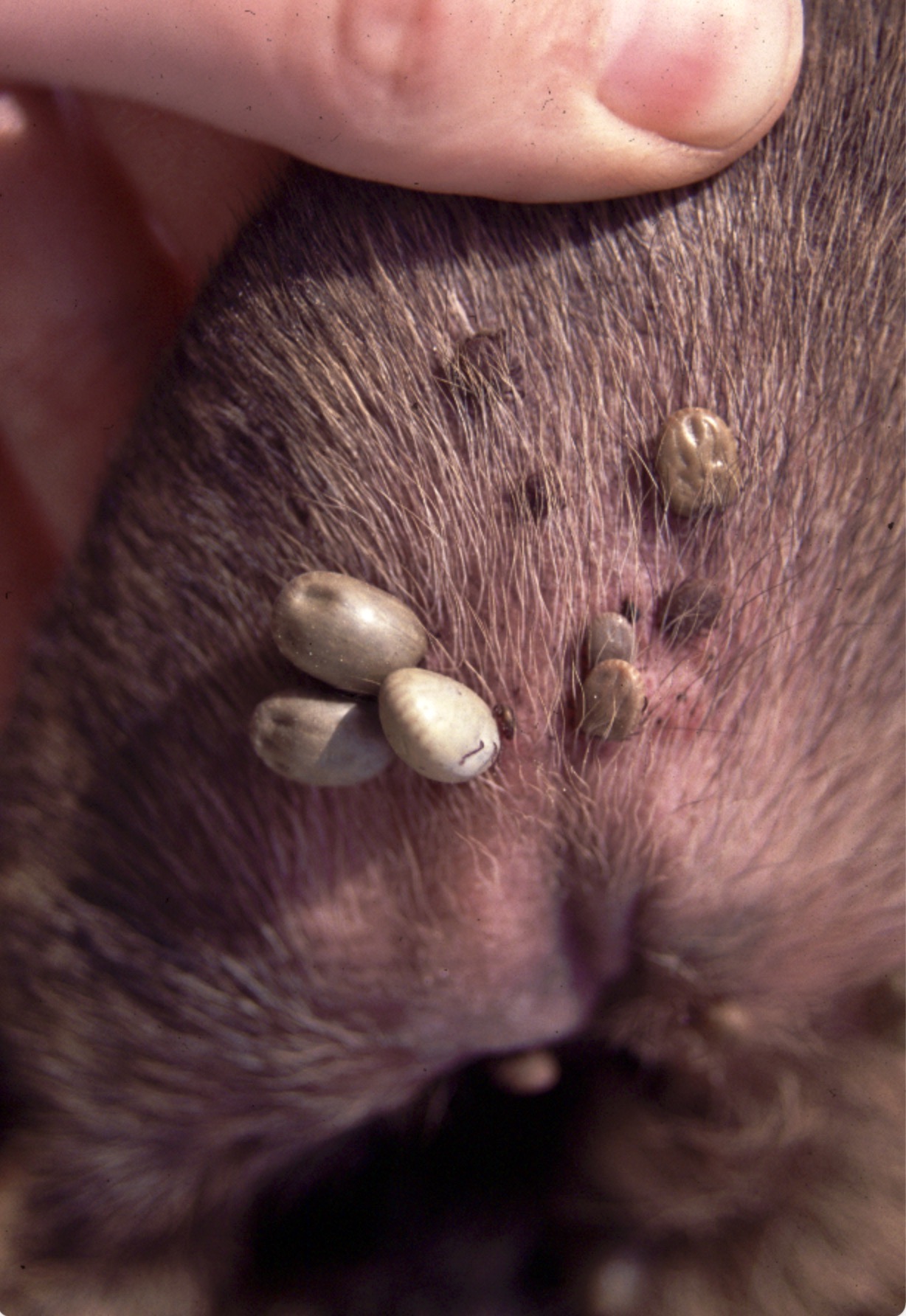
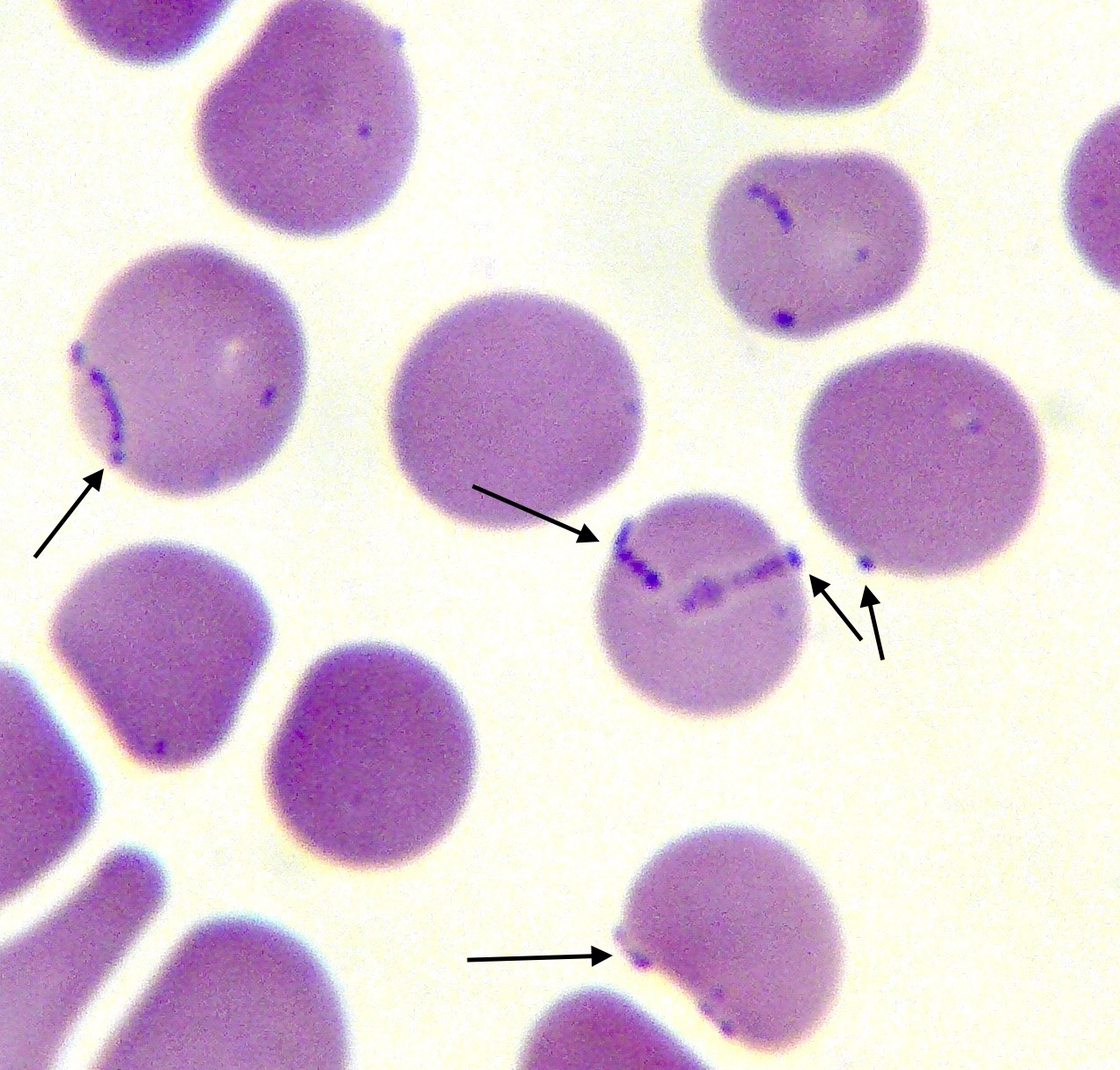
Photo de gauche : à table ! Deux tiques Rhipicephalus sanguineus surprises en plein repas, sur l’oreille d’un chien. L’une des deux est déjà bien gorgée ! A droite : quatre formes immatures de tiques dans le pavillon de l’oreille d’un chat (quand même, il n’y a pas de raison !)
Où, quand, comment ?
Si l’on veut lutter efficacement contre les tiques, et anticiper les différents problèmes qu’elles peuvent causer à nos chiens et, dans une moindre mesure, à nos chats, il est nécessaire d’en savoir un minimum sur leur mode de vie : où elles se trouvent, quand elles se montrent, et comment elles s’y prennent pour se nourrir et se reproduire. Quelques éléments de réponse ci-dessous.
Où ?
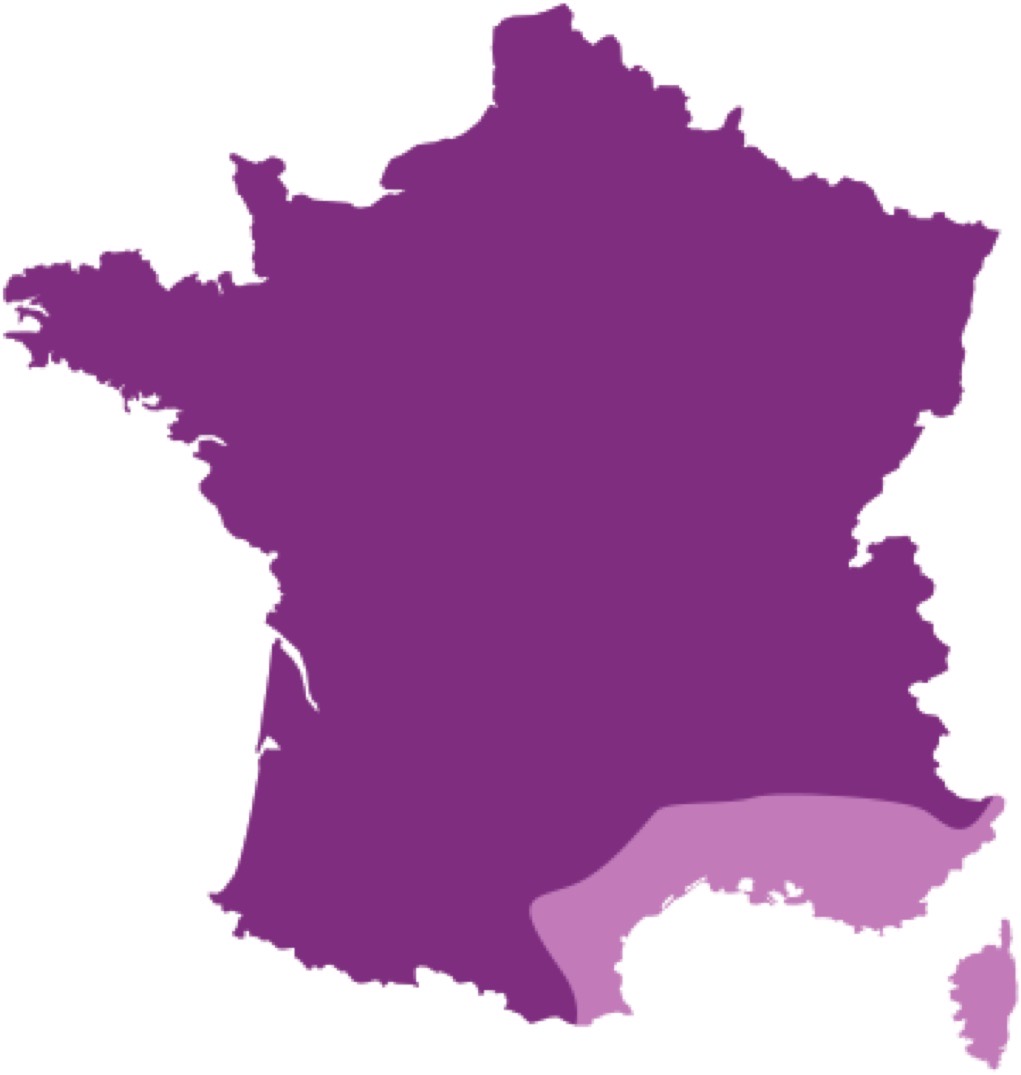
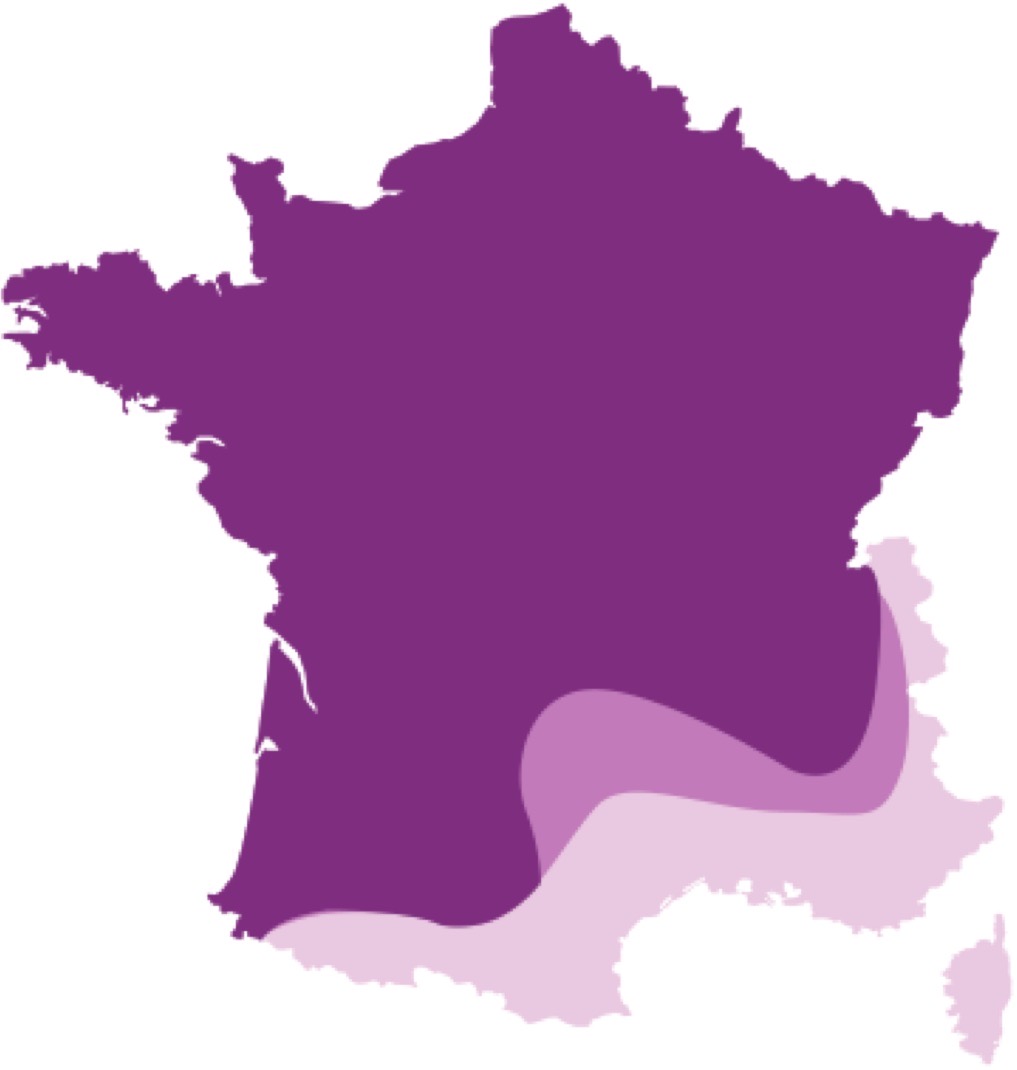
Les trois espèces de tiques qui nous intéressent ne sont pas réparties de façon uniforme sur le territoire métropolitain. En schématisant (un peu), on pourrait dire que Rhipicephalus sanguineus se rencontre surtout dans le sud, et Ixodes ricinus et Dermacentor reticulatus partout ailleurs. (Voir les cartes ci-dessous pour nuancer un peu). Il y a une explication à cela : Rh. sanguineus est ce qu’on appelle une tique xénophile, qui vit dans les zones chaudes et craint le gel, tandis que les deux autres sont des tiques hygrophiles, qui recherchent plutôt le froid (surtout I. ricinus) et l’humidité (surtout D. reticulatus), et craignent les fortes chaleurs et la dessiccation.
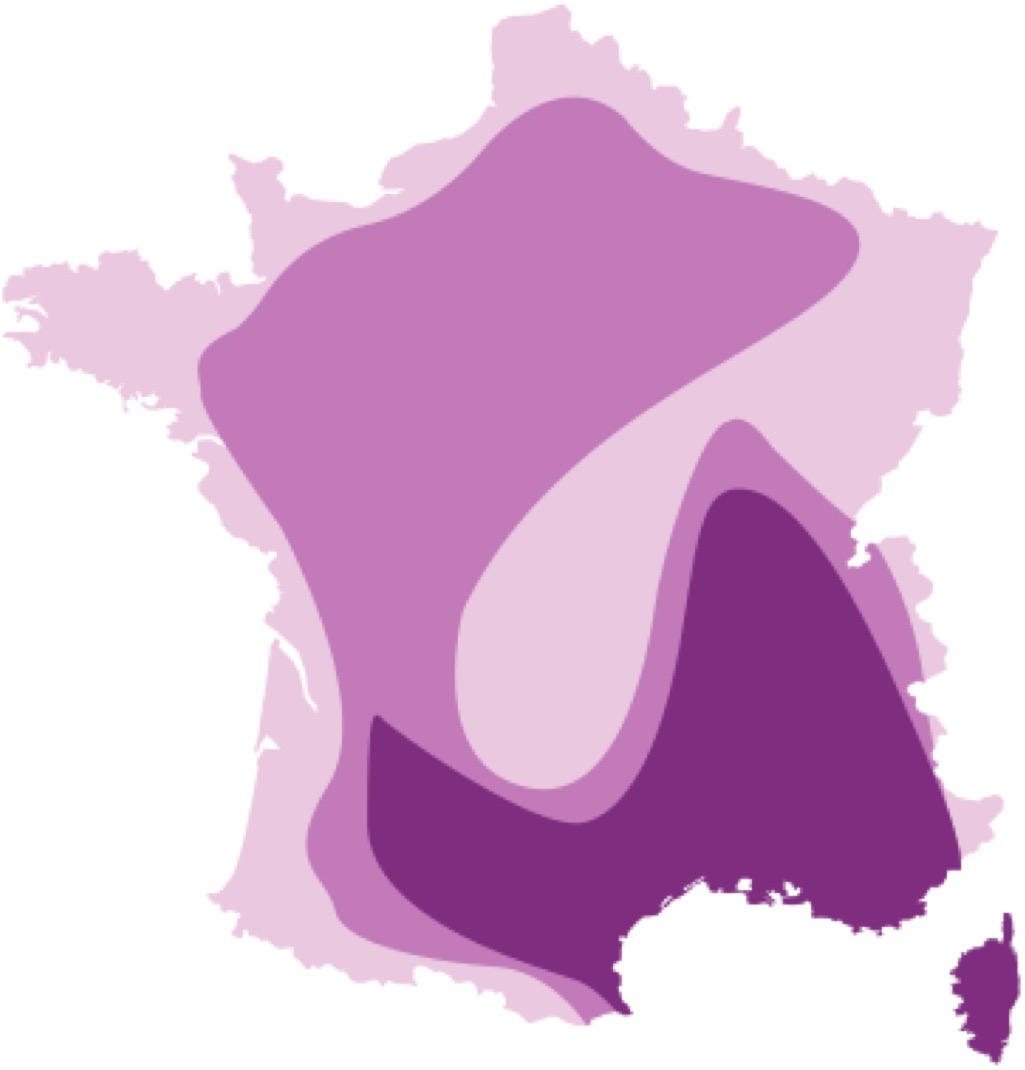
Répartition géographique d’Ixodes ricinus (ci-dessus à gauche), Dermacentor reticulatus (ci-dessus à droite), et Rhipicephalus sanguineus (ci-contre). Plus c’est foncé, plus il y en a ! (d’abondant à sporadique).
Cartes tirées du site de l’ESCCAP (European Scientific Counsel Companion Animal Parasites), où vous trouverez toutes les informations (en français) que vous cherchez sur les principales parasitoses internes et externes des animaux de compagnie, mais aussi de l’Homme dans sa relation à l’animal. (Image ESCCAP France)
Concernant nos tiques à nous, les résultats d’une enquête menée dans le Gard entre janvier 2010 et mai 2012 (M. René-Martellet & coll, 2015) ont montré que les tiques collectées sur les chiens dans des cliniques vétérinaires du département étaient à 100% des Rh. sanguineus ! Ce qui aura, on le verra plus loin, des conséquences sur le type de maladies que nous rencontrons chez nos patients.
Et puis à un niveau encore plus local, chaque tique a aussi ses petites habitudes, et on ne les trouvera pas toutes aux mêmes endroits : c’est ainsi que Rh. sanguineus est également appelée « tique des chenils », du fait de sa capacité à coloniser les habitations – on la trouve aussi dans les jardins : on parle de tique endophile. Contrairement aux deux autres, qui se retrouvent plutôt dans les prairies, terrains vagues, haies et berges de rivières pour Dermacentor reticulatus, et dans les forêts de feuillus et les sous-bois pour Ixodes ricinus. Sans oublier que chez ces deux tiques exophiles, si les adultes vivent effectivement au grand air, on trouvera plus volontiers les larves et les nymphes à l’intérieur des terriers de petits mammifères : hérissons, rongeurs, lapins…
Quand ?
Surtout au printemps et à l’automne (voire fin d’été)… mais il peut y en avoir toute l’année ! Il nous est ainsi arrivé de trouver, en janvier, des cas de piroplasmose, (maladie transmise par Rh. sanguineus, dont l’incubation n’est que de quelques jours), ce qui veut dire que les chiens venaient d’être piqués. Une enquête déjà citée plus haut, menée dans le Gard entre janvier 2010 et mai 2012, a montré une corrélation entre le nombre de tiques collectées sur des chiens dans des cliniques vétérinaires (pour rappel, 100% de Rh. sanguineus), et les températures extérieures (graphique ci-dessous). Globalement, les tiques ont surtout été trouvées sur les chiens entre mars et septembre.

Corrélation entre le nombre de tiques collectées et les températures extérieures dans le Gard, entre janvier 2010 et mai 2012. Source : M. René-Martellet & coll : Piroplasms of dogs and R. sanguineus ticks in southern France: epidemiological aspects and evolutionary perspectives (2015).
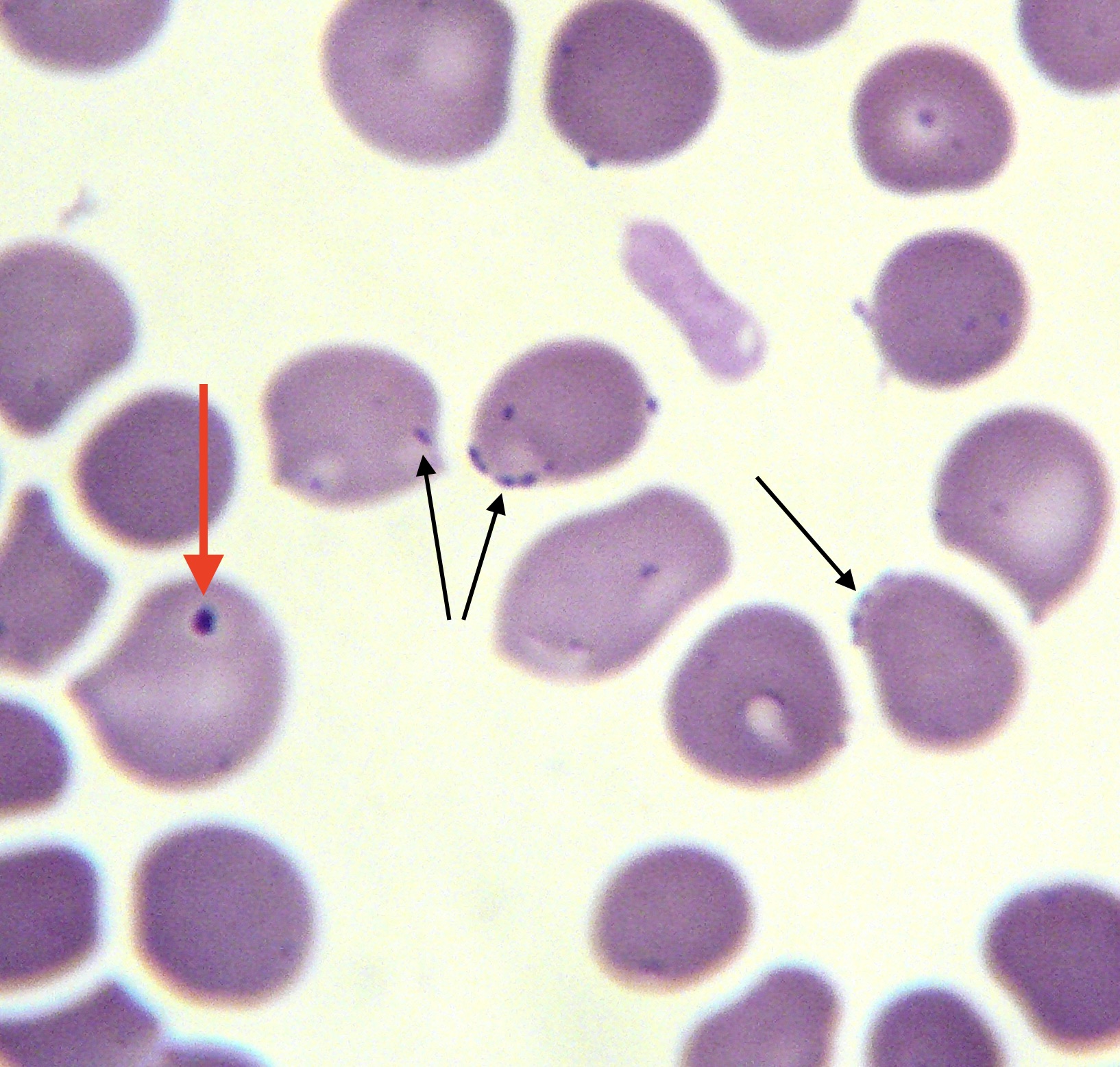
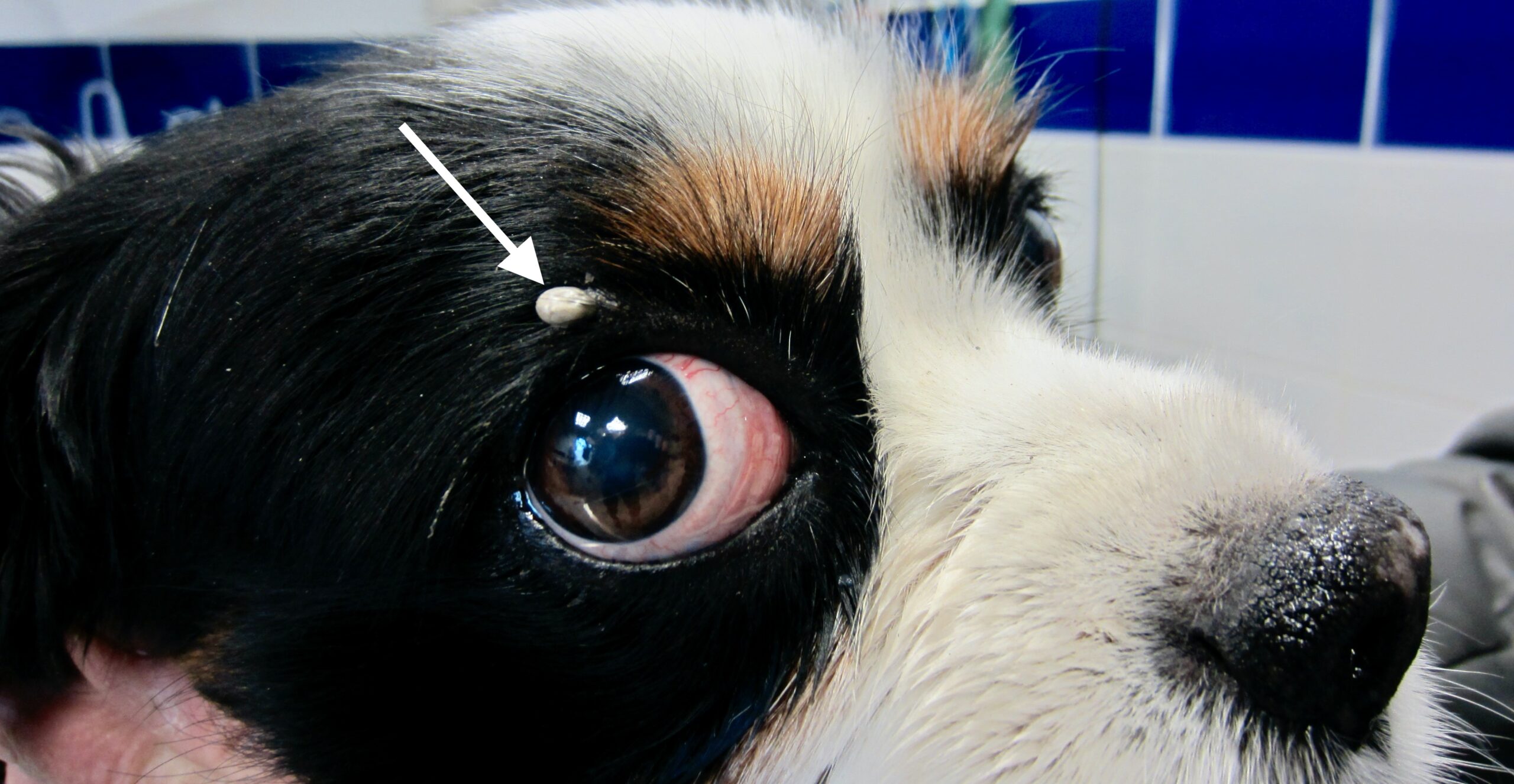
A chaque règle ses exceptions : la petite tique surprise en train de se planter dans l’oreille d’un chat (ci-dessus à gauche), a été photographiée un 9 février. Et celle qui gambade sur la photo de droite, un 14 février. Quand à celle plantée au-dessus de l’œil du gentil Cavalier King Charles ci-dessous, elle a été surprise en pleine action un 29 novembre. Comme quoi…
Comment ?
Alors, comment ça vit, une tique ? Ou pour faire court, comment ça se nourrit, et comment ça se reproduit ? (Non pas qu’il n’y ait que ça dans la vie, mais comme on a peu d’indices sur la vie intérieure et culturelle de la tique, on se limitera à ces deux aspects). Et au passage, savoir comment la tique mange nous dira comment elle transmet la plupart des maladies dont elle est le vecteur.
Comment elle se reproduit ?
D’abord, donc, le cycle : il n’est pas le même pour les plus de neuf-cents espèces de tiques existantes, mais dans la plupart des cas – et notamment chez les trois espèces qui nous intéressent – il s’agit d’un cycle triphasique, ce qui veut dire que chaque stade de la tique, (larve, nymphe et adulte), va grimper et prendre son repas sur un hôte différent.
Dans le détail… commençons par le commencement, quand Monsieur tique rencontre Madame tique. La rencontre se fera le plus souvent à l’occasion d’un dîner – en l’occurrence un repas sanguin. Pour Rh. sanguineus, ce sera sur un chien, plus occasionnellement un autres carnivore – dont le chat – ou un herbivore ; un grand ongulé (cheval, ruminant) ou accessoirement un chien pour D. reticulatus ; et pour I. ricinus, un herbivore ou un omnivore sauvage (cervidé, sanglier…) ou, dans une moindre mesure, un herbivore ou un carnivore domestique.

Les tiques repèrent leur hôte, et évaluent la distance qui les sépare, en utilisant l’organe de Haller, situé sur le tarse de leur première paire de pattes, grâce auquel elles détectent le CO2 (provenant de la respiration), les odeurs, la chaleur, les vibrations… Ensuite, elles n’ont « plus qu’à » grimper dessus : certaines chassent à l’affût en haut d’un brin d’herbe, (c’est le cas d’Ixodes et de Dermacentor, dans leur forêt ou leur prairie), d’autres chassent plus activement… et elles peuvent courir vite ! C’est le cas de Rhipicephalus, qui vit déjà dans la maison ou le chenil et peut donc grimper directement sur sa proie, qu’elle a à disposition, à domicile. (Photo ci-contre : une tique à l’affût sur son brin d’herbe – document Mérial).
Une fois sur l’hôte, Monsieur est attiré par des phéromones émises par Madame. Tous deux copulent… parfois en mangeant ! Ce repas sanguin peut être l’occasion pour les tiques d’échanger quelques agents pathogènes, via le site d’alimentation commun. (A noter que les tiques de certaines espèces redescendent après le repas, et la copulation se produit alors sur le sol). La maturation des ovocytes fécondés commence déjà pendant le repas de la femelle, qui dure en moyenne 5 à 7 jours. Après, elle se laisse tomber au sol, trouve un coin pour se cacher, et commence à pondre – entre 1 000 et 15 000 œufs ! – dans les 48-72 heures. Au passage, l’extrémité antérieure (le capitulum) de Madame tique se déchire, et elle meurt. Monsieur tique, lui, est déjà décédé après l’accouplement. Franchement, ça ne donne pas envie !
Après 30 à 50 jours, l’œuf éclot, et il en sort une larve molle à six pattes, ce qui la différencie des nymphes et des adultes, avec leurs quatre paires de pattes. Après quelques jours et une chitinisation qui la rend un peu moins molle, la larve se cherche un hôte sur lequel elle va grimper et prendre un unique repas sanguin avant de retourner au sol. Ce repas lui permet de muer en une nymphe qui va à son tour monter sur un hôte et y prendre un unique repas sanguin, avant de retourner, elle aussi, sur le sol et de muer, cette fois, en adulte – ce qui nous ramène au point de départ du cycle. Tout cela ci-dessous, en images.
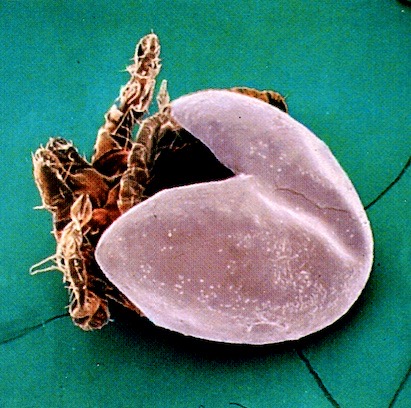

A gauche : l’éclosion de l’œuf (document Mérial). Ci-dessus : vue au microscope d’une larve de Rh. sanguineus avec ses trois paires de pattes, qui la distinguent des nymphes et des adultes.
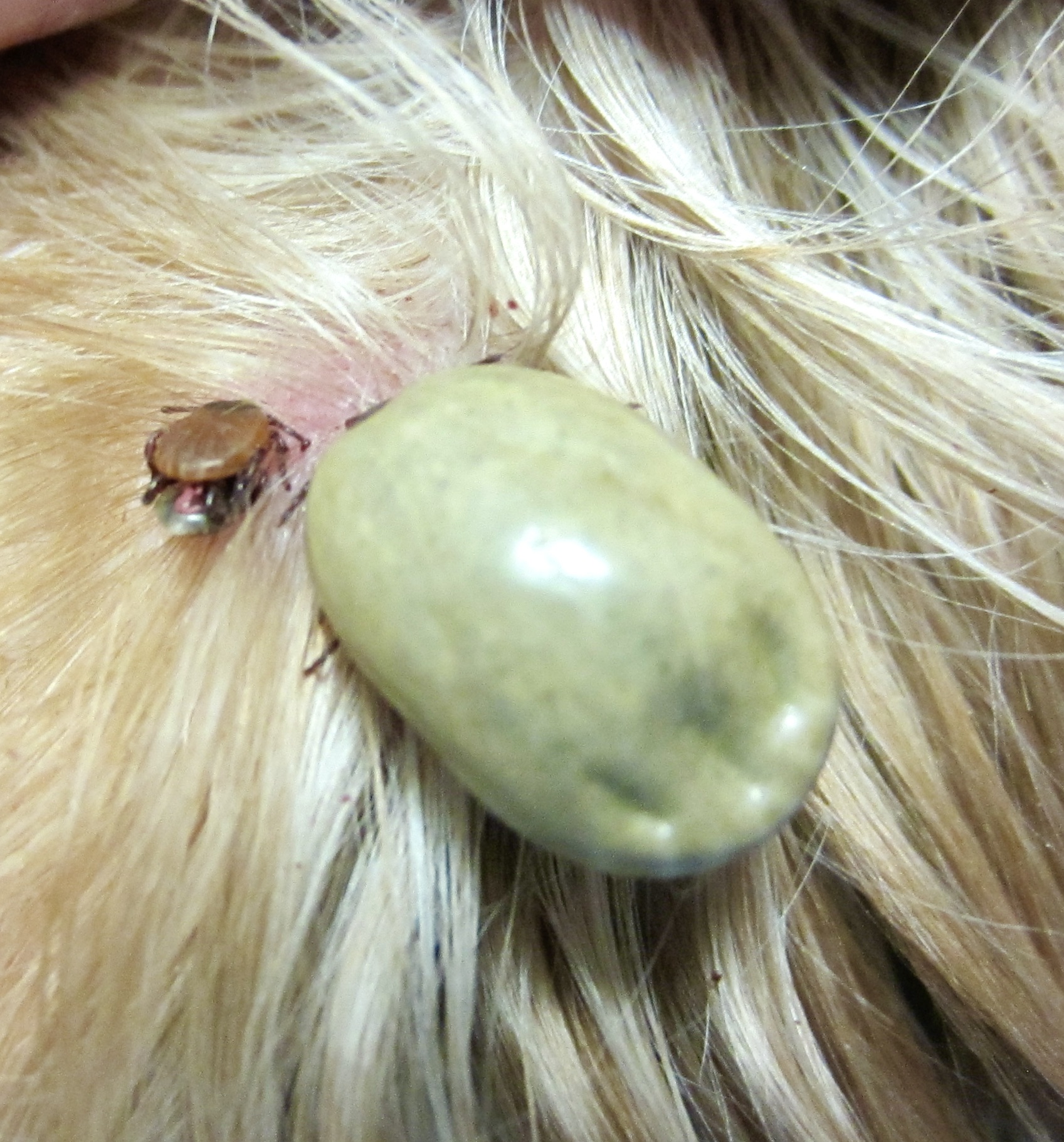
A gauche : une tique Rhipicephalus sanguineus adulte. La femelle adulte mesure 3-4 mm à jeun, mais une fois gorgée, elle dépasse allègrement le centimètre. A droite : des « plombs », appellation qui désigne communément les formes immatures, du fait de leur ressemblance avec… des plombs de chasse. Il s’agit ici de nymphes, ainsi qu’en témoignent leurs quatre paires de pattes. Les plombs mesurent généralement dans les 2-3 mm, et on les rencontre plutôt en fin d’été ou en automne. On en reparlera un peu plus loin, dans la partie consacrée aux dégâts causés par les tiques.
A noter que les trois hôtes (de la larve, de la nymphe et de l’adulte), n’appartiennent pas toujours à la même espèce. Chez I. ricinus et D. reticulatus, on l’a vu, les formes immatures (larve et nymphe), vivent habituellement dans des terriers de petits mammifères, qui seront donc souvent leurs victimes naturelles. Les adultes, eux, choisiront des hôtes plus conséquents : vache, cheval, sanglier, chien… On parle de tiques ditropes ou télétropes, selon la variété plus ou moins large d’hôtes possibles à chaque stade. Au contraire, chez Rh. sanguineus, tous les stades sont attirés par le même hôte, à savoir en priorité le chien : on parle dans ce cas de tique monotrope.
La durée complète du cycle est très variable, en fonction notamment des conditions extérieures : si tout va bien, qu’il fait beau et que la nourriture (les hôtes) est abondante, alors la tique est contente : elle mange pendant une semaine, tombe au sol, mue en 3-4 jours, après quoi il lui faut juste le temps de trouver un nouvel hôte… et le cycle complet est bouclé en deux mois. En revanche, s’il fait froid, ça peut être beaucoup plus lent : dans des conditions défavorables, le passage d’un stade à l’autre chez I. ricinus peut prendre un an, soit trois ans pour le cycle complet. Ce qui signifie au passage que si une larve de tique arrive quelque part porteuse de Babesia canis (l’agent de la piroplasmose du chien), sachant que les Babesia se transmettent d’un stade à l’autre, et même d’une génération de tique à l’autre en passant par les œufs, et qu’en plus I. ricinus peut se nourrir sur d’autres animaux que les chiens, (notamment les petits mammifères)… alors les tiques peuvent servir de réservoir pour la piroplasmose dans un secteur pendant pas mal d’années, même en l’absence de chien !
Comment elle mange… et contamine ?
Quand elle arrive sur un hôte, (un chien ou un chat, pour ce qui nous intéresse), soit du haut de son brin d’herbe, soit après une chasse active, la tique s’accroche grâce à un organe collant présent sur ses tarses, (le bout de la patte, en gros), puis commence à ramper entre les poils, au moyen de ses pattes couvertes de petits poils épineux et dotées d’une griffe à leur extrémité – le même équipement qui lui a permis de grimper sur un brin d’herbe. Elle chemine ainsi pendant une moyenne de quatre à six heures, jusqu’à trouver le coin qui lui convient, à savoir, tant qu’à faire, une zone à peau fine : oreilles (l’endroit préféré des Rhipicephales), régions axillaire et inguinale (les dessous de bras, quoi), scrotum et mamelles.
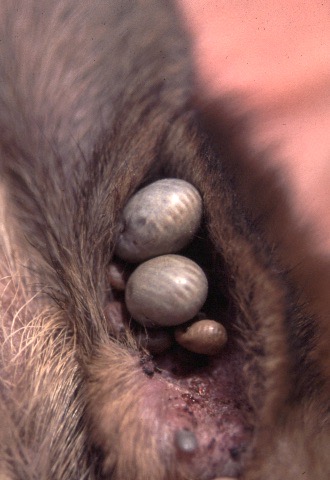
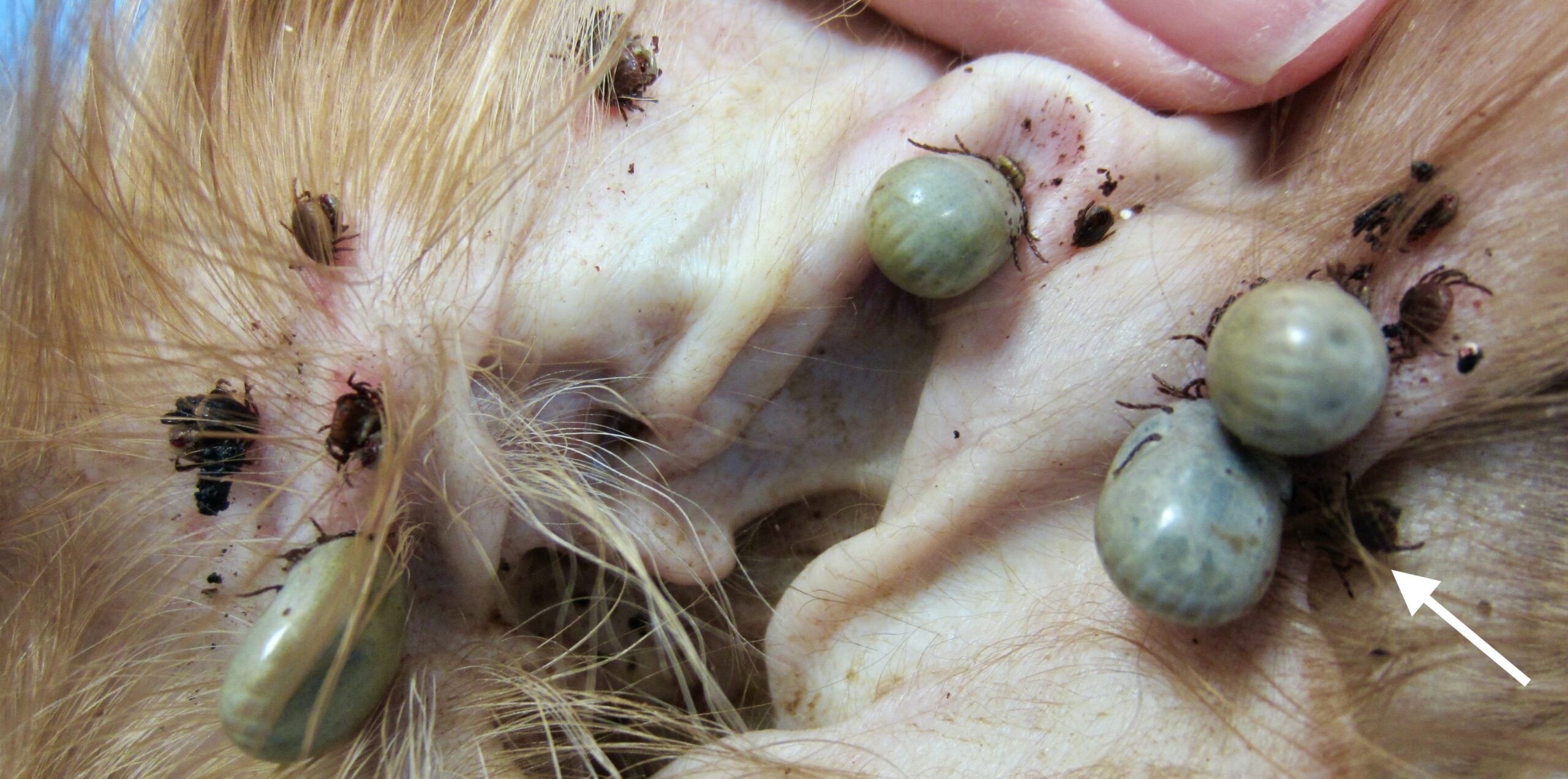
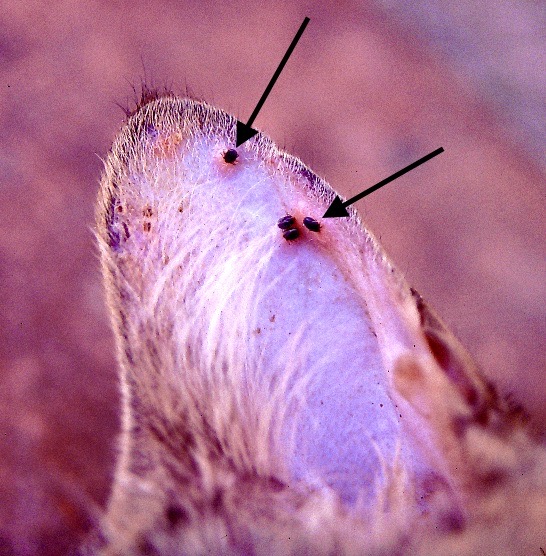
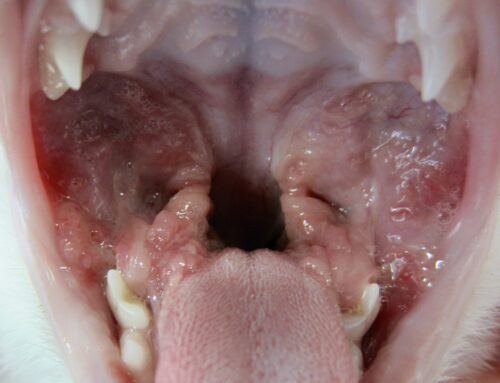
La face interne du pavillon de l’oreille, le nirvana pour Rhipicephalus sanguineus. Mention spéciale pour l’oreillon = le petit repli de peau à la base et à l’arrière du pavillon : occupé par toute une famille de Rhipicéphales sur la photo en haut à droite, et marqué par une flèche blanche sur la photo ci-dessus. Quand il n’y a pas beaucoup de tiques, c’est souvent là qu’il faut aller les chercher !
Après, il ne reste plus qu’à se planter. La tique repère le bon endroit avec ses pédipalpes, attrape et pénètre la peau avec ses chélicères qui ressemblent à deux petits harpons, les rétracte pour que la peau prenne une incidence oblique, plus facile à perforer pour l’hypostome, par lequel transiteront la salive de la tique dans un sens, et le sang de la victime dans l’autre. (Quand on voit ce genre de chose, on ne sait pas si on doit vraiment s’en réjouir, mais on ne peut s’empêcher de penser que la nature est vraiment bien faite !) La tique sécrète alors un cément pendant 10 à 30 minutes, et la voilà solidement arrimée à la peau. Le festin peut commencer !
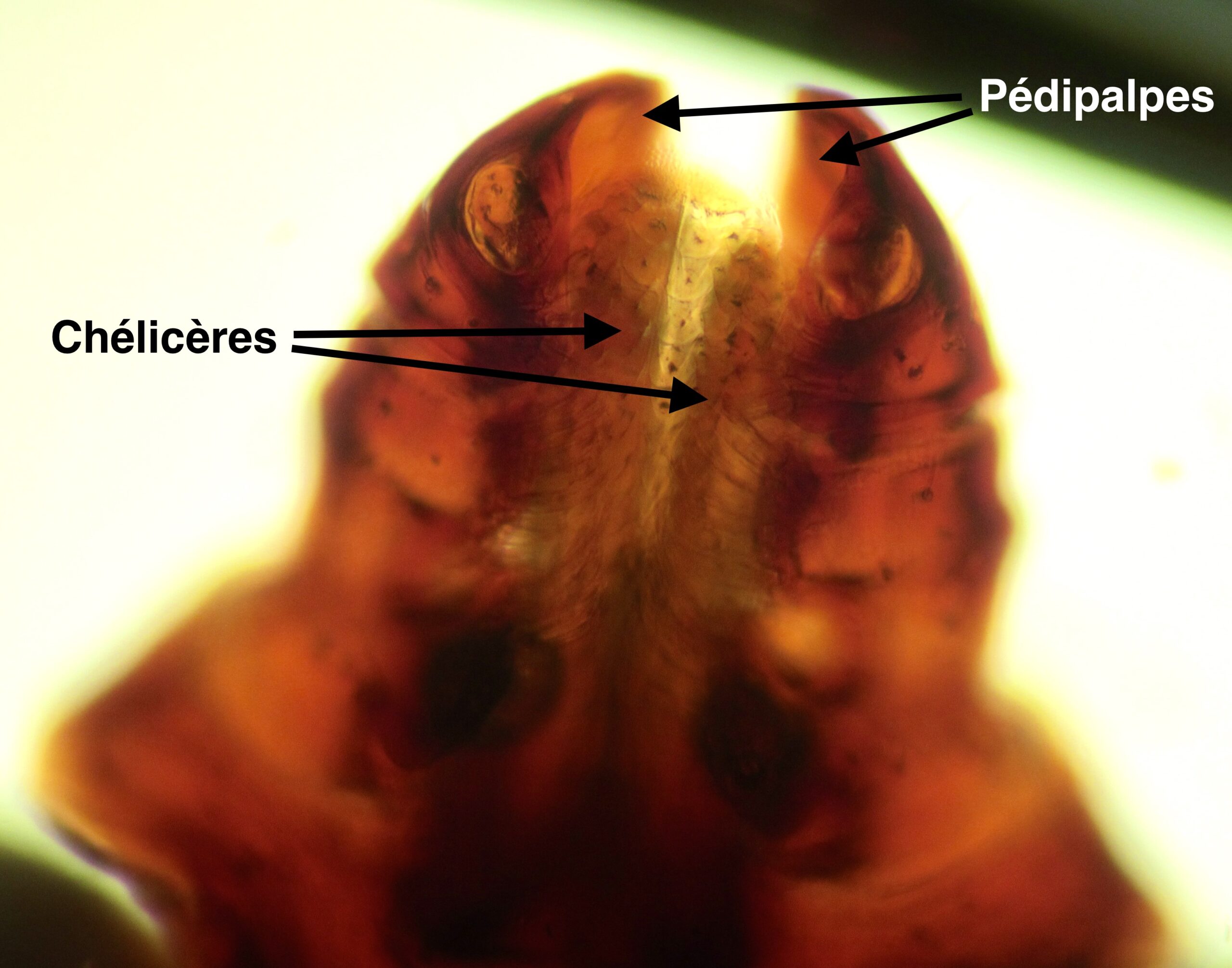
Photo ci-dessus : aspect microscopique du capitulum (la tête, quoi), d’une tique Rhipicephalus sanguineus adulte, avec pédipalpes à l’extérieur et chélicères à l’intérieur.
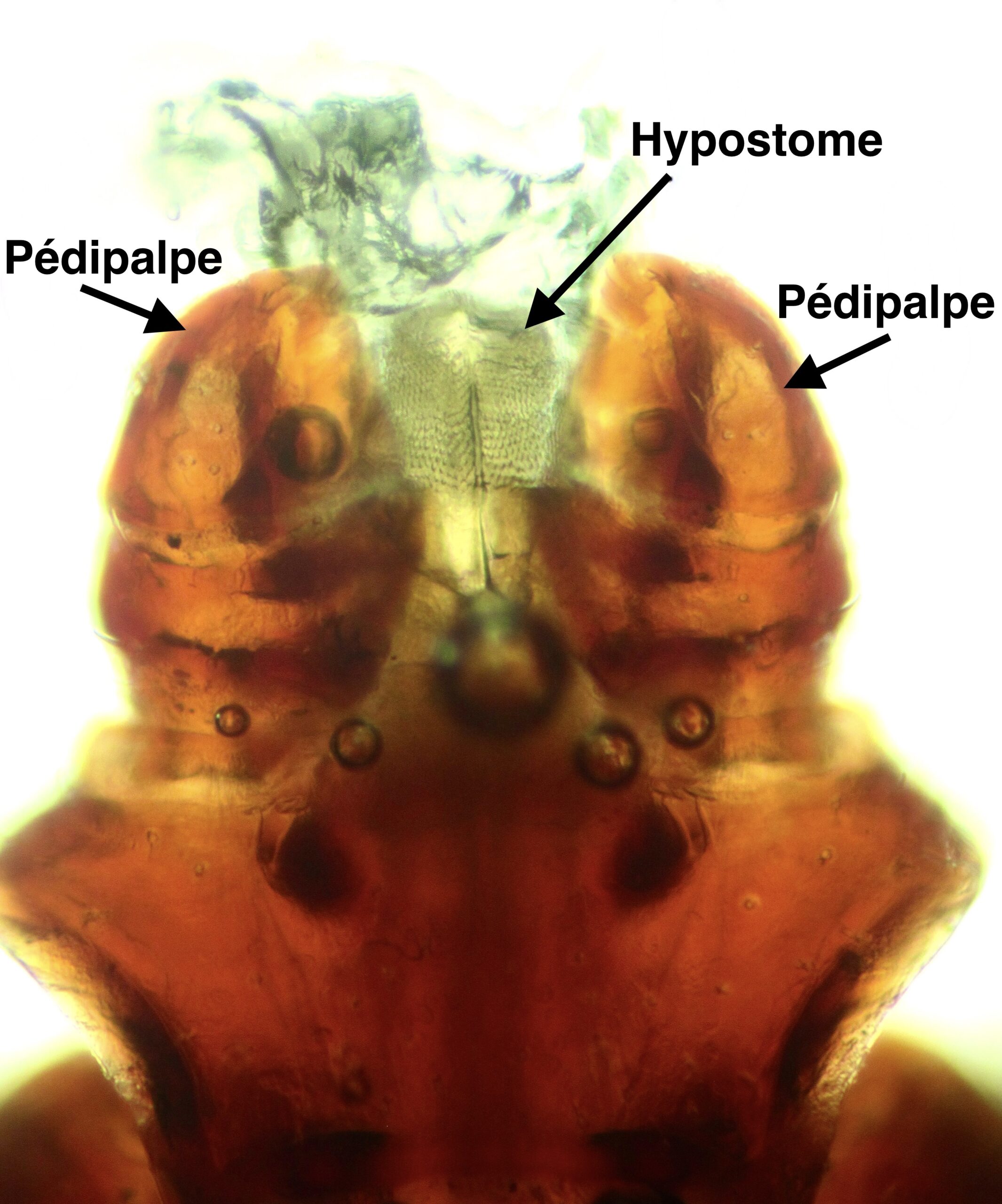

Ci-dessus à gauche : capitulum d’une larve de Rhipicephalus sanguineus, reconnaissable à sa forme hexagonale, dite en casque de Dark Vador (ci-dessus à droite) : effectivement, la ressemblance est frappante ! L’hypostome est bien visible entre les deux pédipalpes, il reste même un peu de chien accroché au bout (enfin… de tissu cutané ou sous-cutané de chien).
Celui-ci se déroule en deux étapes : une phase préparatoire qui dure au moins trois jours, pendant laquelle la tique sécrète toutes sortes d’enzymes et de peptides (= petites protéines), qui auront pour effet d’empêcher la coagulation du sang de l’hôte (pour le rendre plus facile à avaler !), d’attirer des globules blancs et de provoquer une nécrose des tissus là où la tique est implantée. A ce stade, le parasite a déjà ingéré un peu de sang et de tissus digérés, mais tout cela va s’accélérer pendant la seconde phase où, en 24-48 heures, le poids de la tique va passer de 50 à 250 grammes ! (contre 2 à 50 pendant la première phase). Globalement, le repas dure de 3 à 5 jours pour les larves et les nymphes, et de 5 à 7 jours pour les adultes.
C’est pendant tous ces échanges de fluides que les agents pathogènes vont passer de la tique à sa malheureuse victime. Ceux qui sont déjà présents dans la salive et immédiatement infectieux (en l’occurrence les virus), pourront être inoculés dans les 15 minutes suivant la fixation. Les bactéries également déjà présentes dans la salive et immédiatement infectieuses (Ehrlichia, Anaplasma, Rickettsia…), passeront, elles, dans les premières 8 à 24 heures (3 heures pour Ehrlichia canis !). Ce sera un peu plus long pour les agents devant encore se multiplier, gagner les glandes salivaires et/ou devenir infectieux : c’est le cas de Borrelia burdorferi (responsable de la maladie de Lyme : transmission 36 à 48 heures après la morsure), et de Babesia (48 à 96 heures). Et puis n’oublions pas que pendant les phases d’aspiration, c’est la tique qui s’infecte si son hôte était porteur de Babesia, d’Ehrlichia, ou autres créatures indésirables.
Les affections dues aux tiques
L’effet pathogène direct
L’anémie par spoliation :
L’effet direct le plus évident, c’est logiquement la spoliation sanguine. Bon, c’est sûr qu’avant que les tiques pompent suffisamment de sang à un chien pour mettre sa vie en danger, il en faut pas mal : deux ou trois sur un bouvier bernois ne risquent pas de le saigner à blanc. En revanche, si un chien de taille petite ou moyenne est envahi par des centaines de tiques, ça peut être plus problématique. Bien que rare, c’est un cas de figure que l’on rencontre notamment en fin d’été, lorsqu’on voit sortir les plombs dont on a déjà parlé, qui sont les formes immatures issues de la ponte des tiques adultes qui ont sévi au printemps. Et là, pour le coup, on peut vraiment en trouver des centaines sur un chien… voire des milliers !

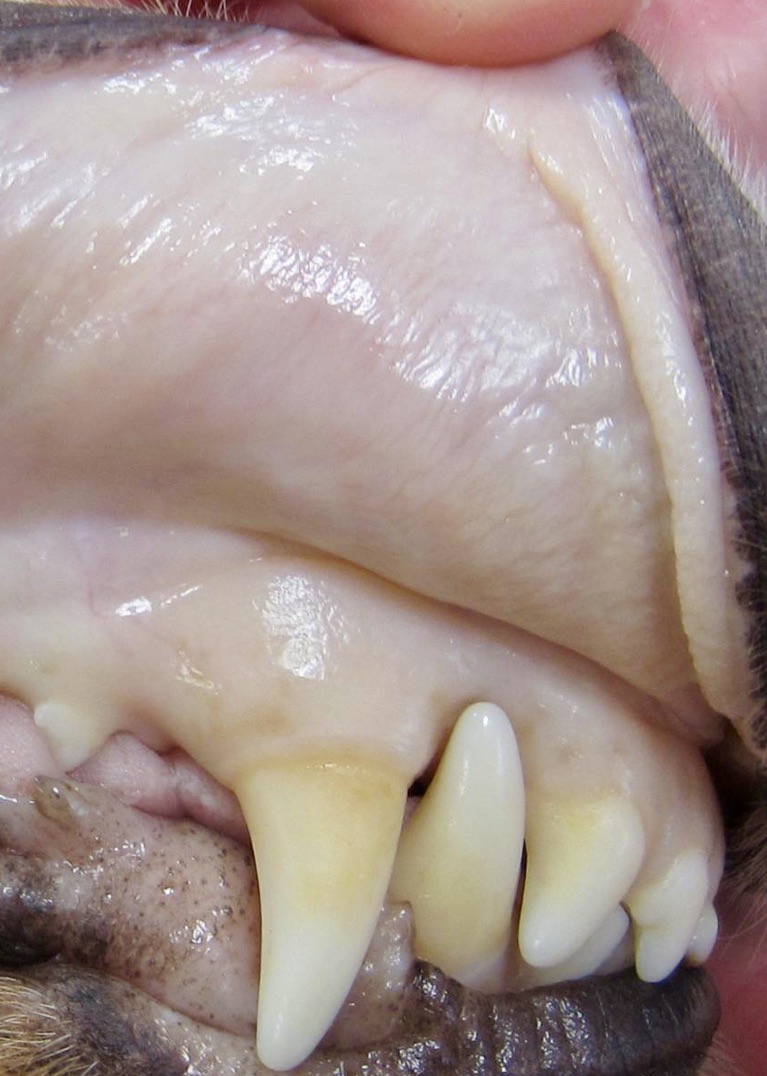
En haut à gauche : tiques adultes bien gorgées, sur la face interne du pavillon de l’oreille d’un chien (photo prise au mois de mars). Nombreuses, mais sans doute pas de là à « saigner » le chien. Ci-dessus : quelques plombs parmi les centaines ou milliers observés sur un chien très lourdement parasité ; la photo a été prise fin juillet, il s’agit peut-être des nymphes issues des adultes de la première photo ! (NB : la lame de bistouri n’est là que pour donner une idée de la taille des plombs, pas plus gros (et de la même couleur) que des plombs de chasse – d’où leur nom). En haut à droite : le résultat de tout ça, avec cette muqueuse buccale bien pâlichonne chez un chien très anémié.
La production de toxines :
De véritables toxines sont présentes dans la salive de certaines tiques. Ces toxines vont se fixer sur les neurorécepteurs des chiens, et provoquent une paralysie ascendante. La forme la plus connue est la « paralysie à tiques » due à Ixodes holocyclus en Australie, dont plusieurs milliers de cas sont décrits chaque année chez le chien, un certain nombre se terminant par le décès de l’animal, du fait notamment d’une atteinte respiratoire. Des affections similaires sont décrites sur le continent africain et en Amérique du nord. Il nous est arrivé d’observer quelques fois, en été, des paralysies ascendantes (paralysies flasques avec perte des réflexes, mais pas de la sensibilité), commençant par les membres postérieurs avant de gagner en quelques jours la partie antérieure du corps, chez des chiens infestés par des tiques. La plupart ont fini par guérir après retrait des tiques et administration d’un traitement symptomatique… sans que nous ayons pu savoir s’il s’agissait réellement de paralysies à tiques, ou d’une autre affection neurologique chez des chiens qui se trouvaient par hasard être porteurs de tiques.
La transmission d’agents pathogènes
Voilà la partie que tout le monde attend, (enfin, c’est du moins ce qu’on suppose), parce que savoir combien d’œufs pond Madame Tique, c’est sans doute passionnant, mais le plus intéressant, c’est quand même les maladies que ces bestioles peuvent transmettre à nos compagnons à quatre pattes.
On dira un mot de ces différentes maladies, mais on ne les décrira pas toutes en détail, parce que la plupart d’entre elles font (ou feront prochainement, on l’espère), l’objet d’un article séparé sur ce site. Même chose pour les maladies vectorielles du chat : elles sont détaillées dans un article qui leur est entièrement consacré. Nous nous limiterons par ailleurs aux principales maladies que l’on peut rencontrer sous nos latitudes – même s’il serait sans doute captivant de s’attarder sur la fièvre pourprée des montagnes rocheuses (Rocky mountain spotted fever) due à Rickettsia ricketsii et présente essentiellement en Amérique du nord – mais bon…
Enfin, dernier détail à ne pas négliger : les tiques hébergent plein de parasites différents et se font une joie de tous les inoculer à la fois, si elles en ont la possibilité. Donc, ce n’est pas parce qu’on trouve une belle piroplasmose chez un chien qu’il n’a pas en plus une ehrlichiose, une hépatozoonose, etc.
La piroplasmose :
A tout seigneur tout honneur, la piroplasmose (ou babésiose, due à des parasites appartenant au genre Babesia), est la plus connue et la plus répandue des maladies transmises par les tiques en France métropolitaine. Comme indiqué ci-dessus, nous n’en dirons que quelques mots, vu qu’elle fait déjà l’objet d’un article détaillé sur ce site.
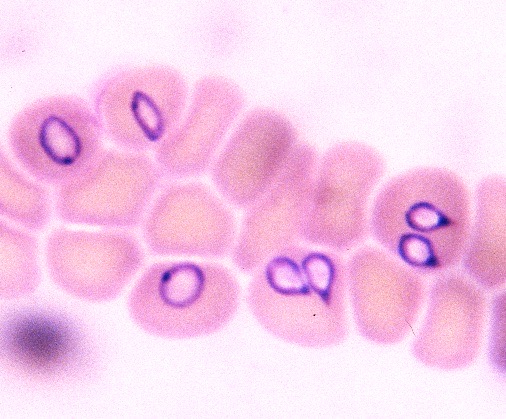
Photo de gauche : Anouck, montagne des Pyrénées de 1,5 an, atteinte de piroplasmose, abattue et anorexique depuis trois jours. Le jour de la consultation, elle est très abattue, éprouve des difficultés à rester debout, et crie dès qu’elle se déplace. A droite, les coupables, visibles sur un frottis réalisé à partir d’une simple goutte de sang : toutes ces petites images en forme de poire à l’intérieur des globules rouges sont des piroplasmes.
Il existe une centaine d’espèces de Babesia, mais les plus importantes pour le chien en France métropolitaine sont Babesia canis, transmise par Dermacentor reticulatus, et Babesia vogeli, prédominante dans le sud-est, transmise par Rhipicephalus sanguineus. La maladie est plus fréquente au printemps et à l’automne, et dans certaines régions, notamment le Sud-Ouest, le Centre, l’Est et la région parisienne. Les principaux symptômes sont peu typiques (abattement, anorexie, hyperthermie…), avec quand même des muqueuses pâles et des urines foncées dans la moitié des cas. Le diagnostic se fait le plus souvent facilement, sur frottis sanguin (photo ci-dessus). Chez la plupart des chiens – car il y a toujours, malheureusement, des exceptions – le traitement est simple et la guérison rapide. La prévention passe par les lutte contre les tiques (on y revient dans le chapitre suivant), et on dispose d’un vaccin.
Les ehrlichioses :
Là aussi, il existe pas mal d’espèces d’Ehrlichia, mais celle qui nous intéresse est avant tout Ehrlichia canis. Elle aussi fait l’objet d’un article à part sur le site.
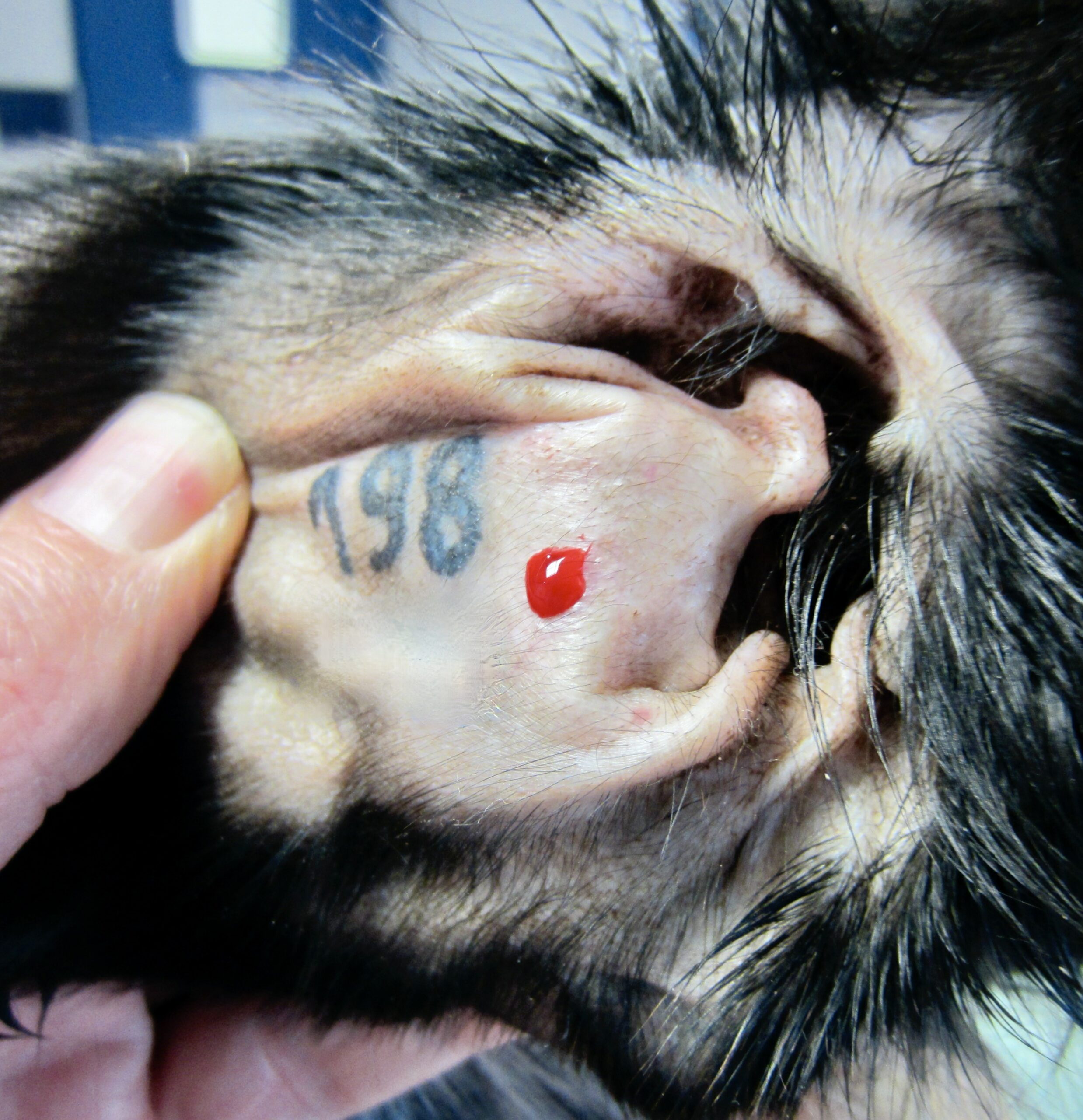
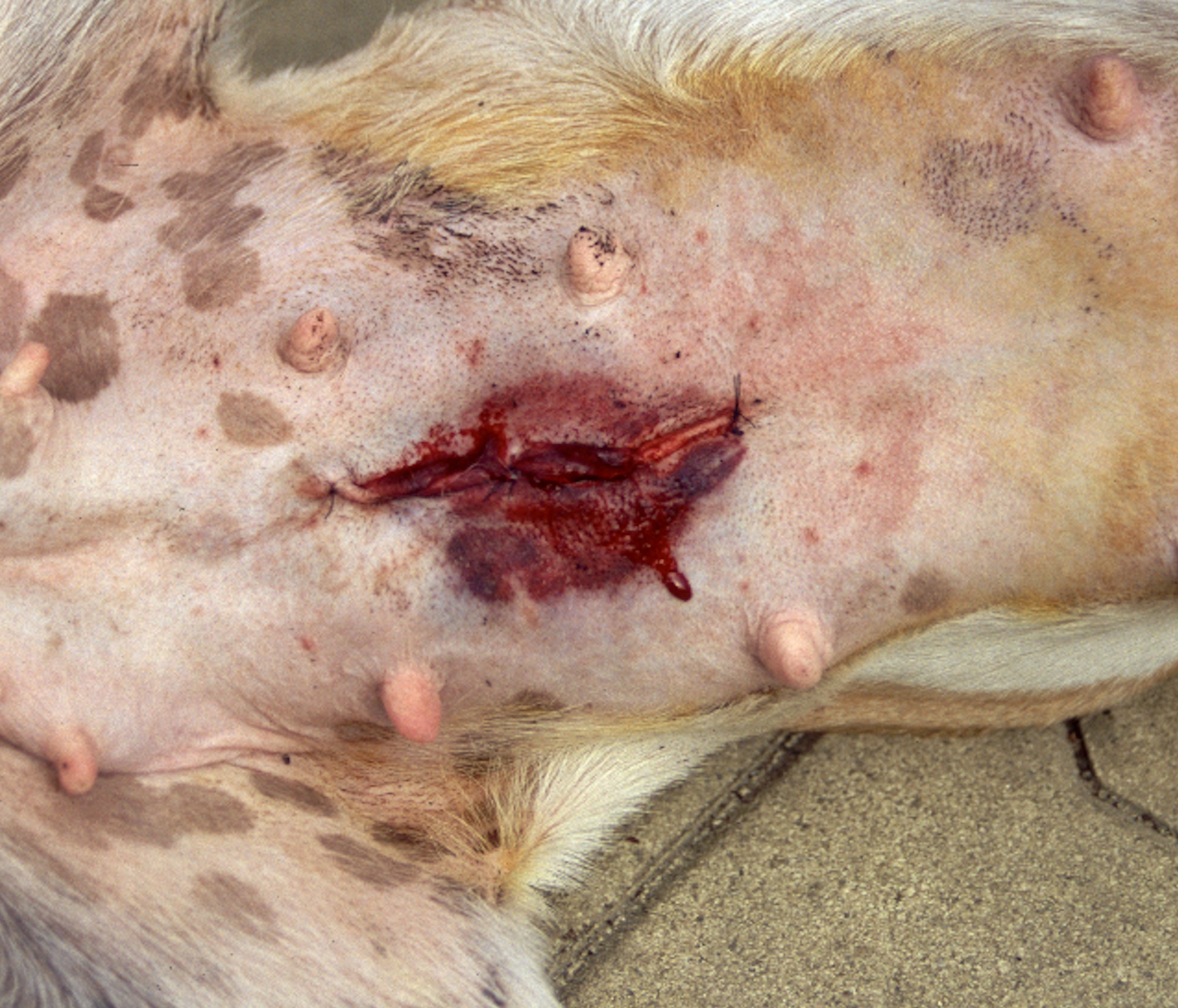
Trouble de l’hémostase chez un chien infecté par Ehrlichia canis : plusieurs minutes après avoir pratiqué une minuscule incision en face interne du pavillon d’une oreille, la petite plaie continue de saigner, et on peut voir que le sang n’est pas bien rouge, témoignant d’une anémie marquée. A droite, les responsables : deux morulas d’E. canis (flèches) dans le cytoplasme d’une cellule sanguine (ici, un lymphocyte).
Donc, Ehrlichia canis est une bactérie transmise par Rhipicephalus sanguineus. Elle se présente dans les cellules infectées (monocytes ou lymphocytes), sous la forme d’inclusions ressemblant à des mûres, que du coup on appelle morulas. Comme pour la piroplasmose, les symptômes sont souvent peu spécifiques (abattement, anorexie et hyperthermie dans les trois quarts des cas environ), mais certains, moins fréquents, sont aussi plus évocateurs, comme des saignements (par le nez, dans les urines ou par n’importe quelle petite brèche cutanée ou muqueuse … photo ci-dessus à gauche), saignements dus à une baisse du nombre et à un mauvais fonctionnement des plaquettes sanguines, responsables de l’hémostase. Le diagnostic se fait par mise en évidence de l’Ehrlichia au microscope (ci-dessus à droite), ou plus souvent par sérologie ou par PCR. Le traitement repose essentiellement sur un antibiotique (la doxycycline), mais la guérison, souvent rapide chez les chiens récemment infectés, peut s’avérer plus longue et difficile à obtenir lorsque l’infection est plus ancienne. La prévention repose essentiellement sur le contrôle des tiques, vu qu’il n’existe pas de vaccin.
Les anaplamoses :
Il y a quelques années, les Anaplasma actuelles étaient à peu près toutes classées parmi les Ehrlichia : Ehrlichia platys, qui se logeait dans les plaquettes sanguines du chien, Ehrlichia equi dans les granulocytes du cheval, Ehrlichia phagocytophila (l’agent de la Tick borne fever, ou fièvre des pâtures), dans ceux des ruminants, et l’agent de l’ehrlichiose granulocytaire humaine. Depuis une révision de la classification en 2001, E. platys est devenue Anaplasma platys, et les trois autres ont été regroupées au sein d’une même espèce : Anaplasma phagocytophilum.
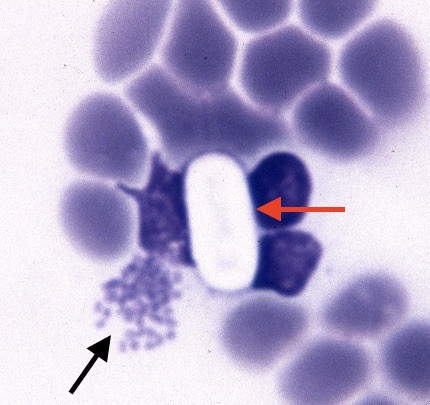
Chez nous, dans le Gard, nous rencontrons surtout Anaplasma platys, une bactérie qui se présente sous la forme de morulas un peu semblables à celles d’Ehrlichia canis (en plus petit), mais qui se loge dans les plaquettes sanguine. L’une des conséquences de l’atteinte des plaquettes est, bien sûr, un trouble de l’hémostase (photo ci-dessous), mais on observe aussi hyperthermie, abattement, anorexie et douleurs. Le plus souvent, A. platys est mise en évidence sur un frottis sanguin, mais quand on n’en trouve pas et qu’on suspecte sa présence, on peut demander une recherche sérologique ou, mieux, moléculaire par PCR. Le traitement par la doxycycline est généralement efficace.
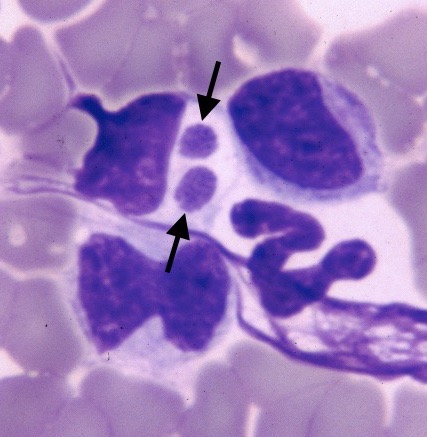
Photo de gauche : 24 heures après une stérilisation, la plaie chirurgicale de cette chienne est au centre d’un gros hématome et saignotte toujours, ce qui n’est pas normal du tout du tout du tout ! En outre, la chienne est abattue, fiévreuse… Un bilan sanguin, et notamment l’examen du frottis sanguin, a montré, outre un taux de plaquettes sanguines anormalement bas, la présence, dans ces mêmes plaquettes, de nombreuses morulas d’A. platys semblables à celles que l’on peut voir sur la photo de droite (flèches).
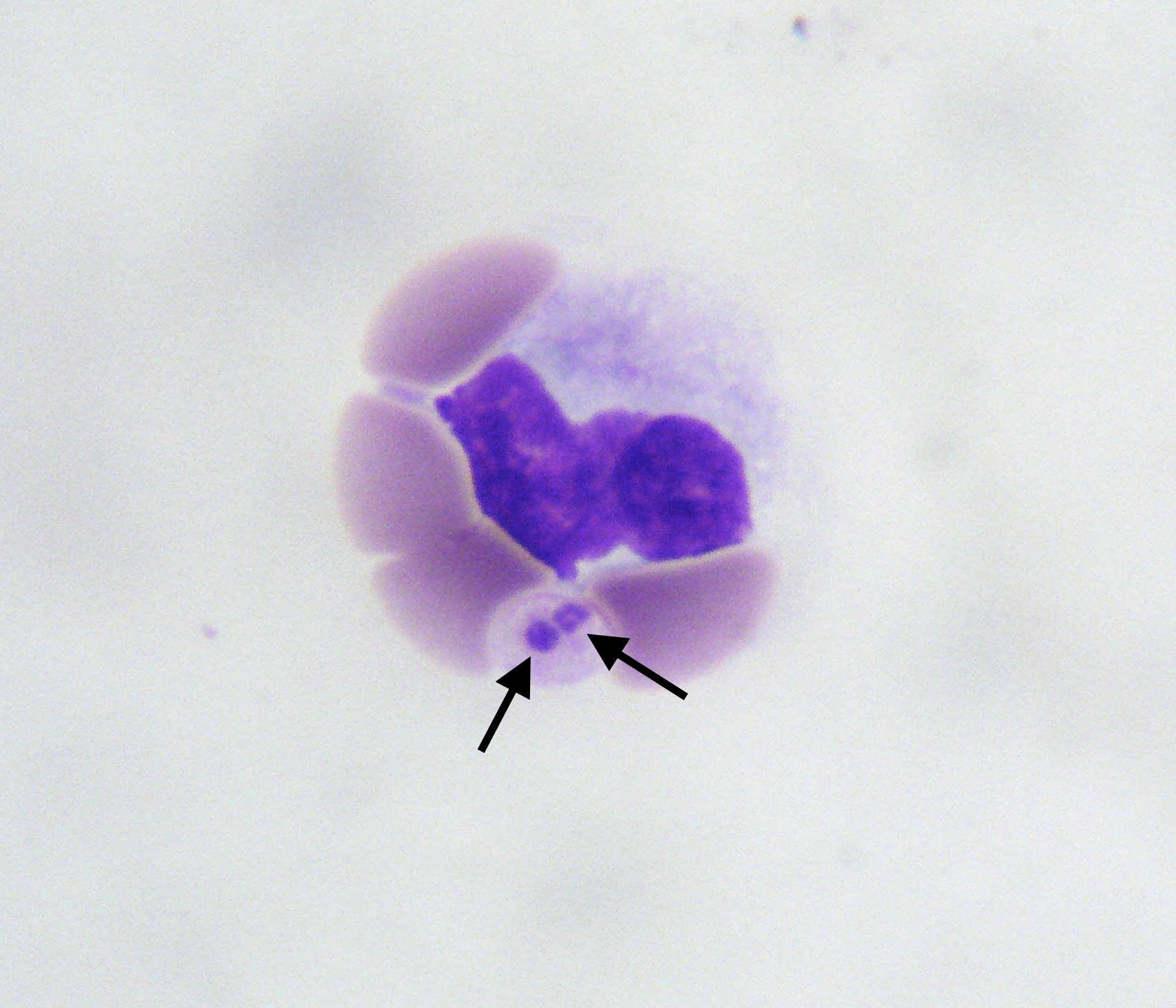
Un mot sur Anaplasma phagocytophilum, qui se présente sous la forme de morulas comme Ehrlichia canis, mais dans les granulocytes, et non les cellules mononucléées. Elle est transmise par la tique Ixodes ricinus, dans le nord de l’Europe : on la trouve plus souvent en Scandinavie, en Suisse, voire dans le nord de la France, que sur les berges de la Méditerranée ! On a quand même trouvé une fois, sur le frottis sanguin d’un chien, des morulas granulocytaires (photo ci-contre, une morula qui éclate : flèche noire), associées dans la même cellule à des gamétocytes d’Hepatozoon canis (flèche rouge, on en parle juste après). Mais comme c’était il y a très longtemps et que la PCR n’était pas disponible (voire pas encore inventée !?), on n’a pas pu savoir s’il s’agissait d’A. phagocytophilum ou d’une autre bestiole.
Quoi qu’il en soit, les signes cliniques et biologiques ressemblent à ceux observés dans l’infection par E. canis, le plus souvent en un peu moins sévère. Le traitement par la doxycycline entraîne généralement une guérison clinique rapide et sans rechute.
L’hépatozoonose :
L’hépatozoonose, donc. Il existe plus de 300 espèces d’Hepatozoon, (un protozoaire proche des coccidies), qui infestent des mammifères, des oiseaux, des reptiles, des batraciens… nous ne parlerons ici que d’Hepatozoon canis, dont la répartition se superpose à celle de son vecteur, Rhipicephalus sanguineus. Attention, contrairement à tous les agents infectieux dont nous venons de parler, H. canis ne se transmet pas par piqure de tique, mais quand le chien mange une tique contaminée !
Parmi les chiens infestés, certains ne présentent aucun symptôme, à moins que ceux-ci ne soient masqués par une maladie intercurrente plus grave (souvent une autre maladie transmise par les tiques). Les symptômes que nous avons observés chez des chiens infestés, sans mise en évidence d’une maladie intercurrente, étaient l’abattement, l’anorexie et l’hyperthermie, ainsi que des douleurs (avec boiteries, difficultés à se lever…), moins fréquentes, mais plus évocatrices. A noter qu’aux États-Unis sévit une autre espèce, H. americanum, responsable de symptômes beaucoup plus dramatiques, qui conduisent souvent au décès de l’animal.
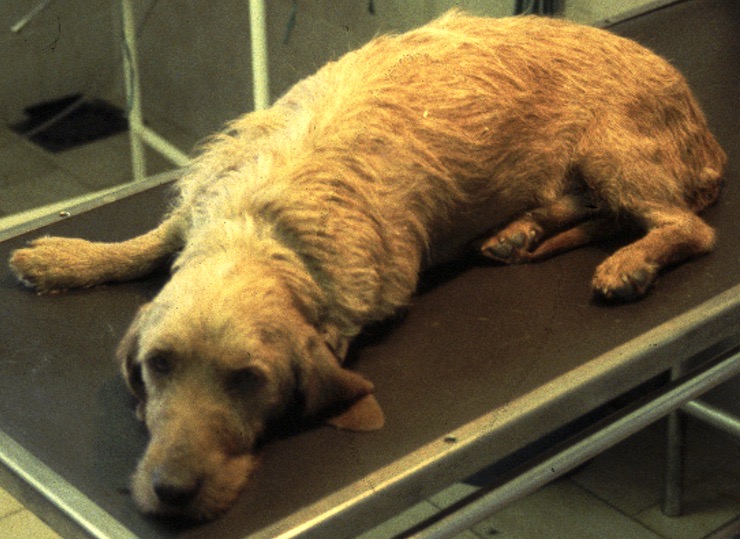
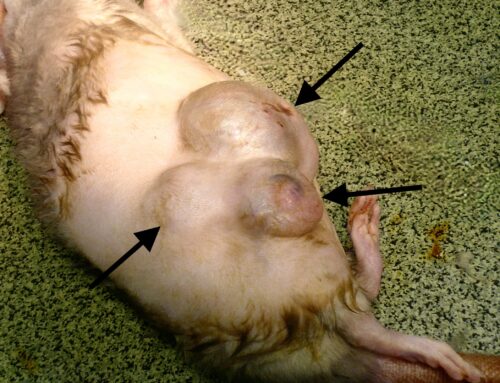
Jeune fauve de Bretagne, infesté par Hepatozoon canis. Lors de sa présentation en consultation, le chien était très abattu, ne posait pas son antérieur gauche (photo de gauche), et ne pouvait rester debout très longtemps (photo de droite). Après 48 heures d’évolution, il était incapable de se relever, et montrait d’importants signes de douleur malgré les anti-inflammatoires. Une réponse rapide a été obtenue après administration de toltrazuril.
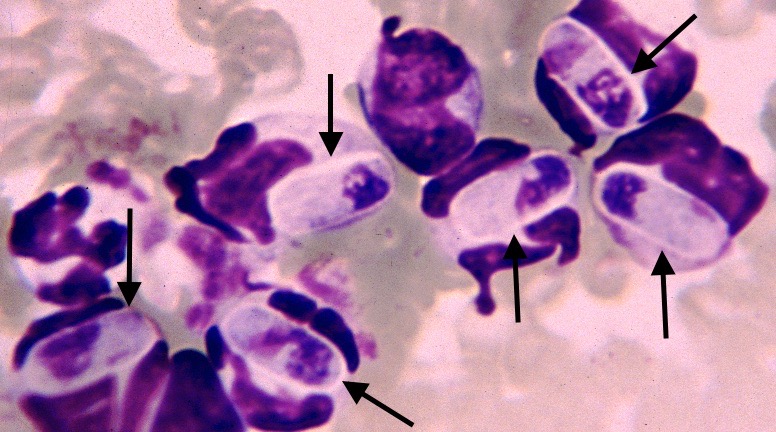
Six gamétocytes d’Hepatozoon canis (flèches) à l’intérieur de globules blancs, sur le frottis sanguin d’un chien.
Le parasite est facile à reconnaître sur un frottis sanguin, à l’intérieur de certains globules blancs (les polynucléaires neutrophiles ; photo ci-dessus)… sauf que parfois, il y en a peu, et qu’il faut donc chercher longtemps ! Il existe aussi un test PCR. Toutes sortes de traitements ont été décrits, souvent inefficaces – le fait que beaucoup de chiens infestés ne présentent pas de symptômes rendant, de plus, difficile l’évaluation de leur efficacité. Sur un nombre réduit de cas, nous avons obtenu d’excellents résultats, à la fois cliniques et parasitologiques, avec le toltrazuril, un anticoccidien pour volailles, porcins et ruminants qui, par principe, ne devra donc être utilisé chez le chien qu’en toute connaissance de cause, et après évaluation avec votre vétérinaire du rapport bénéfices/risques.
La maladie (borréliose) de Lyme :
Cette maladie est due à une bactérie spiralée appartenant à l’ordre des Spirochaetales : Borrelia burgdorferi, transmise par morsure d’Ixodes ricinus. Il s’agit de la plus fréquente des maladies transmises par les tiques en France, chez l’humain. Mais qu’en est-il chez le chien ? Celui-ci peut également être infecté, comme le prouvent les nombreuses sérologies positives, ou la (difficile) mise en évidence de l’agent infectieux, par PCR, dans certains tissus des chiens atteints. Pour autant, les symptômes attribués à la Borrelia (boiterie intermittente avec atteinte d’une ou plusieurs articulations, fièvre, abattement, anorexie, plus rarement uvéite ou myocardite)… sont-ils toujours dus à celle-ci ?
Quelques éléments de réflexion :
50 à 90 % des chiens parfaitement sains vivant en zone d’endémie (là où l’on trouve beaucoup de maladie de Lyme) sont séropositifs. Plus de 95 % de ces chiens séropositifs se portent très bien.
4,8 % des chiens séropositifs ont présenté des boiteries, de la fièvre, de l’abattement et de l’anorexie, sur une période d’observation de 20 mois… mais 4,6 % des chiens séronégatifs vivant dans la même zône ont présenté ces mêmes signes, pendant la même période.
Dans le Connecticut, (là où la maladie a été identifiée pour la première fois dans les années 1970), la sérologie Lyme est positive chez 68 % des chiens qui présentent une boiterie… et chez 70 % des chiens qui n’en présentent pas.
D’un point de vue expérimental, l’inoculation de Borrelia burgdorferi à des chiots (je sais, ce n’est pas bien !), n’a provoqué que des symptômes bénins, qui ont disparu spontanément en quelques heures, sans vraiment affecter l’état général des chiots. Pour avoir des symptômes plus « parlants », il a fallu injecter à des chiens de 6 mois de fortes doses de corticoïdes pour bien déprimer leur immunité, avant de les inoculer… Bon…
Et pour finir, ne pas oublier que la plupart des chiens séropositifs pour Borrelia et présentant des symptômes, sont également infectés par d’autres agents infectieux, au premier rang desquels Anaplasma phagocytophilum, dont nous avons déjà parlé, également transmise par morsure d’Ixodes ricinus… ce qui peut expliquer pas mal de choses.
Donc… on n’ira pas jusqu’à dire que la maladie de Lyme n’existe pas chez le chien, mais quand même, on évitera peut-être de diagnostiquer une maladie de Lyme chez tous les chiens qui boitillent et qui sont séropositifs pour Borrelia !
Signalons tout de même l’existence d’une forme de borréliose particulièrement sévère : la néphrite (ou néphropathie) de Lyme, associant une atteinte à médiation immune des glomérules et une nécrose marquée des tubules rénaux. Cette forme affecte majoritairement les labradors et golden retrievers, mais on ne la trouve que chez moins de 2% des chiens séropositifs à Borrelia burgdorferi… et esssentiellement aux USA.
La mycoplasmose (ex-hémobartonellose) du chat :
On va quand même parler un peu du chat ! Sans trop s’étendre non plus, puisque cette maladie est développée dans un article à part de ce site. Elle est due à trois bactéries gram-négatif polymorphes (de forme tantôt ronde, en anneau ou en bâtonnet), que l’on observe à la surface des globules rouges (= hématies) du chat. Il s’agit de Mycoplasma haemominutum, (une petite forme pas trop méchante), de Mycoplasma haemofelis (une grande forme, généralement plus pathogène), et de Mycoplasma turicensis, de découverte plus récente chez des chats suisses, et que l’on rencontre plus rarement. Ces trois espèces étaient autrefois regroupées sous le nom d’Haemobartonella felis.
Alors, ça peut paraître dingue, mais on ne sait toujours pas très précisément comment cette bactérie se transmet ! Une transmission – entre autres – par les puces et les tiques est tout de même très probable, d’où la présence de la mycoplasmose dans cet article. Les mycoplasmes adhèrent à la surface des globules rouges, dont ils provoquent la destruction, entraînant logiquement une anémie, mais aussi de la fièvre, un abattement, une anorexie, un amaigrissement, des vomissements… sachant quand même que de nombreux chats restent porteurs sains.
L’examen du frottis sanguin permet souvent la mise en évidence des mycoplasmes, accrochés à leur globule rouge.
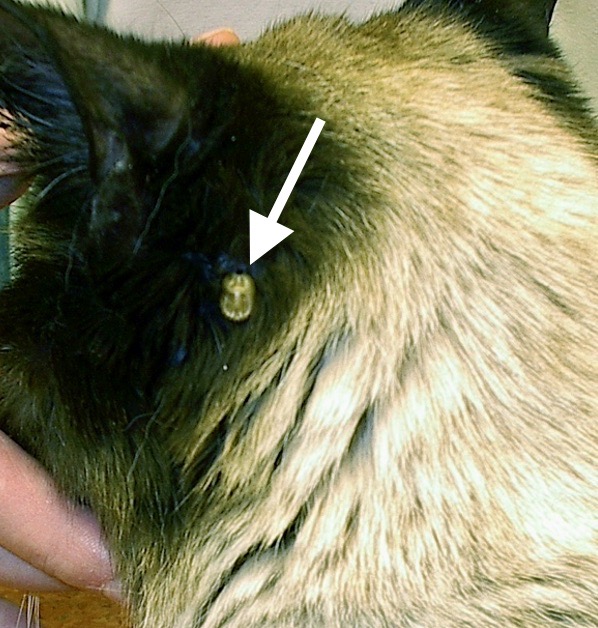
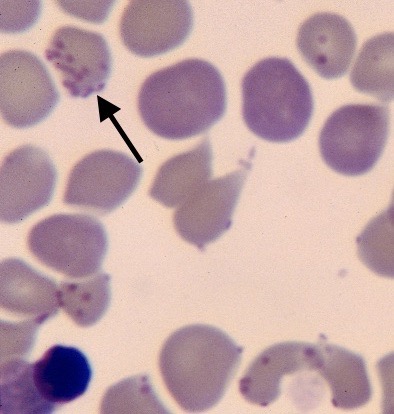
Photo ci-contre : l’hématie marquée par une flèche est bien envahie, mais plusieurs autres (en bas de la photo), ne sont pas mal non plus ! Noter aussi les différences de couleurs entre les globules rouges, ce qui témoigne du caractère régénératif de l’anémie : des hématies jeunes (plus colorées) sont larguées précipitamment dans la circulation pour remplacer celles qui ont été détruites par les mycoplasmes.
Mais comme le taux de mycoplasmes dans le sang évolue de façon cyclique, et que parfois il y en a très peu, on risque de les rater si on se contente de les chercher sur frottis sanguin : la PCR constitue alors une méthode de diagnostic beaucoup plus sensible.
En plus, la PCR permet de distinguer Mycoplasma haemominutum (moins méchante) de Mycoplasma haemofelis (plus méchante), et de les quantifier… ce qui peut toujours être utile.
Le traitement fait appel à des antibiotiques, notamment la doxycycline. Les symptômes disparaissent généralement assez vite (à condition qu’il n’y ait pas de maladie intercurrente, ce qui est assez fréquent), mais beaucoup de chats ne se débarrassent pas totalement de leurs mycoplasmes, et sont donc exposés à des rechutes – même si cela ne se produit pas très souvent.
La mycoplasmose canine :
Il n’y a pas que les chats qui attrapent des mycoplasmes, les chiens aussi, il n’y a pas de raison. Mais bon, on en a trouvé un cas en presque 40 ans, donc on ne va pas passer des heures dessus ! C’est juste histoire d’en dire un mot et d’en montrer quelques photos. A noter tout de même que dans une étude portant sur 460 chiens en France, plus de 15% en étaient porteurs. Ce n’est donc pas si rare que ça, mais ça montre que la plupart des chiens infectés ne tombent pas malades – on en reparle plus loin.
Nombreux mycoplasmes, isolés ou en chaînettes (flèches noires), à la surface des globules rouges d’un chien de trois ans. Celui-ci avait subi une ablation de la rate un an plus tôt, à cause d’une tumeur bénigne, mais de grande taille. Les mycoplasmes ne devront pas être confondus avec des corps de Howell-Jolly, (flèche rouge), restes de noyau sans signification pathologique – du moment qu’il n’y en a pas trop !
La maladie est due à Mycoplasma haemocanis, (ex-Haemobartonella canis) et Candidatus Mycoplasma haematoparvum, de petites bactéries de forme ronde qui s’attachent et se développent, isolées ou en chainettes, à la surface des globules rouges (photos ci-dessus). Leur transmission est assurée essentiellement par morsure de notre vieille connaissance Rhipicephalus sanguineus. Une fois arrimés à la surface des globules rouges, les mycoplasmes entraînent leur destruction, et les symptômes qui s’ensuivent sont ceux d’une anémie (abattement, anorexie, pâleur des muqueuses…) – tout cela est d’une logique implacable. Mais pourquoi, me direz-vous, si 15% des chiens en sont porteurs, n’en avons-nous vu qu’un seul cas en 40 ans ? Parce que pour que la maladie s’exprime, il faut que le chien soit bien immunodéprimé, et en particulier… qu’il n’ait plus de rate ! (Concrètement, qu’on la lui ait retirée suite à un trauma ou à une tumeur). Le diagnostic se fait par mise en évidence des mycoplasmes sur frottis sanguin ou, plus sûrement, par PCR. (Mais encore une fois, ce n’est pas parce qu’un chien est PCR+ que ses symptômes viennent de là !) Le traitement par des antibiotiques adaptés provoque généralement la disparition des symptômes, mais certains chiens peuvent rester porteurs.
Alors, qu’est-ce qu’on fait ?
On sauve le chien !
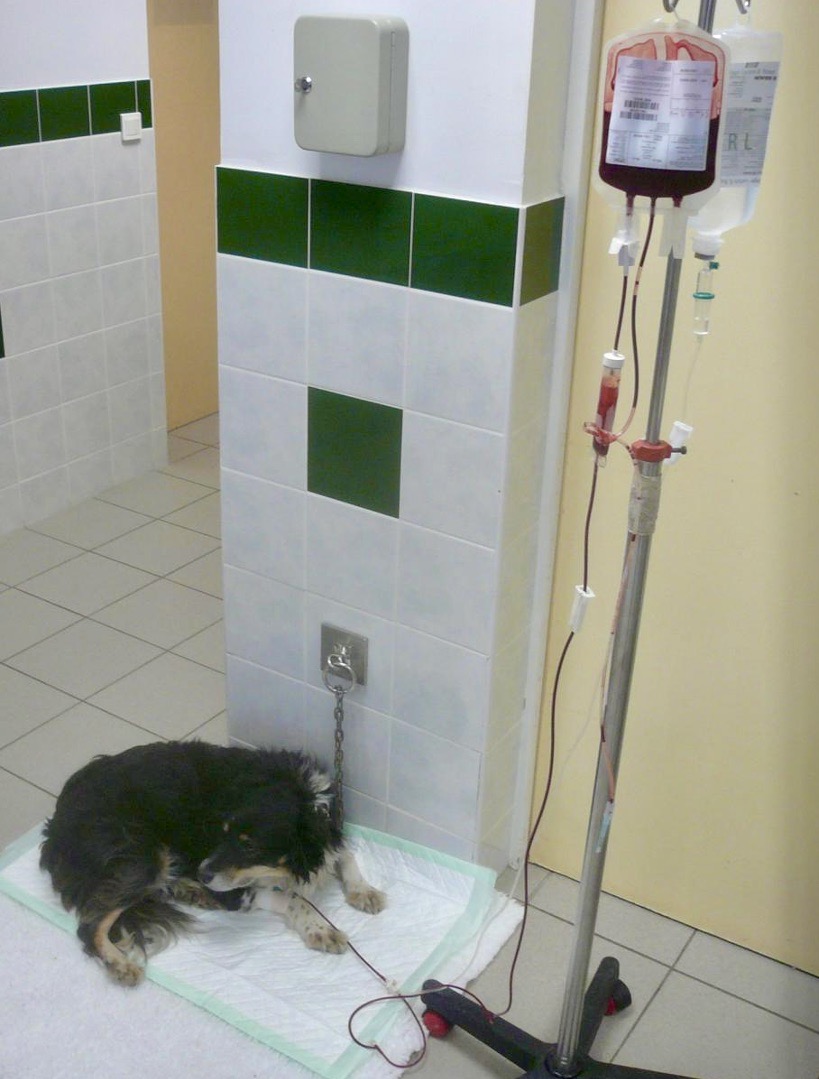
On l’a vu plus haut dans la partie consacrée à la spoliation : même si ça n’arrive pas tous les jours, certains chiens nous sont présentés en très mauvais état, avec des muqueuses toutes blanches, après que les tiques leur ont pompé une grande quantité de sang. L’idéal, dans ce cas, est de transfuser rapidement le chien avec du sang frais (photo ci-contre). Trouver un donneur peut malheureusement s’avérer problématique, surtout dans des conditions d’urgence. Heureusement, le risque de choc transfusionnel est très réduit lors d’une première transfusion chez le chien, (il augmente à partir de la deuxième), et on n’a donc pas besoin de disposer de cinq ou six donneurs pour en trouver un compatible ! Il est cependant bien de s’assurer que notre donneur ne soit pas porteur d’une maladies transmissible par transfusion… catégorie à laquelle appartiennent la plupart des maladies transmises par les tiques !
Et puis sinon, mais ça tombe sous le sens, si l’on identifie une maladie transmise par les tiques, on met en route le traitement – on en a mentionné quelques-uns plus haut – sans oublier de faire ce qu’il faut pour soutenir l’état général, calmer les symptômes et soulager l’animal : mise sous perfusion si nécessaire, anti-vomitifs, antalgiques, etc.
On élimine les tiques
On l’a vu plus haut : si les piroplasmes mettent plus de 48 heures à passer de la tique au chien, d’autres agents pathogènes lambinent beaucoup moins : trois heures pour Ehrlichia canis ! Il n’y a donc pas de temps à perdre. Même si certains produits tuent aujourd’hui les tiques très rapidement, trois heures… ça fait court. Il est donc préférable de retirer les tiques manuellement dès qu’on les voit, et de réaliser une inspection systématique du chien au retour de chaque promenade dans des endroits à risque. (Une prairie bien herbeuse au printemps, par exemple).
Si on en a un sous la main, il est préférable d’utiliser un crochet à tiques (photos ci-dessous), plutôt que d’arracher ces bestioles avec une pince ou directement avec les doigts. Le crochet présente plusieurs avantages : d’abord, il permet d’extraire la tique sans risquer de laisser sa tête dans la peau du chien ou du chat, (ce n’est quand même pas très fréquent, mais ça arrive) ; ensuite il évite le contact direct des doigts avec les sécrétions de la tique, surtout si on l’écrase malencontreusement en la retirant (il y a un risque de transmission de maladies à l’humain) ; enfin, il est toujours possible qu’en comprimant la tique lorsqu’on la saisit, on provoque une régurgitation de salive, bien chargée en agents pathogènes, en direction du chien ou du chat ! Brûler la tique avec son briquet ou sa cigarette, ou encore l’asperger d’alcool ou d’éther, pourra également provoquer une régurgitation réflexe. Bon, après, si on n’a pas de crochet, tant pis, on enlève avec les doigts, c’est toujours mieux que de laisser la tique en place. Autre solution, si l’on dispose d’un spray anti-tiques efficace, on peut toujours en pulvériser directement sur la tique (au risque d’une régurgitation réflexe, comme on vient de le voir ?) : elle mettra peut-être du temps à tomber mais au moins, si elle est morte, elle ne pourra plus transmettre de maladie. Encore faut-il qu’elle meure rapidement…
Quelques exemples de retrait de tiques avec un crochet sont visibles sur cette vidéo.
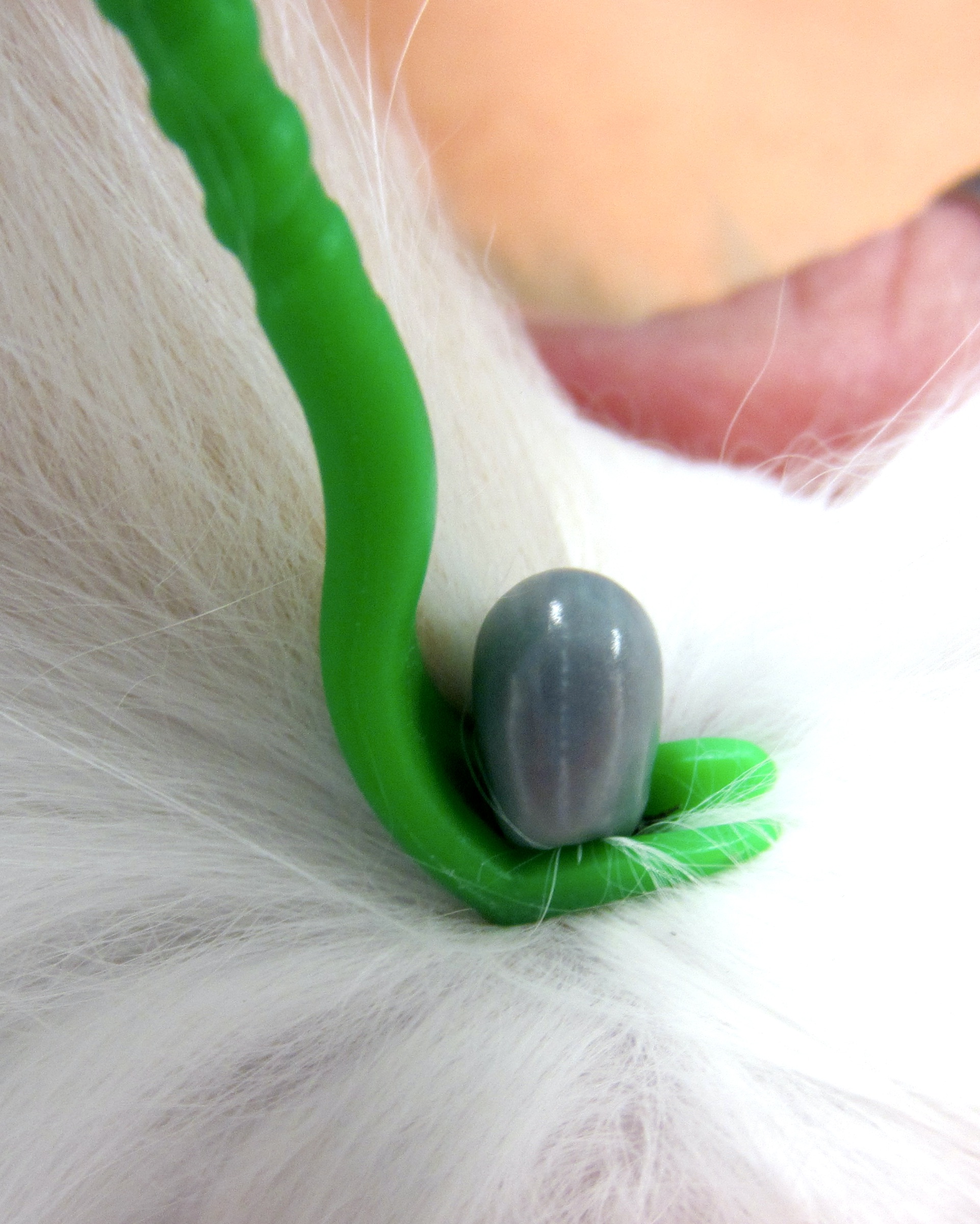
En voilà une qui se nourrit tranquillement sur un chat, (elle est déjà bien gorgée), sans se douter de ce qui va lui arriver ! Pour voir le crochet anti-tiques en action, suivre le lien indiqué juste au-dessus des photos.
A noter que l’implantation de beaucoup d’espèces de tiques est indolore : ceux qui ont déjà senti une petite croûte sur leur tête en faisant leur shampooing, et qui se sont aperçus, après avoir tiré dessus, qu’il s’agissait en fait d’une tique, sont bien placés pour le savoir ! Une petite réaction inflammatoire peut parfois se mettre en place autour du point d’implantation, mais ce n’est pas le cas le plus fréquent, et il ne faut donc pas attendre une manifestation douloureuse ou prurigineuse de la part du chien pour commencer à lui chercher des tiques.
On fait de la prévention
Il n’est pas facile d’éliminer les tiques de l’environnement du chien ou du chat. On peut évidemment éviter de promener son chien dans les zones que l’on sait très infestées, (prairie, sous-bois…), spécialement au printemps et à l’automne… mais il peut n’y avoir pas d’autre endroit où aller le promener. Dans le cas de chiens vivant en chenil, particulièrement visés par Rhipicephalus sanguineus, il est possible de pulvériser un produit antiparasitaire… en veillant à ce qu’il ne présente pas de toxicité pour les animaux domestiques. Un sol lisse sera évidemment plus facile à traiter qu’un sol en terre battue recouvert de paille ! Si l’on commence à trouver des tiques qui cheminent sur le tapis de la salle à manger, on pourra aussi utiliser un fogger (diffuseur), actif à la fois sur les puces et les tiques. Il en existe beaucoup – des bons et des moins bons : à discuter avec votre vétérinaire.
Il est plus facile de faire de la prévention directement sur son animal, et pour cela, nous disposons aujourd’hui de toutes sortes de produits. Notons que la plupart de ces produits auraient pu trouver leur place dans le chapitre précédent, car on peut aussi les utiliser pour traiter un chien ou un chat qui rentre de sa promenade couvert de tiques, mais pour les raisons déjà évoquées, (le passage d’agents infectieux de la tique à notre compagnon, quelques heures seulement après l’implantation), il est préférable de retirer les tiques une à une avec un crochet. Bon, évidemment, si le chien est recouvert par plusieurs centaines de tiques, dont des larves ou des nymphes de quelques millimètres bien cachées sous les poils, on se contentera peut-être de lui administrer un traitement, en choisissant un de ceux qui agissent le plus vite, et on attendra que les tiques décèdent toutes seules… mais les enlever manuellement, ce sera quand même toujours mieux.
Dans le détail :
- Les poudres, lotions, shampooings : on peut oublier tout de suite les poudres et les shampooings : en admettant qu’ils agissent sur les tiques déjà en place, la poudre disparaîtra dès que le chien se sera secoué, et le shampooing partira au rinçage, donc aucun effet rémanent et aucune prévention pour la suite. Certaines lotions, comme l’amitraz, bien que d’application contraignante, surtout sur un chien à poils longs, avaient l’avantage d’être efficaces et peu coûteuses… sauf qu’il n’existe plus actuellement de formulation pour les chiens. Celles prévues, par exemple, pour le bétail, seront employées… sous la responsabilité de l’utilisateur ! Grosse toxicité chez le chat.
-
Les sprays : les plus efficaces sont à base de fipronil ou de perméthrine. Ils tuent les tiques en place et préviennent les infestations pendant 2 à 4 semaines selon les produits… à condition de respecter le nombre de pulvérisations à appliquer en fonction du poids de l’animal : il faut donc compter le nombre de pressions, et ne pas se contenter de trois petits pschitts le long de la ligne du dos. Après une pulvérisation à rebrousse-poil sur tout le corps, de sorte que le pelage soit uniformément mouillé, on frictionne bien pour faire pénétrer le produit jusqu’à la peau, après quoi on laisse sécher sans essuyer – sinon, on enlève tout ce qu’on vient de mettre ! On ne rince pas non plus, évidemment, et on évite les shampooings et les bains de mer (ou de rivière) pendant 48 heures. L’inconvénient du spray est qu’il est plus compliqué de l’appliquer (surtout sur un bouvier bernois de 50 kg bien velu), que de mettre une pipette ou de donner un comprimé, et qu’on risque donc de laisser tomber rapidement. Avantages et inconvénients des différents produits à discuter avec votre vétérinaire ; à noter que la perméthrine est toxique pour les chats. Comme pour les colliers ci-dessous, il existe des sprays « naturels », aux ingrédients d’origine végétale, qu’il sera toujours tentant de vouloir utiliser… mais qui n’impressionnent pas beaucoup les tiques, en général.
- Les colliers : il en existe plusieurs, les plus efficaces étant ceux à base de pyréthrynoïdes. Ils exercent une action acaricide (= ils tuent les tiques) pendant au moins six mois, et possèdent en outre une action répulsive, à la fois sur les tiques mais aussi sur les moustiques et les phlébotomes, ces derniers susceptibles de transmettre la leishmaniose. (Notons que l’action répulsive réduit, mais ne supprime pas le risque de piqure par une tique ou un phlébotome). Ils sont efficaces sur Ixodes ricinus et Rhipicephalus sanguineus, peut-être un peu moins sur Dermacentor reticulatus, si l’on en croit les différents résumés des caractéristiques du produit (RCP). Ils tuent les tiques nouvellement implantées en 24 à 48 heures, ce qui peut suffire (c’est parfois un peu juste) pour éviter une piroplasmose, mais pas une ehrlichiose ou une anaplasmose pour lesquelles, on l’a vu, la transmission se fait dans les premières heures suivant la morsure : le port du collier ne dispense donc pas de l’épluchage manuel du chien au retour d’une promenade ! Concernant les tiques déjà implantées lors de la pose du collier, elles ne seront pas tuées dans les 48 premières heures : les RCP recommandent d’ailleurs de mettre le collier au chien une semaine avant le début de la saison des tiques, ou avant un déplacement dans une zone à risque. Donc si votre chien est plein de tiques, il ne faut pas se contenter de lui mettre un collier et d’attendre tranquillement que ça tombe : il faudra soit les retirer manuellement, soit utiliser un produit d’action plus rapide. Le choix entre les différents colliers existants (en fonction de leur durée d’action, ou de la protection contre tel ou tel stade de développement ou espèce de tiques), sera à discuter avec votre vétérinaire. A noter que la deltaméthrine est toxique chez le chat. Un dernier mot pour dire que tout le monde aimerait éviter d’utiliser des produits chimiques, (même si les pyréthrinoïdes sont moins toxiques que les organochlorés ou les organophosphorés, par exemple), mais l’efficacité des colliers à base d’extraits de plante, ou émettant des vibrations et des résonances magnétiques… n’a pas été démontrée ; et on parle quand même ici de la prévention de maladies potentiellement mortelles pour le chien… dont certaines transmissibles aux humains !
- Les pipettes, encore appelées spot-on : alors là, il y en a plein, dont les principes actifs vont des plus classiques (entre autres la perméthrine et le fipronil, dont on a déjà parlé), jusqu’aux plus récents comme les isoxazolines (qu’on trouve surtout sous forme de comprimés, on en parle plus loin), en passant par des huiles aromatiques dont l’efficacité, là aussi, reste à démontrer. Comme les colliers, les pipettes « anti-tiques » les plus intéressantes, (votre vétérinaire vous conseillera à ce sujet), ont une efficacité à la fois acaricide et répulsive contre les tiques, et un effet répulsif sur les moustiques, phlébotomes et mouches piquantes. Elles sont également efficaces contre les puces, (plus de détails dans l’article de ce site consacré à ces bestioles). Certaines pipettes ont, en outre, une activité sur d’autres parasites externes comme les poux broyeurs, la gale sarcoptique et la démodécie. Tous les RCP (résumé des caractéristiques du produit) ne précisent pas combien de temps est nécessaire pour tuer les tiques présentes sur l’animal, après application de la pipette. Il semble que ce délai soit de 48 heures minimum, mais puisse atteindre une semaine selon les produits. Le délai est plus court pour les nouvelles tiques infestantes, mais là aussi, rarement précisé dans les RCP. La plupart des pipettes sont efficaces pendant un mois (3 à 5 semaines) après application, certaines (moins nombreuses), jusqu’à trois mois. Il n’est pas interdit de laver son animal ou de le laisser se baigner pendant cet intervalle… mais tout de même avec modération : les notices des produits vous renseigneront généralement sur la fréquence à laquelle les chiens (et les chats qui se baignent) peuvent aller faire trempette, sans perte d’efficacité du produit. Les notices vous indiqueront également les limites d’âge et de poids en deçà desquelles le produit ne doit pas être utilisé. Attention, certaines pipettes pour chiens, notamment celles contenant de la perméthrine, sont extrêmement toxiques pour les chats, chez qui elles peuvent déclencher des symptômes neurologiques (convulsions), qui conduisent souvent au décès ! Si une de ces pipettes a été appliquée par erreur sur un chat et qu’on s’en aperçoit rapidement, il faudra shampooiner énergiquement l’animal pour éliminer le maximum de produit avant que celui-ci ait été absorbé… puis amener rapidement son petit félin chez un vétérinaire ! A noter que si un chat lèche le point d’application d’une de ces pipettes sur la peau d’un chien avant que tout ait complètement seché, on peut arriver au même résultat.
Mettre une pipette d’antiparasitaire à un chien est un acte simple, mais qui pose parfois problème à certains propriétaires – tout au moins la première fois. Du coup, on vous a fait un tuto ! Alors, d’abord, on perce l’opercule de la pipette, puis on choisit un point d’application que le chien ne pourra pas lécher, généralement entre les omoplates. Les poils sont ensuite écartés, et le produit est appliqué directement sur la peau. S’il y en a trop par rapport à la surface de peau dégagée, et qu’on voit que ça risque de couler, on répartit le produit en deux ou trois points, après quoi on ramène les poils par-dessus. A noter que le contenu de certaines pipettes est à répartir tout le long de la ligne du dos, et non en un seul point. On évite ensuite de toucher le site pendant quelques heures, jusqu’à ce que le produit ait complètement séché. On évitera aussi que le chien aille directement se plonger dans la rivière ! A la fois pour que le produit ne soit pas directement éliminé au contact de l’eau, et aussi (surtout), parce que certains antiparasitaires sont toxique pour les poissons. Et pour le chat, ça fonctionne pareil ! (Excepté le risque de bain dans la rivière, en général).
- Les comprimés : depuis quelques années, la lutte contre les insectes et acariens parasites des chiens et des chats a été grandement facilitée par l’arrivée d’une nouvelle classe d’antiparasitaires appartenant à la famille des isoxazolines : afoxolaner, fluralaner, lotilaner, sarolaner… La plupart de ces produits existent sous forme de comprimés à mâcher très appétents, spontanément consommés par la plupart des chiens et pas mal de chats. (Attention, tous ne sont pas prévus pour les chats). La durée d’action après la prise d’un comprimé va de un à trois mois, selon la formulation. Les tiques décèdent en 48 heures maximum après leur arrivée sur le chien (et les puces en 8 heures). Tiques et puces doivent de toute façon s’attacher à l’hôte et commencer leur repas pour être exposées à la substance active, le risque de transmission des maladies ne peut donc être exclu. Les éventuels effets secondaires varient selon les molécules, mais restent exceptionnels : votre vétérinaire vous renseignera à ce sujet, ainsi que sur les rares contre-indications. Cette famille de produits a donc pour avantages l’efficacité et la facilité d’administration. Le principal inconvénient est l’absence d’effet répulsif sur les puces et les tiques (elles meurent après avoir piqué), et sur les moustiques et phlébotomes (pas d’effet préventif sur la leishmaniose : dans les zones d’enzootie de leishmaniose, il est donc nécessaire d’associer les comprimés à un répulsif en collier ou en spot-on). A noter que ces produits sont également très efficaces pour traiter un certain nombre d’affections cutanées, (gale sarcoptique et gale des oreilles, démodécie, cheyletiellose…), dont certaines étaient jusque-là difficiles à guérir, du fait de traitements parfois peu performants, mais surtout astreignants pour les propriétaires.
Signalons que des antiparasitaires appartenant à la famille des isoxazolines existent également en version pipette (on en a parlé), et injectable (fluralaner), la durée d’action de cette dernière formulation, administrée uniquement par les vétérinaires, étant annoncée comme pouvant atteindre un an.
Et nous, dans tout ça ?
Bon, on ne va pas écrire une thèse sur les maladies transmises par les tiques chez les humains : d’abord parce qu’on n’en a ni les compétences ni les prérogatives, ensuite parce que ce n’est pas le sujet de l’article, et enfin parce qu’on n’était pas partis pour écrire un traité de 500 pages. Les paragraphes ci-dessous n’auront donc pas d’autre objectif que de décrire succinctement le rôle que peuvent jouer le chien, et plus rarement le chat, dans la contamination des humains par les tiques, et par les maladies qu’elles transmettent. Ce qui veut dire que si vous avez été piqué par une tique il y a une semaine, et que vous avez maintenant des boutons qui vous sortent un peu partout ou un gros mal de tête, ce genre de choses… ne perdez pas de temps à continuer la lecture, et téléphonez plutôt à votre médecin !
Deux points importants avant de commencer : ils découlent de ce qu’on a écrit dans les paragraphes précédents, mais c’est toujours bien de les rappeler:
1 – D’abord, les maladies transmises par les tiques sont des maladies qui se transmettent… par les tiques. Formulé comme ça, ça a l’air idiot, mais ça veut dire que si vous faites des papouilles à votre chien et qu’en retour, celui-ci vous léchouille, vous ne risquez pas d’attraper la maladie de Lyme ou une ehrlichiose.
2 – On l’a vu, les trois espèces de tiques qui parasitent nos carnivores domestiques en France métropolitaine, prennent un seul repas sanguin sur leur hôte ; après quoi elles tombent par terre et muent (pour les larves et les nymphes) ou pondent (pour les femelles adultes). Donc, une tique ne va pas piquer votre chien, s’infecter (avec une Borrelia, une Ehrlichia… si toutefois il en est porteur), puis galoper jusqu’à vous, vous piquer et vous transmettre aussi sec la bactérie qu’elle vient d’attraper sur votre chien. Au pire, celui-ci ne fera que rapporter à la maison des tiques qu’il a attrapées à l’extérieur : certaines qui ne l’ont pas piqué et se promènent encore entre ses poils, d’autres qui l’ont piqué, mais dont seul(e)s les descendant(e)s pourront éventuellement vous piquer à leur tour, plusieurs semaines ou mois plus tard.
Les tiques
D’abord, quelles sont les tiques qui s’attaquent aux humains en France ? En premier lieu notre vieille connaissance Ixodes ricinus, que l’on attrape lors des balades en forêt, où elle nous guette, à l’affût sur son brin d’herbe. C’est la plus répandue des tiques présentes en métropole, probablement parce qu’elle n’est pas trop regardante sur le type de sang qu’elle consomme : avec elle, tout fait ventre, des petits lézards aux grands cervidés, plus de 300 espèces en tout. Nous avons aussi Dermacentor reticulatus, ainsi que sa cousine plus méditerranéenne Dermacentor marginatus qui, pour des raisons qui n’appartiennent qu’à elles, (un attrait pour les zones à fourrure et à poils ?), se fixent essentiellement sur le cuir chevelu des humains. Enfin, pour compléter notre trio infernal, Rhipicephalus sanguineus qui, si elle n’a pas de chien à se mettre sous la dent (pardon, sous l’hypostome), se résoudra éventuellement à piquer un humain, et ce d’autant plus facilement que comme on l’a vu plus haut, elle vit à proximité, voire à l’intérieur des habitations. N’oublions pas Hyalomma marginatum, présente depuis une dizaine d’années sur le littoral méditerranéen avec une préférence pour les milieux ouverts de type maquis ou garrigue, et dont l’aire de répartition s’étend vers le nord du fait du réchauffement climatique. Ajoutons pour finir à cette liste (non exhaustive !) Argas reflexus, la tique du pigeon, qui peut sévir dans les habitations proches… des nids de pigeons, ou des pigeonniers.
Quelques conseils de prévention contre les piqûres de tiques, (vêtements couvrants, chaussures fermées… y compris une liste des principes actifs revendiquant une efficacité répulsive contre ces bestioles), sont consultables sur le site de l’ANSES.

Quelques endroits où l’on pourrait bien se faire piquer par les tiques. (Ok, c’est un peu restrictif, mais ça donne quand même une idée) : forêts à feuilles caduques et forêts mixtes (feuillus, conifères), mais aussi milieux plus ouverts (prairies, pâtures), pour Ixodes ricinus (en haut à gauche). Milieux ouverts (prairies, landes, clairières, haies, berges de rivière, mais aussi terrains vagues en zones péri-urbaines) pour Dermacentor reticulatus (en haut à droite). NB : on parle bien sûr d’I.ricinus et D. reticulatus adultes, les larves et nymphes se terrant dans des terriers ! Ci-dessus : un paysage méditerranéen ; pour peu qu’il y ait un chien dans cette petite maisonnette perdue au milieu des vignes et de la garrigue, ça fera un parfait habitat pour Rhipicephalus sanguineus… et pour la nouvelle venue Hyalomma marginatum.
La maladie de Lyme
Maintenant, parmi les maladies transmises par les tiques affectant le chien ou le chat, lesquelles sont des zoonoses (= des infections ou maladies naturellement transmissibles des animaux aux humains et réciproquement) ?
La maladie de Lyme, dont nous avons déjà parlé chez le chien, est la maladie transmise par les tiques (quatre espèces d’Ixodes dans le monde, Ixodes ricinus en France), la plus répandue chez les humains : près de 47 000 cas en France métropolitaine en 2021, selon Santé Publique France. Elle est due, on l’a vu, à diverses bactéries appartenant au genre Borrelia, la plus connue étant Borrelia burgdorferi (photo ci-dessous). La maladie n’est identifiée sous son nom actuel que depuis 1976, mais certaines de ses manifestations, comme l’érythème migrant, sont décrites depuis 1883 ! On ne va pas décrire en détail la maladie chez l’humain, disons seulement qu’elle reste souvent sans symptôme, au moins dans un premier temps, et que ces symptômes, lorsqu’ils sont présents, s’avèrent très variables. Classiquement, ça commence par une rougeur qui s’étend de façon circulaire autour du site de la piqûre, (l’érythème migrant) ; quelques semaines ou mois plus tard, un syndrome pseudo-grippal caractérisé par de la fièvre, des frissons, des maux de tête, une grosse fatigue, des douleurs musculaires et articulaires, voire des troubles neurologiques et cardiaques ; et après plusieurs années, des troubles dermatologiques, des douleurs articulaires chroniques avec notamment des genoux enflés entraînant des difficultés à se déplacer, ainsi qu’une atteinte neurologique avec notamment troubles de l’humeur, de la mémoire et du sommeil.
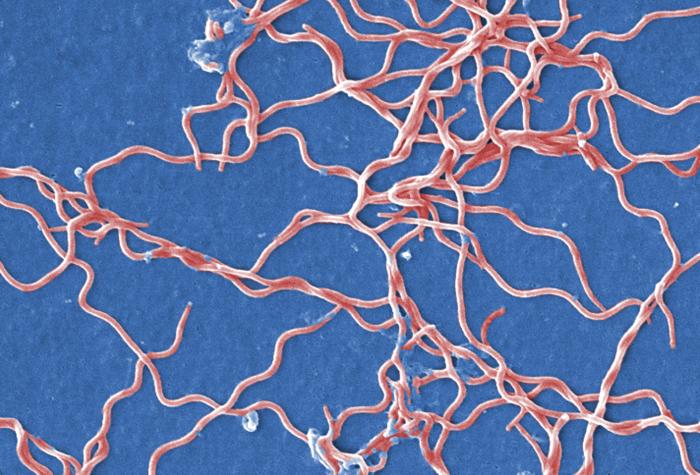
Bactéries de l’espèce Borrelia burgdorferi en culture, telles qu’elles apparaissent en microscopie électronique à balayage colorisée. Ces bactéries appartiennent à l’ordre des Spirochaetales – du grec speira qui signifie spirale, et khaitê, chevelure longue et épaisse – on comprend pourquoi quand on regarde la photo. (Crédit : Janice Haney Carr, CDC Public Health Image Library).
Les chiens étant l’un des multiples réservoirs possibles de Borrelia burgdorferi, une tique qui se nourrit sur un chien infecté peut elle-même s’infecter, et le stade suivant (par exemple la nymphe si c’est la larve qui s’est infectée), transmettre à son tour la bactérie à d’autres vertébrés, dont les humains, à l’occasion de son propre repas sanguin. Les chiens peuvent donc contribuer à introduire des tiques porteuses de Borrelia dans l’environnement humain… mais les réservoirs biologiques naturels des Borrelia étant essentiellement constitués par les micromammifères forestiers et les oiseaux, et leur dissémination, principalement assurée par les cervidés et les sangliers… on a quand même nettement plus de risques de se faire piquer par une tique contaminée lors d’une balade en forêt qu’en faisant des papouilles à son chien. Quoi qu’il en soit, raison de plus pour inspecter son animal de fond en comble à chaque retour de promenade, crochet à tiques à la main !
Ehrlichioses et anaplasmoses
Concernant les ehrlichioses et les anaplasmoses, il s’agit d’infections causées par des bactéries intracellulaires de la famille des Anaplasmataceae, qu’on a déjà décrites chez le chien. On pourrait en parler pendant des heures, vu qu’il en existe plein plein plein d’espèces différentes, et qu’on en découvre toujours des nouvelles quelque part dans le monde, qui ne diffèrent des précédentes que par quelques acides nucléiques… sachant que la plupart sont peu, voire pas du tout décrites en France. (Un article de 2018, très complet, sur le sujet, est à lire ici).
On citera Anaplasma phagocytophilum, dont nous avons parlé plus haut chez le chien, transmise en Europe par Ixodes ricinus, et responsable de l’anaplasmose granulocytique humaine. En 2018, on comptait une centaine de cas humains confirmés en Europe… dont 6 en France. Aux dernières nouvelles, l’ehrlichiose monocytique humaine due à Ehrlichia chaffeensis (proche d’Ehrlichia canis) et l’ehrlichiose granulocytique due à Ehrlichia ewingii n’étaient pas décrites en Europe. Ces trois bactéries sont responsables, chez l’humain, de fièvres, douleurs musculaires et céphalées.
La fièvre boutonneuse méditerranéenne
Un mot sur Rickettsia conorii, responsable de la Fièvre boutonneuse méditerranéenne. On n’entend pas trop parler de cette maladie, pourtant décrite depuis 1909, identifiée à Marseille en 1925, et présente sur tout le pourtour méditerranéen (mais aussi au Moyen-Orient, en Afrique…). Il faut dire que son incidence est assez basse, avec 48 cas / 100 000 habitants dans le sud-est de la France, et que les manifestations chez l’humain sont le plus souvent qualifiées de « bénignes » (un ulcère au point d’inoculation (on parle de « tache noire »), une fièvre, des douleurs et, comme son nom l’indique, une éruption de boutons), mais avec quand même 6-7% de formes sévères, et 2 à 5% de mortalité ! Chez le chien, sauf cas très très très très exceptionnels, la bactérie ne provoque aucun symptôme, raison pour laquelle on n’en a pas parlé plus haut.
La transmission est assurée par notre vieille connaissance Rhipicephalus sanguineus, essentiellement de chien à chien, (cette tique, on l’a vu, a une grande spécificité d’hôtes), mais aussi du chien à l’humain. Les tiques transmettent la rickettsie d’un stade à l’autre, mais aussi d’une génération à l’autre par leurs œufs (photo ci-contre)… sachant que les tiques infectées meurent souvent après la première génération, ce qui relativise leur rôle de réservoir. Les chiens infectés expérimentalement n’ont développé qu’une rickettsiémie (= présence de rickettsies dans le sang) faible et intermittente, du 2ème au 10ème jours après inoculation, ce qui n’en ferait pas non plus de très bons réservoirs. Ce rôle pourrait être tenu par les petits rongeurs, hérissons, lièvres et lapins.
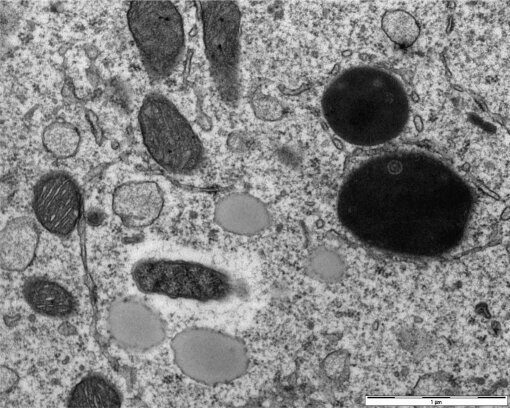
Ricketsia conorii, vue en microscopie électronique dans l’ovaire d’une tique Rhipicephalus sanguineus adulte. (dans : C. Socolovschi & coll : The relationship between spotted fever group Rickettsiae and Ixodid ticks, Vet Res 2009, 40 (34)).
L’essentiel des contaminations humaines se situe entre juillet et septembre avec un pic au mois d’août, correspondant à la période d’activité maximale des stades immatures (larves et nymphes) de Rh. sanguineus. Des études réalisées dans différents quartiers de Marseille au début des années 1990 par D. Raoult & Coll ont montré une corrélation entre le nombre de malades hospitalisés pour une FBM, la séroprévalence de R. conorii chez les donneurs de sang, le nombre de chiens par 100 habitants, et la proportion de chiens porteurs de tiques. 9 à 15% de celles-ci, (quand même !), étaient porteuses de R. conorii.
La conclusion de tout cela est que le chien ne transmet pas lui-même l’infection aux humains, (la FBM n’est d’ailleurs pas une maladie animale réputée contagieuse, selon l’INRS), mais qu’en apportant des tiques dans l’environnement humain, il peut augmenter le risque d’infection pour l’Homme. Il joue aussi un rôle de sentinelle, dans la mesure où, quand on trouve quelque part beaucoup de chiens séropositifs pour R. conorii, on peut se dire qu’il est urgent de prendre les mesures de prévention dont on a déjà abondamment parlé plus haut, à la fois pour les humains et pour les chiens !
Et pour en finir avec les rickettsies, on ne dira rien de Rickettsia rickettsii, responsable de la Fièvre pourprée des montagnes rocheuses, très importante chez le chien et chez les humains dans certaines parties du monde, (notamment en Amérique du nord), mais qu’on ne rencontre pas chez nous. Ouf, quand même une bonne nouvelle !
Enfin, aucun cas d’infection par une Babesia de carnivore n’a été signalé dans l’espèce humaine.