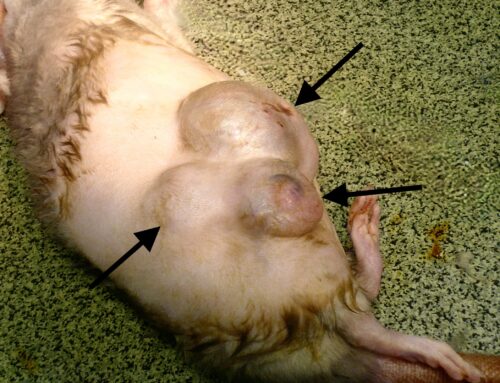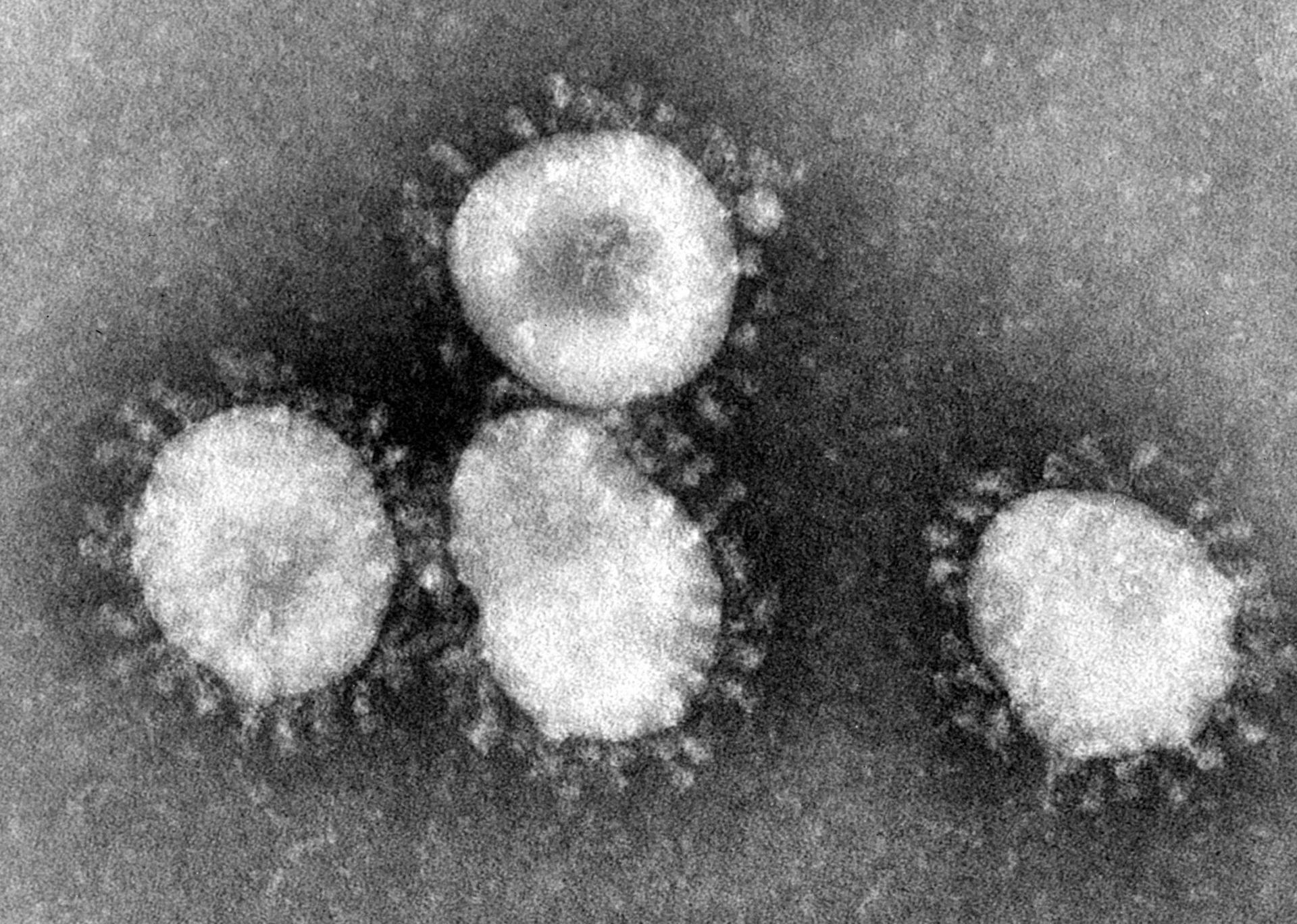
Quatre coronavirus, observés au microscope électronique. Source : CDC/Dr. Fred Murphy, Bibliothèque d’images de santé publique des Centres pour le contrôle et la prévention des maladies.
Jusqu’à un passé récent, la péritonite infectieuse féline (PIF) tuait 100% des chats atteints. Depuis la toute fin des années 2010, et officiellement/légalement en France depuis 2024, un traitement permet d’en sauver près de 90%. Cela valait bien un article, vous ne croyez pas ?

Le coronavirus félin FCoV
1 – Il ressemble à quoi, Ie FCoV ?
Le coronavirus félin (FCoV pour Feline Coronavirus) est un gros virus sphérique, pléomorphe, (c’est à dire qu’il peut changer de forme selon les circonstances), enveloppé (c’est à dire qu’il est entouré… d’une enveloppe, ce qui n’est pas le cas de tout le monde : on en reparle plus loin). Il appartient à l’ordre des Nidovirales, à la famille des Coronaviridae, à la sous-famille des Coronavirinae, au genre Alphacoronavirus, et à l’espèce alphacoronavirus 1.
Alors, toute cette énumération n’est pas là juste pour faire joli : l’intérêt, c’est de savoir que parmi les Alphacoronavirus, en dehors des deux formes de coronavirus félin dont on va parler tout au long de cette page, on trouve aussi le coronavirus canin (CCoV), responsable de l’entérite à coronavirus du chien, tout un tas de virus causant des diarrhées (TGEV, PEDV, SeCoV, SADS) ou une maladie respiratoire (PRCoV) chez le porc, et quelques virus pouvant contaminer l’Homme. Le CCoV, en particulier, sans doute du fait de sa proximité avec le FCoV, peut infecter les chats, provoquer chez eux une séroconversion avec des anticorps qui croisent avec le FCoV, déclencher de la diarrhée et même une PIF. De façon plus exceptionnelle, CCoV et FCoV peuvent même se recombiner entre eux et là, ça devient très très très embêtant : on en parle en fin d’article avec ce qui se passe à Chypre depuis 2023.
En revanche, et c’est un point important, le SARS-CoV-2 responsable de la COVID 19 qui nous a bien pourri la vie ces dernières années, appartient au genre Betacoronavirus, qui n’a donc rien à voir avec le FCoV. Donc, ce qu’il faut retenir de tout cela, c’est que si votre chat a la PIF, c’est bien embêtant pour lui, mais vous n’allez pas attraper la COVID, et vous n’allez pas mourir !

Représentation schématique du FCoV (d’après E. Barker, University of Bristol, cité par S. Tasker, 2023) : son enveloppe lipidique dérive de la membrane d’une cellule de chat, (la cellule dans laquelle le virus s’est répliqué), membrane dans laquelle sont venues s’insérer des protéines virales : les protéines de surface (S), qui donnent au virus sa forme en couronne, d’où le nom Coronavirus. Ce sont elles qui reconnaissent les récepteurs présents sur les cellules du chat, se lient à ces récepteurs, et permettent ensuite au virus de pénétrer dans la cellule. Les protéines de l’enveloppe (E) interviennent (entre autres), dans l’assemblage et la formation de l’enveloppe, et la libération de nouveaux virus. Les protéines membranaires (M), les plus abondantes, maintiennent toute la structure en place. A l’intérieur, la protéine de la nucléocapside (N) protège et stabilise l’ARN viral, ce dernier porteur du code génétique permettant la fabrication des protéines qui donneront naissance à de nouveaux virus. Ce descriptif étant très résumé et schématique !
Histoire de mettre cette question de côté, vous lirez peut-être qu’il existe des coronavirus félins de type I et de type II, le type I étant le plus fréquent, (80 à 95% des FCoV dans le monde), et le type II, résultant de recombinaisons entre le type I et le coronavirus canin, moins fréquent, mais plus facile à étudier en laboratoire. Mais en pratique, on s’en moque un peu, dans la mesure où tous les deux peuvent se présenter à la fois sous une forme peu dangereuse, ou sous la forme responsable de la PIF : on en parle plus loin.
Les coronavirus, on l’a vu, sont des virus enveloppés et ça peut paraître contre-intuitif, comme ça, mais en dehors de l’hôte, un virus enveloppé est plus fragile qu’un virus nu. En effet l’enveloppe peut être facilement détruite (par exemple, rien qu’en se lavant les mains). Pour un virus enveloppé, le FCoV est tout de même assez résistant : en particulier, il se conserve assez bien à l’intérieur d’une matière organique (typiquement, dans des selles). Il résiste également bien aux températures basses, alors qu’il commence à être inactivé quand la température atteint 37°C, et qu’il ne résiste pas à un lavage à 60°C. Il est également sensible à la plupart des désinfectants, détergents, et à la vapeur. Dans des conditions favorables, (en milieu sec, comme dans un tapis), il peut survivre jusqu’à 7 semaines, et donc être transmis par des vêtements, jouets ou brosses.
2 – Gentil virus, ou méchant virus ?
Alors, le FCoV, c’est un peu Docteur Jekyll et Mister Hyde chez les virus, et on n’a pas fini de parler de cette dichotomie dans cette page. Donc, le FCoV peut se présenter sous la forme de deux « pathotypes » ou « biotypes » : le coronavirus félin entérique (FECV) qui, comme son nom l’indique, se multiplie dans les cellules de l’intestin du chat (= entérocytes), où il se tient à peu près tranquille et ne cause pas trop de problèmes : une petite diarrhée de temps en temps et encore, pas toujours ; et le virus félin de la péritonite infectieuse (FIPV) qui,
lui, se multiplie dans certaines cellules sanguines (monocytes) et tissulaires (macrophages – on précisera la différence dans la partie consacrée à la pathogénie). Ces cellules vont le disséminer dans tout l’organisme (distribution systémique), où il provoquera une maladie systématiquement mortelle, du moins sans traitement. Comme les choses ne sont jamais aussi simples qu’on le voudrait, il arrive parfois que le coronavirus intestinal aille, lui aussi, se multiplier ailleurs dans l’organisme, sans pour autant provoquer une PIF… mais bon, on va en rester sur cette idée d’un FECV gentil dans l’intestin, d’un FIPV méchant qui se promène, et on nuancera quand ce sera nécessaire.

Maintenant, me direz-vous, ils sortent d’où, ces deux virus ? Eh bien il faut savoir qu’une des particularités des coronavirus en général et du FCoV en particulier, c’est que quand ils dupliquent leur ARN, (pour se multiplier), ils se trompent souvent : et on se retrouve avec des mutations ponctuelles, des recombinaisons, des morceaux d’ARN qui se perdent en route (délétions)… et que quand ce genre de mutation arrive chez un gentil FECV qui n’a d’autre but dans la vie que de rester bien tranquille dans ses entérocytes, il peut se transformer en un méchant FIPV qui, lui, préfère partir à l’aventure à l’intérieur des monocytes et des macrophages ! Sachant que les mutations touchant les gènes codant pour la protéine S dont on a parlé plus haut, (celle qui permet notamment au virus de pénétrer dans une cellule), semblent jouer un rôle particulièrement important dans la bascule du FECV vers le FIPV. Bon, il existe d’autres théories, mais celle-ci est la plus largement acceptée. Et déjà, on voit poindre une difficulté pour la suite : c’est que comme la mutation qui conduit un FECV à devenir FIPV ne porte souvent que sur un tout petit morceau d’ARN, il y aura très peu de différence, parmi les chats d’une même maison, entre le FECV présent dans les selles d’un chat en bonne santé, et le FIPV muté de son coloc atteint de PIF. Et même, ces deux virus seront plus semblables entre eux, que le FECV du chat en bonne santé, et le FECV présent dans les selles du chat d’une autre maison. Du coup, avec plus de différences entre les ARN de deux virus gentils, qu’entre les ARN d’un virus gentil et d’un virus méchant… bon courage pour le diagnostic !
Epidémiologie : comment il se transmet ?
1 – L’excrétion du virus
Une petite définition pour commencer : l’épidémiologie (en l’occurrence, ici, de la PIF), c’est l’étude, au sein d’une population de chats, de la fréquence et de la répartition de la maladie dans le temps et dans l’espace, ainsi que le rôle des facteurs qui les déterminent.
Comme il faut bien commencer quelque part, on va partir de l’excrétion du FCoV dans les selles d’un chat porteur, puisque le coronavirus non muté, on le rappelle, se multiplie dans les cellules intestinales du chat. (On peut mentionner qu’en début d’infection, on trouve aussi le virus dans la salive, (replication dans les amygdales), dans les sécrétions respiratoires et dans les urines, mais tout cela reste marginal).
L’excrétion du FCoV dans les selles commence dès le deuxième jour (!) après l’infection, et elle continue ensuite pendant des jours, des semaines, des mois… voire toute la vie du chat ! Mais en général, on est plutôt entre quelques semaines et quelques mois, après quoi l’excrétion s’arrête. Elle peut aussi être intermittente, s’arrêtant, reprenant, puis s’arrêtant à nouveau… En sachant que parfois, si elle reprend, c’est parce que le chat s’est recontaminé, l’immunité induite par le FCoV étant de courte durée. Dans une étude (Addie & Coll, 2001) particulièrement remarquable par la durée du suivi (jusqu’à cinq ans), et le nombre de chats (155 naturellement infectés par le FCoV, appartenant à 29 propriétaires différents), 18 chats (11,6%) ont excrété du virus en continu pendant toute la durée de l’étude, sans qu’aucun d’eux, soit dit en passant, ne développe une PIF. 56 (36%) ont cessé d’excréter du virus après un certain temps et 44 (28%) en ont excrété de façon intermittente pendant la durée du suivi… à moins qu’ils ne se soient régulièrement ré-infectés auprès de leurs congénères. Dans ces cas d’excrétion intermittente, 73% des épisodes d’excrétion ont duré moins de trois mois, et 95% moins de 9 mois. Quant aux 24% de chats restants, on n’a jamais trouvé de virus dans leurs selles… ce qui n’exclut pas qu’il ait pu y en avoir avant ou après les prélèvements.
Vous assistez ici à l’excrétion (et, de ce fait, la dissémination), du FCoV. (Enfin, si le chat est infecté, bien sûr). Mais comme on le verra au paragraphe suivant, si les selles sont soigneusement recouvertes tout de suite après, il y aura peu de chances qu’un autre chat vienne les renifler de trop près et se contamine, contrairement à ce qui se passe dans une litière commune à plusieurs chats.
Si l’on considère maintenant les chats séropositifs pour le FCoV, un tiers d’entre eux excrètent le virus. Le degré de séropositivité est directement corrélé avec la replication du virus et sa quantité dans l’intestin : les chats très séropositifs excrètent plus souvent et de plus grandes quantités de virus que les chats faiblement positifs. Les chatons excrètent également de grandes quantités de virus.
Et quid des chats à PIF ? nous demanderez-vous. Parce que c’est quand même d’eux qu’on pourrait craindre les pires contaminations, avec notamment du virus muté ! Eh bien non, pour la bonne raison que le virus muté, qui a acquis la faculté de se répliquer dans les monocytes et les macrophages, a du même coup perdu celle de se répliquer dans les cellules intestinales ! (Eh oui, on ne peut pas tout avoir). Les chats atteints de PIF se limitent donc à excréter du FCoV non muté, et qui plus est, en faible quantité : ils ne sont donc pas directement contagieux pour la PIF, et ils ne le sont même que faiblement pour le « simple » FCoV intestinal.
2 – La transmission
Le virus est excrété, il faut maintenant qu’il circule.
Comme le FCoV se multiplie dans les cellules de l’intestin du chat et que son excrétion se fait quasi-exclusivement dans les selles, les chats se contamineront… par les selles (il y a une certaine logique dans tout ça) : contamination directe en reniflant une crotte, et en la léchouillant au passage ; et surtout contamination indirecte par la litière, (y compris le bac et la pelle), les brosses (si le chat s’en est mis plein les poils), les chaussures (si on a marché dedans)… mais aussi par le léchage des pattes quand Garfield fait sa toilette après être allé à la litière. (Comme quoi, des fois, il n’est pas bon d’être trop propre. Oups !). Photo ci-contre : si le chat qui vient de sortir du bac avait du FCoV dans l’intestin, les prochains utilisateurs risquent fort de l’attraper !

Après, toutes sortes d’autres voies d’entrée ont été envisagées : les échanges de salive chez les chats qui mangent dans la même gamelle, mais comme le FCoV n’a été retrouvé que très rarement dans la salive, ce mode de contamination reste très occasionnel. Même chose pour la voie respiratoire (éternuements). La transmission de la chatte au chaton à travers le placenta est possible, mais franchement rare : quand des chatons sont contaminés, c’est plutôt à 6-8 semaines, quand les anticorps maternels (protection héritée de la mère), disparaissent… et au contact de selles contaminées, comme tout le monde. La transmission par voie vénérienne est très improbable ; par transfusion, jamais décrite ; par acarien ou insecte vecteur (puces notamment), jamais confirmée.
En conclusion, la transmission se fait directement ou indirectement par ingestion de selles, et tout le reste est accessoire.
Rappelons ce qu’on a dit un peu plus haut : le FCoV est relativement fragile : il est assez vite inactivé dans le milieu extérieur, et détruit par la plupart des désinfectants et détergents. Cependant, il peut survivre jusqu’à 7 semaines en milieu sec (tapis), et donc être transmis par des vêtements, jouets ou brosses.
3 – La prévalence
Déjà, on va donner une définition de la prévalence : selon le dictionnaire de l’Académie Nationale de Médecine, il s’agit du nombre total de cas d’une maladie donnée dans une population déterminée, sans distinction entre les cas nouveaux et les cas anciens, au cours d’une période de temps définie ou à un instant défini.
Prévalence du FCoV
Concernant le FCoV, (on parle bien du virus, pas de la maladie PIF), on le trouve partout dans le monde, sauf sur quelques îles particulièrement perdues : on citera par exemple les Malouines et les Galapagos, avec une prévalence de 0%, que ce soit chez les chats domestiques ou chez les chats féraux (= chats domestiques, ou leurs descendants, retournés à l’état sauvage). Logiquement, en revanche, le virus prospère particulièrement dans les collectivités, (maisons multi-chats, refuges, élevages…), partout où il y a plein de chats qui défèquent dans la même litière, après avoir reniflé la crotte du chat précédent, et avant de se lécher les pattes une fois sortis. Le risque de se contaminer et de transmettre le virus est évidemment beaucoup moins important pour des chats vivant seuls ou à deux avec accès à l’extérieur, (utilisant donc peu la litière), ou pour des chats sauvages ou féraux, qui ont rarement l’occasion de lécher les crottes des autres, et enfouissent soigneusement les leurs.

Même s’ils vivent en groupe, les chats errants ou féraux ont un risque moins important d’attraper un FCoV que les chats vivant à plusieurs dans une maison, sans accès à l’extérieur (où l’on peut faire ses crottes où l’on veut, puis les recouvrir), et qui se soulagent tous dans le même bac à litière.
Les chats de race semblent aussi davantage exposés que les matous de base… sans qu’on puisse cependant déterminer si c’est parce qu’ils sont de race… ou parce qu’ils ont passé leurs premières semaines de vie dans des élevages où, on l’a vu, le virus circule davantage. Pour prendre, maintenant, quelques exemples : en Grande Bretagne, une étude a montré que 82% des chats d’exposition, 53% des chats d’élevage et 15% des chats de maison vivant seuls étaient séropositifs. Toujours en Grande-Bretagne, parmi 2214 chats accueillis dans 14 refuges, ceux y ayant passé plus de 60 jours avaient 5 fois plus de risques d’être séropositifs qu’à leur arrivée (TA Cave, 2004). Certains auteurs postulent qu’outre l’exposition au virus et la circulation de ce dernier dans les refuges, le stress lié à la perte ou à l’abandon, puis à la vie en groupe, pourrait favoriser encore davantage l’infection par le FCoV. Dans une étude japonaise portant sur 17 392 chats (Taharaguchi, 2012), , 67% des chats de race étaient séropositifs, contre « seulement » 31% des chats sans pédigrée. La séroprévalence atteignait même 80% chez les chatons de race de 3 mois, et ce taux se maintenait jusqu’à l’âge de 2 ans, avant de diminuer progressivement pour atteindre 30% à 14 ans. (Chez les chats sans pédigrée, c’était 30% toute la vie). Dans une étude italienne, sur 120 chats de refuge, 82% étaient séropositifs pour le FCoV. On trouvera plein d’autres exemples de prévalence en fonction, (entre autres), du pays, du mode de vie et du pédigrée du chat, dans une quarantaine de publications citées dans l’article de S Tasker & Coll (2023).
Prévalence de la PIF
Deux études états-uniennes de grande ampleur ont montré une faible prévalence de la PIF dans une population de chats malades – toutes maladies confondues. (Chats qu’on peut même supposer « bien » malades, dans la mesure où ils étaient présentés dans des centres de référés, Université ou hôpitaux vétérinaires) : cette prévalence était, dans un cas, de 0,5%, (60 chats sur 11 535)(Pesteanu-Somogyi, 2006), et dans le second cas, de 0,4% (1 420 sur 397 182)(Rohrbach, 2001). Concernant le pourcentage de chats infectés par le FCoV qui développeront une PIF, les chiffres varient selon les études, mais tournent en général entre 5 et 10%. Logiquement, les chats de race et ceux de moins de 2 ans, qui sont le plus souvent infectés par le FCoV, sont aussi ceux chez qui l’on trouvera le plus de PIF. Pour ce qui est de la race, dans une étude australienne, 77% des chats présentant une PIF étaient des chats de pure race ; et dans une étude réalisée en Caroline du Nord, 1,3% d’une population de chats de race présentaient une PIF, contre 0,35% chez les chats sans pédigrée… sachant qu’ensuite, les races les plus ou les moins représentées varient selon les études. Pour ce qui est de l’âge, dans une publication allemande portant sur 222 chats à PIF, 39% avaient moins de 1 an (Riemer & Coll, 2016).
Pour le reste, certaines études trouvent que les mâles sont plus à risque de faire une PIF que les femelles… et d’autres études concluent que non. Certaines constatent qu’on voit plus de PIF en hiver, (de janvier à avril), d’autres qu’on en voit plus en automne et en hiver. Enfin, il existe une prédisposition génétique à développer une PIF chez les chats infectés par le FCoV, ce qui aura bien sûr des répercussions sur le choix des reproducteurs, notamment en élevage : on en reparle dans la partie « Prévention » (Taylor & Coll, 2025).
Pathogénie
On trouve de nombreuses définitions du terme « pathogénie » : une qui a l’avantage d’être simple nous dit qu’il s’agit du « processus par lequel une cause pathogène » (par exemple une bactérie, un virus…), « agit sur l’organisme et détermine une maladie ». On pourrait ajouter que la réponse de l’organisme à la cause pathogène, (ici le FCoV), n’est pas forcément adaptée et peut faire autant, voire plus de dégâts, que l’agent pathogène lui-même. En l’occurrence, la PIF est souvent définie comme une maladie à médiation immune induite par un coronavirus félin.
Bon, ce n’est pas le paragraphe le plus fou-fou de l’article, et on est tout à fait autorisé à le sauter (on est autorisé à faire ce qu’on veut, de toute façon), mais si l’on s’accroche un peu, on peut y glaner des infos qui seront utiles pour la compréhension de la suite, diagnostic et traitement, notamment. Allez, c’est parti.
1 – Pathogénie de l’infection intestinale
Après infection d’un nouveau chat à partir des selles d’un chat porteur, le virus arrive dans l’intestin, où il se réplique dans les cellules de l’épithélium intestinal, ce qui peut causer leur destruction, et une diarrhée. Le plus souvent cependant, le chat ne présente aucun symptôme, donc, tout va bien – si ce n’est que comme on l’a vu, il se met quand même rapidement à excréter, à son tour, du virus. Des diarrhées sévères, voire fatales, et des infections de l’appareil respiratoire supérieur ont tout de même été décrites, mais cela reste tout à fait exceptionnel.
2 – Pathogénie de la PIF : mutation, réplication…
On en a parlé plus haut : pour que la PIF se développe, il faut que survienne une mutation spontanée chez le gentil FCoV intestinal. C’est une lapalissade, mais il y a forcément plus de risques de mutation (= d’erreurs de replication de l’ARN) chez un chat hébergeant une multitude de virus qui n’arrêtent pas de se multiplier, que chez un chat qui n’hébergerait que quelques virus qui ne se multiplient presque pas : ce qui explique que, comme on l’a vu dans les paragraphes précédents, la PIF apparaisse plus facilement chez un individu jeune, qui se réinfecte en permanence parce qu’il vit en collectivité, et que lui et ses copains se refilent mutuellement le virus à l’infini, notamment par l’intermédiaire de litières communes. L’ARN viral peut subir de multiples mutations à l’origine de la transformation du FECV en FIPV, mais une attention particulière a été portée au gène codant pour la protéine S dont on a parlé plus haut, qui permet au virus de pénétrer dans une cellule et de fusionner avec elle. Un changement de la protéine S entraîne un changement de tropisme du virus qui se désintéressera de ses habituelles cellules intestinales au profit des monocytes et macrophages, à l’intérieur desquels il va se répliquer, et partir se promener un peu partout dans l’organisme du chat. (Petit aparté à propos des monocytes et des macrophages, pour savoir de quoi on parle : en bref, les monocytes (cellules sanguines), sont les précurseurs des macrophages : quand les monocytes quittent le sang et passent dans les tissus, ils se différencient en macrophages, qui sont des sortes de nettoyeurs qui ingèrent (phagocytent) toutes les grosses particules qui traînent et qui leur semblent anormales : bactéries, cellules abimées, particules étrangères, etc).
Le système immunitaire du chat joue un rôle important dans cette histoire : s’il est compétent, il va réussir à éliminer le virus et il n’y aura pas de portage du FCoV ni, a fortiori, de PIF. S’il l’est un peu moins, (naturellement, ou à cause d’une infection concomitante, d’un traitement immunosuppresseur, d’un stress…), le chat ne pourra pas se débarrasser du FCoV, en restera porteur et l’excrètera pendant des mois ou des années, avec toujours le risque d’une mutation. Et puis parfois, le système immunitaire se met à faire vraiment n’importe quoi, et c’est la réponse immunitaire qui va être à l’origine d’une bonne partie des dégâts (on parle d’affection à médiation immune), avec notamment une attaque de la paroi des vaisseaux sanguins mais ça, on en reparle au paragraphe suivant.
Donc si on récapitule, l’apparition d’une PIF dépendra 1) de la charge virale (il y a beaucoup ou pas beaucoup de virus), 2) du type de mutation sur l’ARN du FECV, dont dépendra la virulence du virus muté, et 3) de la réponse immunitaire du chat.
3 – …et développement de la maladie
Donc, voici notre FCoV embarqué dans un monocyte du sang : que lui arrive-t-il ensuite ? Le monocyte va aller se fixer sur la paroi d’une veine de petit ou de moyen diamètre, et larguer une enzyme qui va attaquer la paroi du vaisseau, ce qui permettra la sortie en direction des tissus, à la fois des monocytes qui vont se différencier en macrophages, et aussi du plasma du sang, qui va se répandre à l’extérieur des vaisseaux. Et plus la PIF est aiguë, plus le nombre de vaisseaux lésés est important, l’épanchement de plasma augmentant en proportion. Ajoutons à cela que les macrophages chargés de virus qui meurent (on appelle ça l’apoptose) libèrent de nouveaux virus, (et hop, la dissémination continue), ainsi que diverses substances, dont des substances vasoactives, qui vont encore augmenter la perméabilité des vaisseaux et l’exsudation de protéines plasmatiques. Et comme si tout cela ne suffisait pas, on assiste aussi à la formation de complexes immuns : on dira schématiquement que les antigènes (les virus) et les anticorps (des molécules assurant la défense de l’organisme), forment des complexes qui, quand ils sont trop nombreux, et avec l’intervention d’un troisième larron (le complément), augmentent encore l’inflammation, à la fois des vaisseaux et des tissus autour.
Donc, si on met tout cela bout à bout : les formes aiguës de PIF se caractérisent par des lésions importantes sur la paroi de nombreux vaisseaux, entraînant la formation d’épanchements dans les cavités : thorax, abdomen, ainsi que dans le péricarde : c’est l’une des manifestations les plus évocatrices de la PIF, on reverra ça plus loin, avec les symptômes. On parle de PIF humide. A l’inverse, dans les formes plus chroniques, les vaisseaux lésés sont moins nombreux et, de ce fait, les épanchements moins importants, voire quasiment absents. On constate, en revanche, en périphérie des vaisseaux dans différents organes, (notamment le péritoine, le rein et l’uvée de l’œil), la formation en plus grand nombre de pyogranulomes, (= accumulation de macrophages et de polynucléaires neutrophiles), qu’un examen rapide pourrait parfois faire prendre pour des tumeurs. On parle alors de PIF sèche. Evidemment, il existe des chevauchements entre les deux formes !
Histoire d’en remettre une couche, ajoutons que l’inflammation des vaisseaux, (vascularite à médiation immune), peut provoquer une coagulation intra-vasculaire disséminée (CIVD), c’est à dire que le sang se met à coaguler un peu partout dans la circulation, ce qui, évidemment, n’est pas normal du tout et va poser des problèmes. (On ne détaillera pas ici les mécanismes de la CIVD, sinon on ne va jamais s’en sortir !)
On pourrait continuer comme ça longtemps, mais on va peut-être en rester là ! Retenons en tout cas que dans la PIF, les lésions sont dues à l’action du virus lui-même, mais aussi, et peut-être surtout, à une réaction inadaptée du système immunitaire du chat.
4 – Est-ce que l’immunité sert quand même à quelque chose ?
Evidemment, ce serait trop beau si la réponse était simple, du coup, on va s’en tenir aux grandes lignes, pour éviter de (trop) se perdre dans les détails :
Les chats résistants à la PIF ont une forte immunité à médiation cellulaire (IMC) : comme son nom l’indique, il s’agit d’une immunité qui repose sur l’action de cellules, (lymphocytes T régulateurs et Natural killers, notamment) et c’est le principal mécanisme de protection et d’élimination des agents infectieux qui se cachent à l’intérieur des cellules, en particulier les virus. A contrario, le développement d’une PIF est souvent associé à un effondrement des lymphocytes T régulateurs et Natural killers. L’interféron gamma est un important modulateur de l’immunité à médiation cellulaire : son taux dans le sérum est élevé chez les chats infectés par le FCoV qui ne présentent pas de symptôme, mais faible chez les chats qui développent une PIF.
L’immunité à médiation humorale ne repose pas sur l’action directe de cellules, mais sur la production d’anticorps par les plasmocytes, cellules qui résultent de la différentiation de lymphocytes B. (Il existe aussi des lymphocytes B mémoire qui, comme leur nom l’indique, mémorisent les propriétés de l’antigène les ayant activés ; ce qui fait que si celui-ci repointe un jour le bout de son nez, la réponse immunitaire sera d’emblée rapide, intense et spécifique). Contrairement à l’immunité à médiation cellulaire, l’immunité humorale est principalement dirigée contre les agents infectieux extracellulaires tels que les bactéries… donc moins adaptée à la lutte contre les virus. Mais a-t-elle tout de même un intérêt ? Ce n’est pas clair : il semble que les anticorps maternels protègent les chatons contre le FCoV jusqu’à l’âge de 5-6 semaines, avant de décliner à 6-8 semaines. En revanche, on a vu plus haut les dégâts causés par les complexes antigènes-anticorps, qui sont finalement à l’origine des lésions les plus sévères.
Plus concrètement, un signe que l’immunité sert quand même à quelque chose, est qu’un stress récent est fréquemment rapporté chez les chats ayant déclaré une PIF. On parle bien sûr ici de stress au sens large, et pas uniquement du jour où Garfield a croisé un Pitbull dans la rue ! (Quoique…). Il pourra donc s’agir d’une perte ou d’une abandon, a fortiori si le chat se retrouve ensuite dans un refuge, d’une adoption ou d’un déménagement, d’une intervention chirurgicale (stérilisation notamment), d’une maladie intercurrente (on cite souvent le coryza), d’une vaccination, de l’arrivée d’un nouveau chat à la maison, etc. Tous ces événements peuvent contribuer à la sortie d’une PIF chez un chat déjà infecté par un FCoV. Dans une vaste étude portant sur 629 chats atteints de PIF (M. Ansari Mood, 2026), 557 avaient été soumis à un ou plusieurs stress potentiels dans le mois précédant l’apparition des symptômes : en gros, dans la moitié des cas, un événement « traumatisant » comme ceux cités ci-dessus, (abandon etc), et dans l’autre moitié, une maladie ponctuelle, (un épisode de diarrhée), ou plus chronique. Chez Riemer & Coll (2015), des événements stressants ont précédé, (il n’est pas précisé de combien), le diagnostic de PIF, chez 131 chats sur 231 (56,7%) : adoption (38 cas), passage en refuge (31 cas) et intervention chirurgicale (29 cas), arrivant devant les autres causes. Alors on pourra dire qu’on arrivera toujours à trouver un épisode stressant dans le mois précédant un événement donné, mais de nombreuses études vont quand même dans le même sens, et nous-mêmes avons pu observer le cas d’une jeune chatte sortant d’un élevage, et qui a déclenché une PIF une semaine après sa stérilisation, à l’âge de 5,5 mois.
Symptômes et lésions
Déjà, juste un mot pour dire qu’on ne s’attardera pas sur les symptômes dus au FCoV non muté, vu qu’on en a déjà parlé… et qu’il n’y a pas grand chose à en dire ! Les chatons issus de portées infectées auraient tout de même une croissance altérée, et davantage d’épisodes de diarrhée et d’atteinte des voies respiratoires supérieures. Dans une étude allemande portant sur 234 chats d’élevage, on a relevé une association significative entre infection par le FCoV et diarrhée. D’autres études ont montré une association entre diarrhée chronique et portage du FCoV. De rares cas d’entérites sévères, et parfois mortelles, ont tout de même été décrits. Ceci étant, même quand des symptômes digestifs dus à la présence d’un FCoV sont présents, il est rare qu’ils soient suffisamment visibles pour que le propriétaire les remarque et présente son chat en consultation.
Maintenant qu’on a réglé le sort du FCoV, venons-en à la PIF : ici, les symptômes sont la conséquence directe des vascularites, responsables d’épanchements et d’insuffisances organiques par défauts de vascularisation. et/ou des lésions pyogranulomateuses, qui peuvent conduire à la formation de masses dans différents organes ; et, bien sûr, de la localisation dans l’organisme de ces deux catégories de lésions.
Le délai entre la mutation et l’apparition des signes cliniques varie de quelques semaines à deux ans, selon le statut immunitaire du chat. Le délai entre l’infection par l’inoffensif FCoV et le développement de la PIF est encore plus imprévisible :
le risque de développer une PIF est maximal dans les 6-18 mois après infection par le FCoV, et tombe à 4%, 36 mois après l’infection.
Photo ci-contre : les choses sont malheureusement allées très vite chez ce jeune chaton de moins de trois mois, présenté en très mauvais état général avec un abattement, une maigreur extrême, des muqueuses pâles et une importante distension abdominale. Le chaton était négatif pour le FeLV et le FIV, mais avait une RT-PCR fortement positive pour le FCoV.

On en a déjà pas mal parlé, il existe deux formes de PIF : la forme humide, exsudative, (c’est à dire qu’on a du liquide qui s’accumule quelque part dans l’organisme), avec péritonite fibreuse, pleurésie et/ou péricardite, et la forme non exsudative, sèche, granulomateuse… à quoi s’ajoute parfois un petit pourcentage de formes mixtes. Pour donner une idée des proportions : 78% de formes humides parmi 224 chats atteints de PIF chez Riemer & Coll (2016), 109/127 (85,8%) chez Yin & Coll (2021), ou encore 466/629 (74,1%) chez Ansari Mood (2026). Mais en fait, il faut bien dire que les deux formes se chevauchent, et il y a toujours plus ou moins des épanchements et plus ou moins des lésions granulomateuses, selon le chat, à un moment donné ! L’évolution est généralement rapide dans les formes humides, (quelques semaines, voire quelques jours), alors qu’elle est plus lente (jusqu’à plusieurs mois), dans les formes sèches.
Maintenant, dans le détail :
1 – Symptômes généraux (et non spécifiques)
La fièvre est fréquente chez les chats atteints de PIF : dans l’étude de Riemer & Coll, 91/111 (81%) des chats étaient en hyperthermie (≥ 39,5°C) lors de la première consultation, dont près de la moitié > 40°C, ce pourcentage étant plus élevé chez les chats présentant un épanchement. Ils étaient 505/629 (80,3%) à avoir une température > 39,4°C dans l’étude de M. Ansari Mood… mais seulement 43% chez Coggins & Coll. En prenant le problème dans l’autre sens, dans une étude portant sur 106 chats référés à l’université de Bristol pour explorer une fièvre d’origine inconnue, 22 (20,8%) étaient atteints de PIF (SE Spencer & Coll, 2017). Concernant les autres symptômes peu spécifiques, (on se limitera aux études de Riemer et Ansari Mood qui s’appuient sur les effectifs les plus importants, avant de nous noyer dans les chiffres et de trop nous embrouiller), respectivement 87% et 95% des chats avaient des commémoratifs d’abattement, et 66% et 91% de baisse ou perte d’appétit.

Les chiffres concernant un mauvais état général (perte de poids), sont beaucoup plus inconstants, variant de 37% à 59% ou 89%, selon les publications. (Photo ci-contre, abattement et amaigrissement chez un jeune Chat des forêts norvégiennes, âgé de 14 mois, et atteint de PIF).
Attention, les symptômes peuvent évoluer au cours du temps, et un chat qui ne présente qu’une fièvre avec baisse d’appétit à J0, peut se retrouver avec un important épanchement quelques jours plus tard !
2 – Les épanchements
On l’a vu, les épanchements sont fréquents dans la PIF. Selon les publications, on les retrouve dans 175 cas sur 224 (78%) chez Riemer & Coll (2015), 23/28 cas (82%) chez Coggins & Coll (2023), 25/32 cas (78%) chez Greene & Coll (2023) et chez un pourcentage un peu moins important de chats dans la très vaste étude de Mansari Mood (2026), avec un épanchement dans « seulement » 345/629 cas (54,8%). Parmi ces épanchements, on trouve en premier lieu des ascites (= liquide dans l’abdomen) qui représentent respectivement, dans les trois premières publications citées, 78,3%, 69% et 64% des épanchements, des épanchements pleuraux (= dans la plèvre, qui entoure le poumon) dans 13,1%, 22% et 16% des cas avec épanchement, et les deux associés dans 8%, 9% et 20% des cas ; les épanchements péricardiques étant beaucoup plus rares.
Inversement, parmi 486 chats présentant une ascite, (associée, dans 32% des cas, à un épanchement pleural) (L. Letwin, 2025), la PIF arrivait en quatrième position (14% des cas), très près derrière les péritonites septiques, les cancers (tous deux à 17%) et les inflammations autres que la PIF (16%), insuffisance cardiaque et uropéritoine suivant, avec 9% des cas. Dans une étude rétrospective portant sur 306 chats présentant un épanchement pleural (Mueller & Col, 2019), une insuffisance cardiaque était la cause la plus fréquente (35% des cas), suivie par un processus cancéreux (31%), la PIF n’arrivant qu’en troisième position avec 9%, à égalité avec les pyothorax (= une plèvre pleine de pus).
Photo ci-contre : importante ascite chez ce pauvre petit chaton de trois mois, avec une forte charge de coronavirus détectée par RT-PCR dans le liquide d’épanchement.
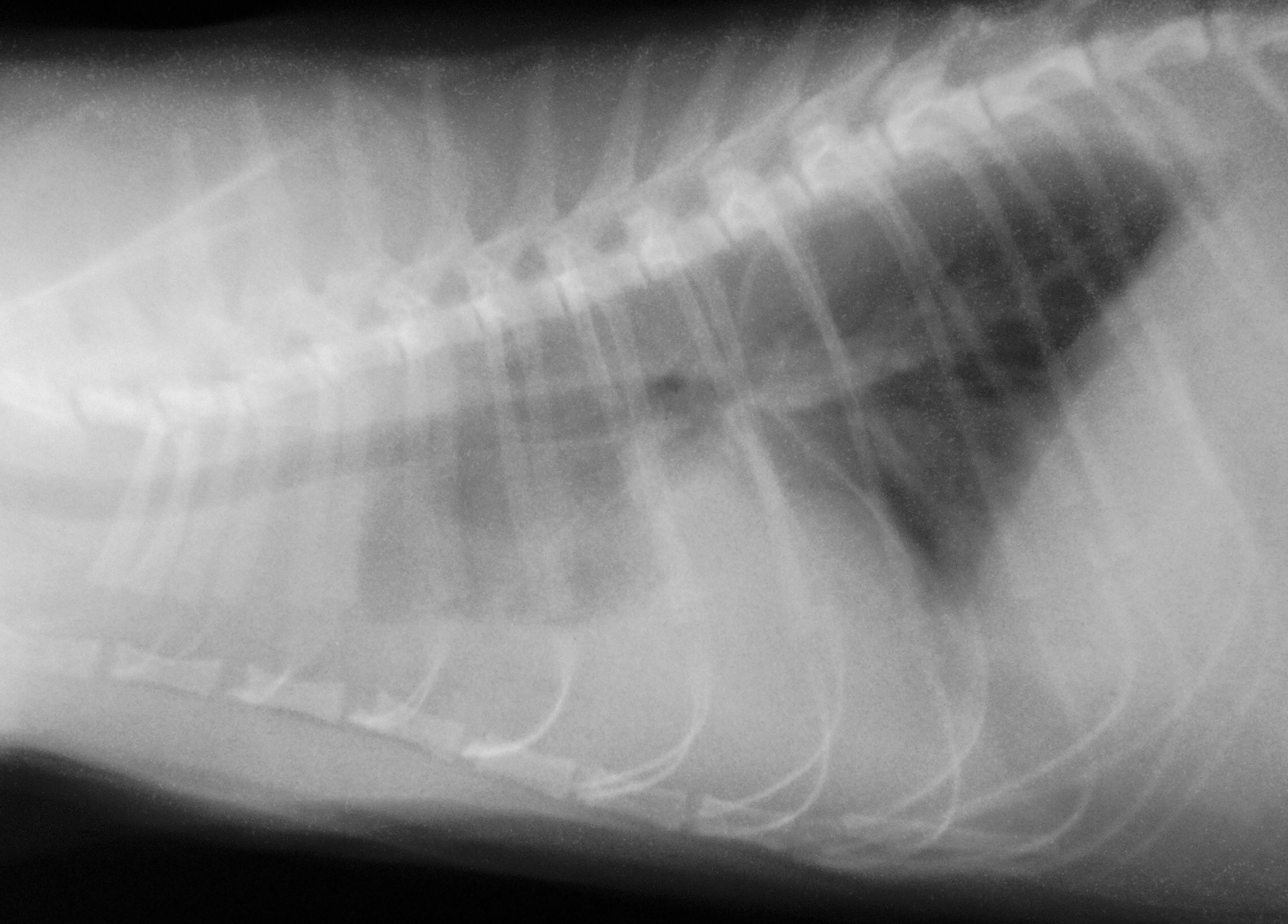
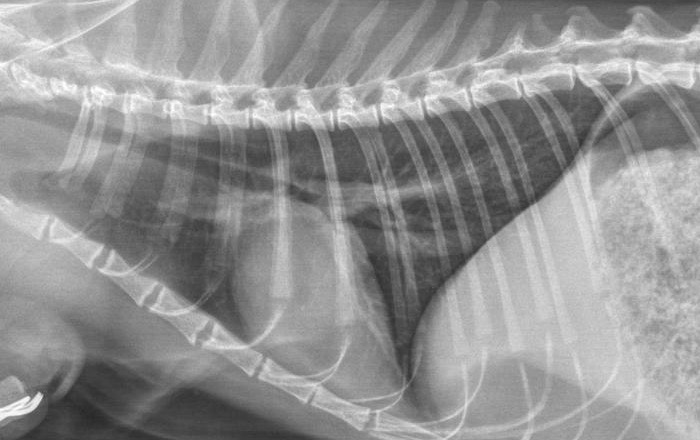
Photo de gauche : cette radio ancienne montre un
épanchement pleural, qui masque une grande partie du cœur et toute la partie crâniale du thorax (à gauche sur la radio), chez un chat de 1 an présentant une forme humide de PIF, avec également une ascite. Par comparaison, ci-dessus, une image normale du thorax chez un chat de 8 ans, également atteint de PIF, mais avec « seulement » une ascite modérée.
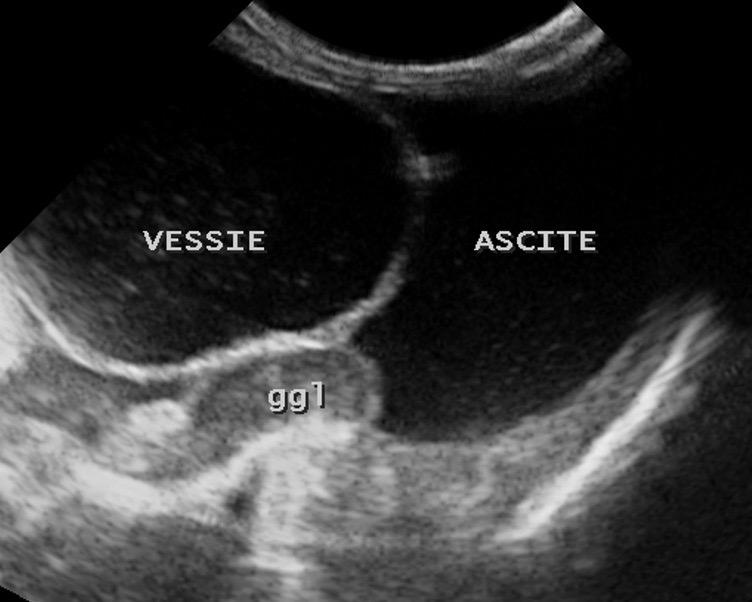
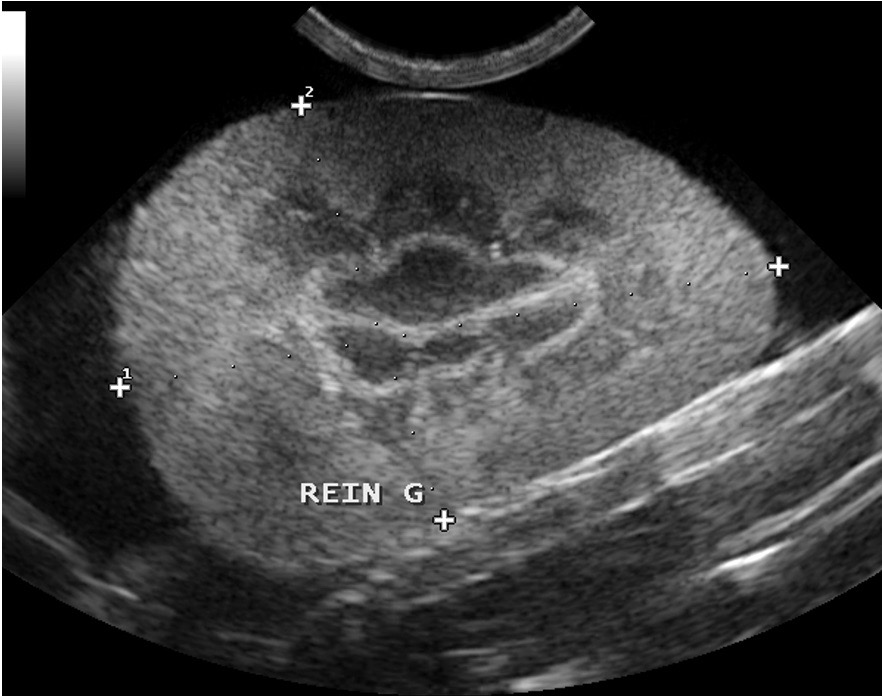
Deux images d’ascite importante chez des chats atteints de PIF : à gauche, seule la mince paroi de la vessie permet de distinguer le liquide à l’intérieur (l’urine) du liquide à l’extérieur (l’ascite). A droite : un rein perdu au milieu du liquide d’ascite ; on remarquera au passage la corticale rénale hyperéchogène, et aussi la présence d’un anneau médullaire (ou « medullary rim », cette ligne hyperéchogène qui suit la jonction cortico-médullaire) marqué : dans une étude portant sur la signification de cette image échographique dans le rein des chats (Ferreira & Coll, 2020), sur 23 chats atteints de PIF, 15 présentaient cet anneau médullaire, le plus souvent épais, et 8 ne le présentaient pas. Pour les auteurs, cette différence permet de conclure à une association significative entre anneau médullaire et PIF. Donc un indice diagnostique intéressant mais bon, ce n’est pas parce qu’on voit un anneau médullaire dans le rein d’un chat que celui-ci a forcément la PIF, et réciproquement !
On l’a déjà mentionné, mais on va le redire puisqu’on est dans le paragraphe consacré aux épanchements : l’évolution de la maladie est le plus souvent rapide (quelques jours à quelques semaines) chez les chats présentant une forme humide. En revanche, en l’absence d’épanchement, l’évolution sera souvent plus chronique, (sur plusieurs semaines, voire parfois plusieurs mois), et les symptômes de PIF généralement peu spécifiques, (cf paragraphe précédent), ou fonction de l’organe affecté par la maladie : système nerveux, yeux, reins, appareil digestif (on y range le pancréas et le foie), rate… On reparle de tout ça dans les paragraphes suivants.
3 – Atteinte des organes abdominaux et thoraciques
Parmi les organes touchés, on trouve d’abord l’intestin, (notamment le colon et la jonction iléo-cæcocolique), et les ganglions qui lui sont associés (ganglions mésentériques : l’hypertrophie de ces derniers est constatée dans environ 30% des cas – un peu plus, un peu moins, selon les études (Coggins & Coll, 2023 ; Katamaya & Coll, 2023), mais jusqu’à 16 cas sur 18, dans une publication. L’intestin épaissi ou les ganglions hypertrophiés donnent souvent une sensation de masse à la palpation de l’abdomen (dans 41% des cas, selon Yin & Coll, 2021). Ces lésions s’accompagnent généralement d’un amaigrissement, et de signes digestifs (vomissements, diarrhée ou constipation), dans 16,4% des cas. Elles sont également responsables d’une fuite protéique, dont nous reparlerons plus loin avec les signes biologiques. La taille des reins est souvent augmentée (rénomégalie)… mais elle peut parfois être diminuée. On observe occasionnellement un ictère (= une jaunisse) en cas d’atteinte hépatique, surtout chez les chats avec épanchement, et une pneumonie, responsable évidemment de difficultés respiratoires chez 7,7% des chats.
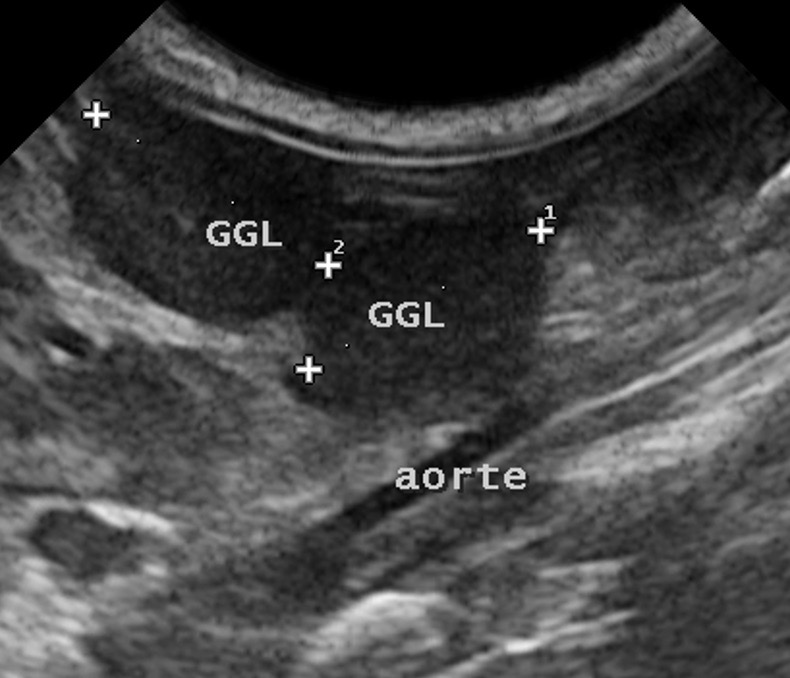
Ganglions de taille très augmentée chez deux jeunes chats atteints de PIF. A gauche : deux ganglions sous lombaires. A droite : très gros ganglions mésentériques (4 x 2 cm), bien palpables dans l’abdomen. En dessous de ces derniers, par comparaison, on peut voir un ganglion (NL = nœud lymphatique) de taille normale.
4 – symptômes oculaires
Les atteintes oculaires sont fréquentes dans la PIF, plus particulièrement dans les formes sèches, selon la plupart des auteurs. Dans l’étude de Mansari Mood, 227/629 chats (36,1%), présentaient des symptômes oculaires. Dans une étude de l’UC Davis, 33% des chats atteints de PIF sèche présentaient une atteinte oculaire, (dont près de la moitié (14%) n’avaient pas d’autre symptôme), ce qui n’était le cas que de 5,5% des chats atteints de forme humide (NC Pedersen, 2021). A noter que dans d’autres études, plus rares, les formes oculaires se retrouvent davantage dans les formes humides (13/15 cas chez Ziółkowska & Coll, 2017). Si l’on prend le problème dans l’autre sens, dans deux études portant sur des chats présentant une uvéite, (120 chats aux Etats-Unis, 92 chats au Royaume-Uni), la cause de l’uvéite a été la PIF dans 16% des cas, dans les deux études.
Cette uvéite est le plus souvent (mais pas toujours) antérieure, et peut être uni ou bilatérale. A l’examen, on peut observer (entre autres) un changement de couleur de l’iris, qui peut aussi apparaître « gonflé » ou nodulaire ; une différence de taille entre les pupilles (anisocorie) ; la présence de sang dans la chambre antérieure (hyphéma) ; et des dépôts inflammatoires (« mutton fat » = avec un aspect de graisse de mouton, selon la formule poétique des anglo-saxons), sur la face interne de la cornée. (cf la photo ci-contre : uvéite unilatérale avec dépôts inflammatoires chez un chat de 11,5 ans présentant une PIF sèche avec fièvre, adénomégalie mésentérique, et une RT-PCR sur sang fortement positive pour le FCoV).
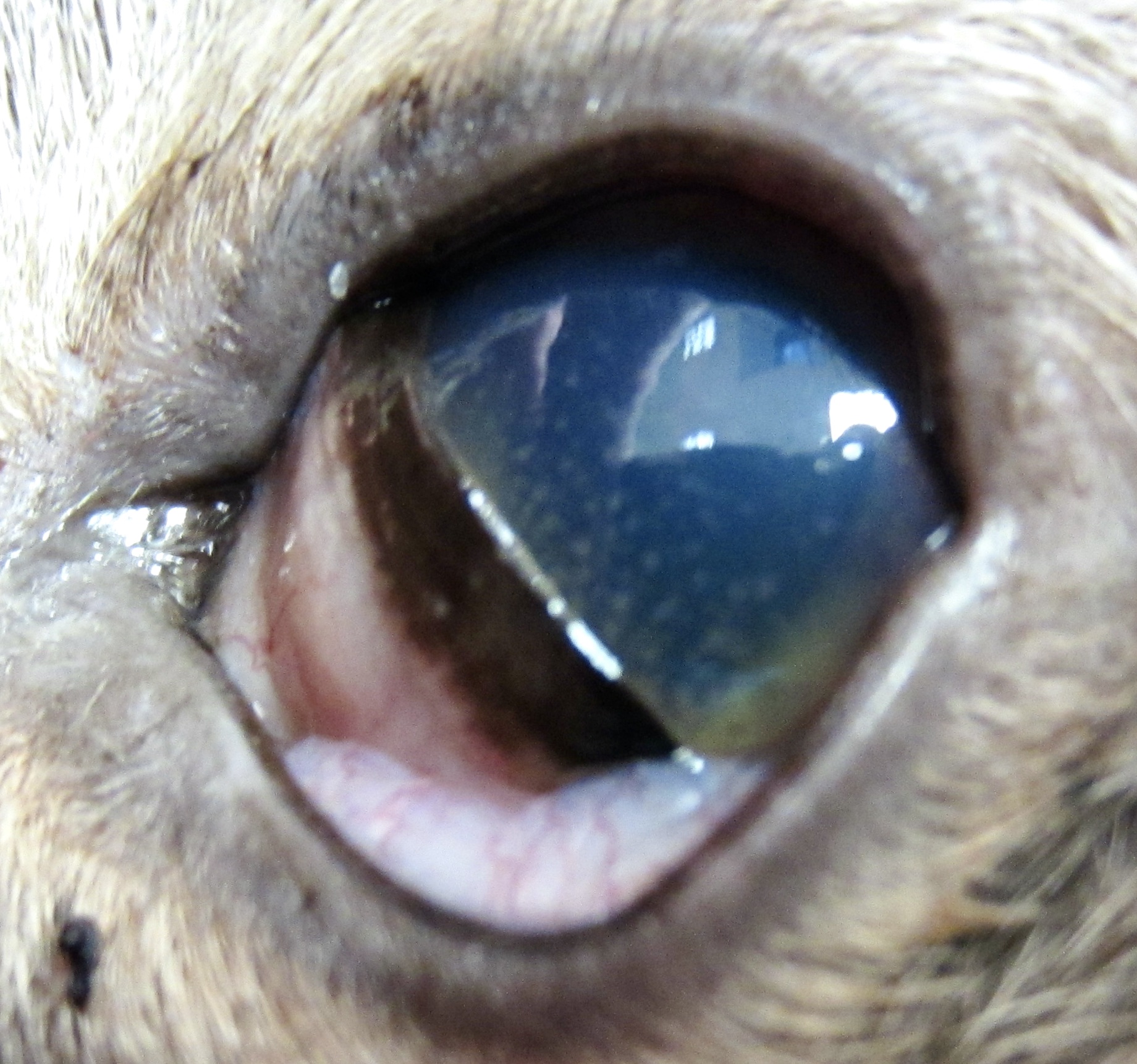
Les anomalies du fond d’œil sont fréquentes, avec notamment des lésions granulomateuses, des hémorragies ou des décollements de la rétine. Une cécité d’apparition brutale a aussi été décrite.
A noter que ces lésions oculaires ne sont pas pathognomoniques : on les retrouve notamment dans la toxoplasmose, les lymphomes, et les infections par le FeLV et le FIV.
5 – signes neurologiques
La PIF peut provoquer des lésions focales, multifocales ou diffuses dans le cerveau, les méninges et la moelle épinière ; autant dire qu’il y a de quoi faire ! L’atteinte neurologique n’est pas rare dans la PIF, touchant jusqu’à 30% des chats atteints (188/629 cas dans l’étude de Mansari Mood) ; pour d’autres auteurs, ce sera 10, 15 ou 17% des cas, (ce qui est déjà pas mal) et parfois, les troubles neurologiques seront les seuls symptômes présents (Rissi, 2018). Les chats présentant ce type de symptômes sont moins souvent hyperthermiques que les autres, et comme pour les symptômes oculaires, les signes neurologiques se rencontrent plus souvent chez des chats présentant une forme sèche (selon Foley & Coll, 2001, dans 1/3 à 1/4 des cas de PIF sèche)… ce qui fait qu’il n’est pas rare que ces deux catégories de symptômes soient associées (18,1% de formes « neuro-oculaires » chez Mansari Mood, contre « seulement » 4,8% de formes uniquement neurologiques, et 7,4% de formes seulement oculaires). Si l’on prend maintenant le problème dans l’autre sens, plus de la moitié des chats présentant des signes neurologiques d’origine inflammatoire ont été trouvés atteints de PIF. Dans une étude portant sur 221 chats présentant une affection de la moelle épinière, 18 (8%) avaient la PIF (Melia & Coll, 2020). Vu la variété de lésions et de localisations mentionnée ci-dessus, on ne sera pas surpris d’apprendre que les signes neurologiques peuvent être très variés : on observe notamment une ataxie, (en très résumé : un trouble de la coordination des mouvements volontaires et de l’équilibre), une hyperesthésie, (= une exacerbation de la sensibilité : on a mal pour un rien), un nystagmus (= mouvements involontaires des yeux), des convulsions, des changements dans le comportement et les états mentaux, et une atteinte des nerfs crâniens. En cas d’atteinte vestibulaire, on retrouvera ataxie et nystagmus, auxquels s’ajoutera une inclinaison de la tête. Des états d’obnubilation sont également décrits. Enfin, une hydrocéphalie, détectée au scanner ou à l’IRM, est très évocatrice d’une PIF.
A noter qu’une publication (Zwicklbauer & Coll, 2023) a décrit le cas de deux chats atteints de PIF, n’ayant présenté aucun signe neurologique avant ou pendant le traitement par le GS-441525, (patience, on en parle plus loin), et qui ont développé un syndrome d’hyperesthésie féline (FHS) respectivement 47 et 35 semaines après le début du traitement. Il s’agissait, dans le premier cas, de fréquents épisodes de tremblements des oreilles et de la peau des lombes occasionnant de violentes réactions de la part du chat, et de « tail chasing » (= courir après sa queue), après quoi l’animal allait se cacher. Ces symptômes se sont atténués progressivement au bout de 6 mois, sans traitement spécifique, et n’ont plus persisté par la suite que sous forme de très rares épisodes. (A voir sur une vidéo attachée à l’article original, en suivant ce lien). Le second chat a également présenté des tremblements de la peau du dos et de l’agitation, mais aussi des difficultés pour sauter et 48 heures d’anorexie avec un 40°C de température et une quantité minime d’ascite. Un nouveau traitement de 12 semaines de GS-441524 a été mis en place, mais les signes neurologiques ont persisté pendant ce traitement et n’ont fini par disparaître que quelques semaines ou mois après la fin du traitement. D’autres cas similaires ont été rapportés, mais non publiés. Les auteurs de l’article considèrent qu’il pourrait s’agir d’un « syndrome PIF long », comme il y a des Covid longs, éventuellement d’un effet secondaire à long terme du GS-441524… ou d’un FHS sans rapport ni avec la PIF, ni avec son traitement. Il leur semble, en revanche, peu probable qu’il se soit agi d’une rechute de la PIF, dans la mesure où l’état général des deux chats est resté bon, la RT-PCR FCoV sur sang, négative, et le bilan biologique, normal – mais en sachant que le liquide céphalo-rachidien des deux chats n’a pas pu être analysé, et qu’on n’a donc pu exclure la présence de quelques FCoV qui traîneraient encore par là.
6 – et aussi…
Mentionnons d’abord l’ictère (= jaunisse), présent chez un assez fort pourcentage de chats à PIF, davantage semble-t-il dans les formes humides : on trouve dans la littérature (entre autres !) 4 cas d’ictère sur 32 chats (12,5%) chez Greene & Coll (2023), 10/28 (36%) chez Coggins & Coll (2023), 253/629 (40,2%) chez Ansari Mood (2026), et jusqu’à 38/64 (59,4%) chez Yin & Coll (2021).
Ce ne sont pas les symptômes les plus évocateurs, mais il existe des troubles cutanés dans la PIF, sous forme de nodules qui peuvent démanger… ou pas. On rencontre également des lésions ulcératives de la peau.
On décrit aussi rarement des signes respiratoires évoquant un coryza, associés à des symptômes de PIF plus caractéristiques, ou précédant leur apparition. Des symptômes en rapport avec une myocardite ont également été rapportés.
Terminons par le plus inattendu : des cas de priapisme (= une érection prolongée et sans excuse valable), ont été observés chez des chats atteints de PIF, du fait de la présence de granulomes inflammatoires dans les tissus entourant le pénis.
Le diagnostic
Alors, c’est là que ça se corse. Parce que pour beaucoup de maladies, on a un test, (sérologique, génétique…), et selon qu’il est positif ou négatif, on peut dire qu’on a la maladie ou qu’on ne l’a pas, et voilà. (Bon, ce n’est pas toujours aussi simple, mais en première approximation, on va dire que ça se passe un peu comme ça). Là où c’est quand même particulier pour la PIF, c’est que comme le virus méchant ne diffère du virus gentil que par une toute petite mutation, et que deux virus gentils sont parfois plus différents l’un de l’autre qu’un virus gentil ne l’est d’un virus méchant… il n’est pas facile du tout de distinguer un gentil d’un méchant. (Ce qui, au demeurant, n’est pas valable que pour les virus mais ça, c’est une autre histoire). Ce sera donc le plus souvent en combinant plusieurs éléments (symptômes, signes biologiques, PCR…), que l’on arrivera finalement à un diagnostic de certitude… ou presque.
Dans cet esprit, un certain nombre de tableaux algorithmiques « d’aide au diagnostic », plus ou moins touffus, ont été publiés pour confirmer, autant que faire se peut, une suspicion de PIF. (Ben oui, les algorithmes ne servent pas qu’à inonder de contenu douteux les utilisateurs de TikTok). Un bon exemple, (il y en a d’autres), en suivant ce lien : le principe, c’est qu’on a un symptôme évocateur de PIF, ce qui nous conduit à faire un premier test : s’il est positif, ça renforce la suspicion et on va faire un deuxième test qui va encore renforcer la suspicion… ou pas ; alors que si le premier test est négatif, la PIF devient peu probable mais quand même encore un peu possible et on va donc faire un deuxième test avec l’idée de l’exclure définitivement… mais si ce deuxième test est positif, ça nous ramène la PIF parmi les hypothèses possibles, alors que s’il est négatif, pour le coup, la PIF sera quasiment exclue. Etc etc, jusqu’à arriver, après quatre ou cinq étapes, à la dernière ligne du tableau, qui nous dit : « PIF confirmée », « PIF probable », « PIF improbable », ou « PIF exclue ». Bon, c’est une aide au diagnostic, mais le passage par ce genre d’algorithme n’est pas non plus obligatoire !
1 – Commémoratifs et examen clinique
On va reprendre ici dans les grandes lignes ce qu’on a vu plus haut.
Les commémoratifs nous mettront un peu la puce à l’oreille, mais ne permettront en aucun cas de confirmer ou d’exclure un diagnostic de PIF : par exemple, si l’on voit arriver un chat fiévreux avec un gros ventre, et qu’il s’agit d’un chat de race, de moins de deux ans, sortant d’un élevage et/ou vivant dans une maison avec dix autres chats, et ayant récemment subi un stress, (changement de maison, maladie, castration ou autre intervention…), alors la PIF sera tout en haut de la liste de nos suspicions. Tout en sachant que ce chat peut très bien avoir une tout autre maladie, et qu’à l’inverse, un matou de cinq ans vivant seul dans son jardin, peut très bien attraper la PIF : donc, il n’est question ici que de probabilités.
Concernant les symptômes qui vont orienter vers un diagnostic de PIF, on en a également parlé. Certains ne sont pas spécifiques : abattement, anorexie, amaigrissement, mais aussi une fièvre, surtout si elle est récurrente ou persistante. On se méfiera plus particulièrement de la PIF lorsque cette fièvre sera associée à un gros ventre (avec une masse ou du liquide mis en évidence à la palpation), et/ou à de fortes difficultés respiratoires. Les symptômes oculaires (uvéite…) et neurologiques (ataxie…) décrits plus haut, seront également très évocateurs.
Il sera alors temps de passer aux examens complémentaires, et notamment à l’imagerie.
2 – Imagerie
La radiographie est généralement suffisante pour confirmer une suspicion d’épanchement pleural (= dans le thorax) : on en a vu un exemple un peu plus haut. En revanche, il sera difficile de confirmer, sur une simple radio, la présence d’une ascite, à moins que cette dernière ne soit importante.
Pour progresser dans un diagnostic de PIF, l’échographie est nettement plus intéressante : côté abdomen surtout, elle permettra non seulement de confirmer (ou pas) la présence de liquide, même lorsque celui-ci est en faible quantité. Elle permettra aussi de voir, à travers ce liquide, l’aspect des organes abdominaux, et notamment les modifications dont on a parlé plus haut : hypertrophie des ganglions, déformations de la paroi intestinale, augmentation ou diminution de la taille des reins avec un éventuel anneau médullaire (on en a vu un exemple dans la partie « Symptômes »), modifications de la forme ou de la structure du foie, etc. Elle permettra enfin de réaliser des ponctions : en premier lieu pour aspirer du liquide d’ascite, (quand il y en a beaucoup, à la limite, on pourrait se passer d’échographie, mais quand il y en a peu, l’écho est indispensable), mais aussi pour ponctionner des organes suspects en vue d’analyses.
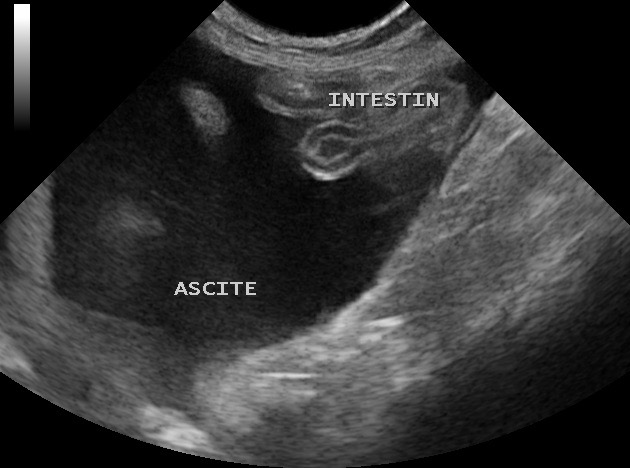
Echographie abdominale chez un chat Sacré de Birmanie âgé de 3 ans avec une ascite importante. Sur les images d’échographie, l’ascite se présente sous forme de plages noires ou gris foncé. Sur la photo de gauche : très importante quantité de liquide avec un petit segment d’intestin qui flotte dans un coin. A droite : une grosse rate d’aspect « mité » flottant dans le liquide. Ce liquide d’ascite, prélevé par ponction, est visible deux paragraphes plus loin (« Caractéristiques des épanchements »).
Côté thorax, on l’a vu, la radio permet de visualiser l’épanchement dans la plupart des cas. (A noter tout de même que chez un chat en grande difficulté respiratoire, le simple fait de le coucher sur le côté pour la prise de radiographies peut être très dangereux, alors que l’échographie, qui se pratique sur le chat debout ou assis, n’augmente pas le risque de décompensation respiratoire). L’échographie présente plusieurs autres avantages sur la radiographie : d’abord, comme côté abdomen, elle permet de voir des quantités de liquide minimes, que ne détecterait pas la radio. (C’est quand même beaucoup moins vrai pour le thorax que pour l’abdomen, la radio étant beaucoup plus sensible pour détecter un épanchement dans le thorax). L’échographie permet aussi de visualiser la présence d’un épanchement à l’intérieur du péricarde, c’est à dire entre le cœur et ses enveloppes. Enfin et surtout, lorsque l’épanchement est important, l’échographie permet de voir ce qui se passe à l’intérieur, contrairement à la radio. Certaines images seront compatibles avec la PIF (par exemple un liquide d’épanchement de densité épaisse et modérément hétérogène), alors que d’autres permettront de partir dans une autre direction dès les premières secondes de l’examen : si le cœur est très déformé avec un atrium gauche qui a quintuplé de volume… finie la PIF, on est sur une insuffisance cardiaque et on commencera tout de suite le traitement de cette dernière. Si on a des masses partout, on est sur un processus tumoral. L’échographie permettra aussi de ponctionner le liquide pour analyse, et éventuellement d’en aspirer pour soulager le chat, si ce dernier éprouve des difficultés pour respirer. Là aussi, l’aspect du liquide nous fournira en quelques secondes des informations intéressantes : si le liquide d’épanchement est jaune et visqueux, ce sera un élément de plus en faveur de la PIF : on en reparle plus loin. S’il s’agit d’un pus épais, granuleux et nauséabond… alors on partira sur une origine bactérienne, et bye bye la PIF.
Un mot sur l’IRM qui, en cas de symptômes neurologiques, pourra permettre de mettre en évidence (entre autres), une hydrocéphalie, une syringomyélie ou une hernie à travers le foramen magnum… mais une IRM (sous anesthésie) n’est peut-être pas le premier examen sur lequel on va se précipitera en voyant arriver un chat suspect de PIF !
3 – Hématologie et biochimie
L’hématologie ne nous apprend pas grand chose : on a le plus souvent une augmentation des globules blancs, avec des polynucléaires neutrophiles augmentés, et des lymphocytes diminués. Une anémie est présente dans 65% des cas : il s’agit le plus souvent d’une anémie non régénérative (due à l’inflammation chronique), mais elle peut être régénérative en cas d’hémolyse (= destruction des globules rouges) à médiation immune associée. Il peut y avoir thrombopénie (= baisse des plaquettes sanguines), notamment en cas de coagulation intra-vasculaire disséminée. Bref, une augmentation des globules blancs et une baisse des globules rouges, ce qu’on trouve dans la plupart des inflammations ou infections : on n’est pas plus avancés.
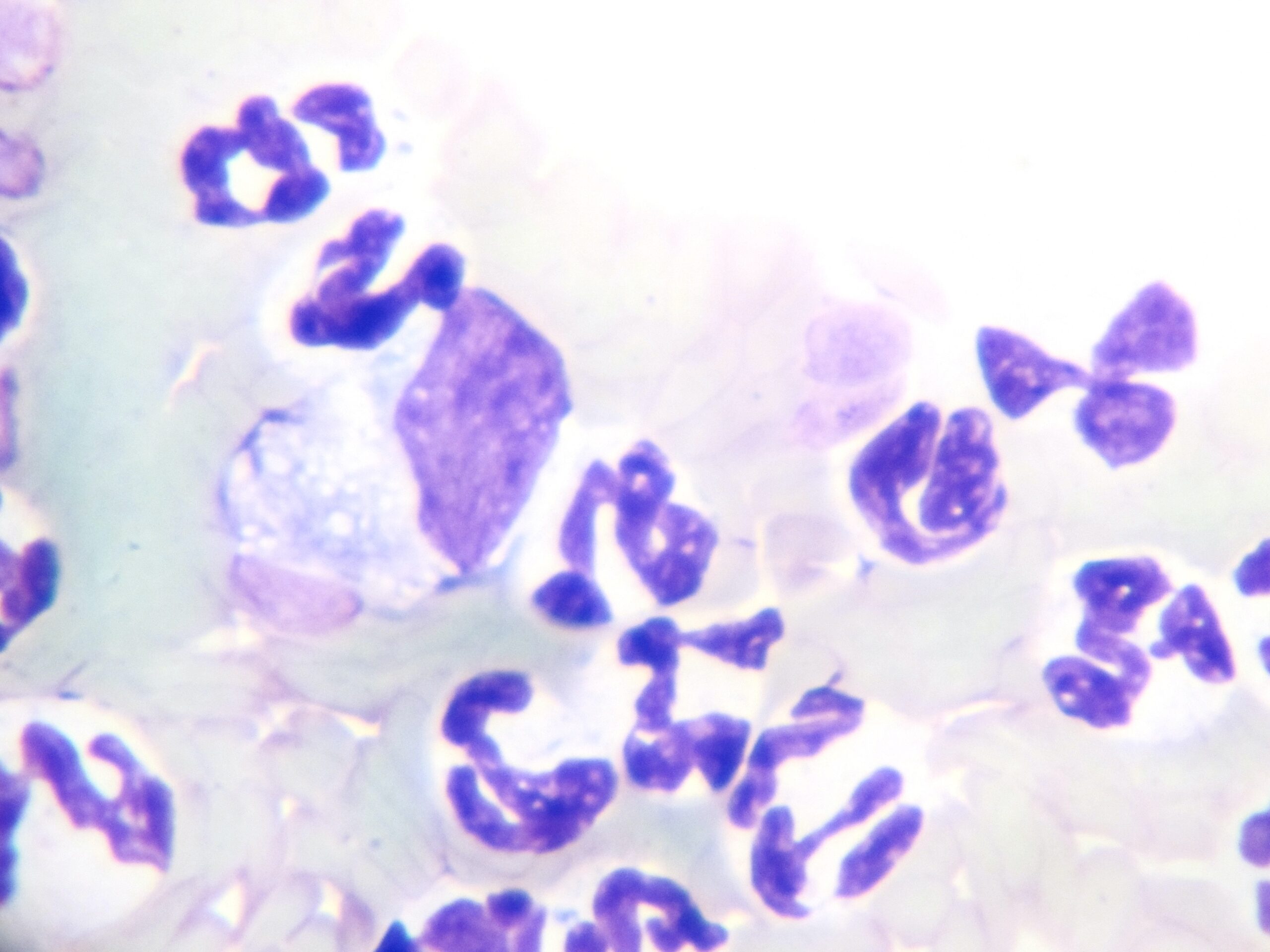
Aspect du frottis sanguin chez le chat Sacré de Birmanie dont nous venons de voir les images d’échographie : très nombreux polynucléaires neutrophiles au noyau hypersegmenté (à gauche), avec en plus un monocyte activé (à droite). Ce frottis constitue un petit élément en faveur d’une PIF, mais on trouverait le même genre d’image en cas de pleurésie, d’infection utérine, etc : il est donc urgent de creuser davantage !
Côté biochimie, maintenant : parmi les chats atteints de PIF, 50% des chats à épanchement et 70% des chats sans épanchement ont un taux de protéines augmenté, qui peut atteindre des valeurs aussi élevées que 120 g/l. (Les valeurs usuelles varient entre 60 et 80 g/l). Avec une protidémie aussi élevée, la probabilité d’une PIF est de 90% (les 10% restants se répartissant pour l’essentiel entre une stomatite chronique sévère, une infection respiratoire chronique, une dirofilariose ou un myélome).
Parmi ces protéines, l’albumine est souvent diminuée, alors que les globulines sont augmentées. (Une fraction de ces dernières, (les gamma globulines), augmentant d’ailleurs parallèlement au taux d’anticorps anti FCoV). On peut donc s’attendre à trouver un rapport Alb/Glob diminué chez les chats à PIF, et diverses études se sont attachées à établir une relation entre l’importance de cette diminution et la probabilité pour le chat d’avoir une PIF : plusieurs articles concluent qu’avec un rapport Alb/Glob < 0,4, la PIF est très probable, tandis qu’elle l’est très peu avec un rapport > 0,8. Attention, au passage, à ne pas s’arrêter au seul taux de protéines totales, parce que si on a des globulines qui grimpent et une albumine qui baisse, la somme des deux risque d’être normale ! (Hartmann & Coll, 2003 ; Tsai & Coll, 2011 ; Green & Coll, 2023).
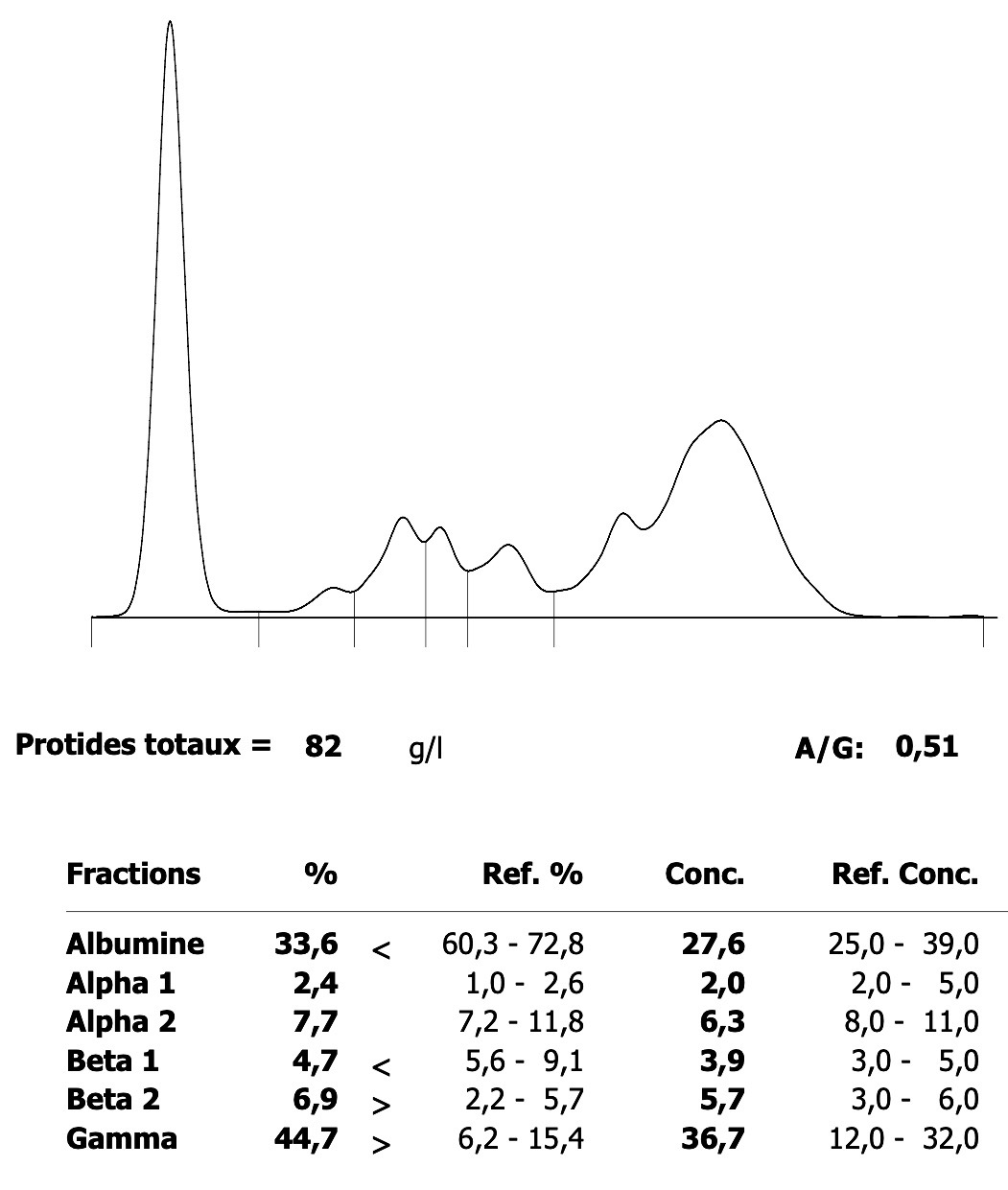
Ci-dessus à droite : on en trouve des plus typiques, mais cette électrophorèse n’est déjà pas si mal, avec des taux de protéines et de gammaglobulines augmentés, un taux d’albumine à la limite inférieure des valeurs de référence, et un rapport A/G diminué à 0,5. Le sérum était ictérique (voir ci-dessous). En plus d’avoir la PIF, ce chat de 11 ans était porteur d’Hepatozoon felis, et de la petite forme d’hémoplasmes (Mycoplasma haemominutum).
Pour les fans d’électrophorèses, les gammaglobulines augmentées se présentent le plus souvent sous la forme d’un « bloc » polyclonal, mais une gammapathie monoclonale est également possible (Taylor & Coll, 2010) : la présence d’une bande étroite en gamma n’est donc pas synonyme de myélome, on en trouve aussi, quoique plus rarement, dans la PIF ou, par exemple, dans l’ehrlichiose ou la leishmaniose chez le chien. Voilà, ça, c’était vraiment pour les fans.
La bilirubine est un pigment de couleur jaune présent dans la bile, et en faible quantité dans le sang. (Quand elle augmente dans le sang, ça nous donne logiquement un ictère = une jaunisse). En très très schématique, quand un globule rouge est détruit, il libère son hémoglobine. Celle-ci est dégradée en bilirubine non conjuguée (= bilirubine libre), qui est transportée jusqu’au foie où elle sera transformée en bilirubine conjuguée, avant d’être excrétée dans l’intestin grêle, via la bile. Elle augmente donc en cas de destruction d’un nombre important de globules rouges, (qui libèrent tout plein d’hémoglobine), et de problème de foie. Il se trouve que la bilirubine est fréquemment augmentée dans la PIF (chez 22 à 84% des chats infectés ; ok, la fourchette est large), plus particulièrement dans les formes humides. La suspicion de PIF sera particulièrement forte si la bilirubine est élevée alors que les enzymes hépatiques, (ALAT et PAL notamment), sont normales – et ça tombe bien, parce que ces deux enzyme ont des valeurs normales chez, respectivement, 86% et 95% des chats à PIF (Riemer & Coll, 2016). Le taux de bilirubine a aussi une valeur pronostique : selon une étude chez des chats atteints de forme humide ou mixte et recevant un des traitements antiviraux dont nous parlerons plus loin, les taux de bilirubine chez les chats qui ont survécu à la PIF étaient significativement inférieurs à ceux des chats qui ne s’en sont pas sortis (Katayama & Coll, 2023).
D’utilisation plus récente, l’AGP (alpha-1-glycoprotéine acide), dosée sur sérum ou sur épanchement, est une « protéine de la phase aiguë », ou PPA, qui augmente, comme son nom l’indique, en cas d’inflammation aiguë. Mais alors, nous direz-vous, n’importe quel accident ou infection peut être à l’origine d’une inflammation aiguë, donc d’une augmentation des PPA en général, et de l’AGP en particulier ! Certes, mais une augmentation moyenne de l’AGP chez des chats présentant des symptômes évocateurs et, plus intéressant encore, une augmentation marquée chez des chats présentant des symptômes peu spécifiques, voire des symptômes totalement atypiques, sont très en faveur d’une PIF – et plus encore si le dosage a été fait sur épanchement. A l’inverse, la PIF est peu probable lorsque l’AGP est basse (Giori & Coll, 2011 ; Hazuchova & Coll, 2017). Autre PPA utilisée pour le diagnostic de la PIF, la SAA (Serum Amyloid A), mais il semble qu’actuellement, ce soit l’AGP qui ait le vent en poupe.
En conclusion, tout cela ne nous donne toujours pas un diagnostic définitif, mais il est certain que si on a un chat avec un épanchement qui présente des gamma-globulines, une bilirubine et une AGP augmentées, ça commencera à sentir très très mauvais…
4 – Caractéristiques des épanchements
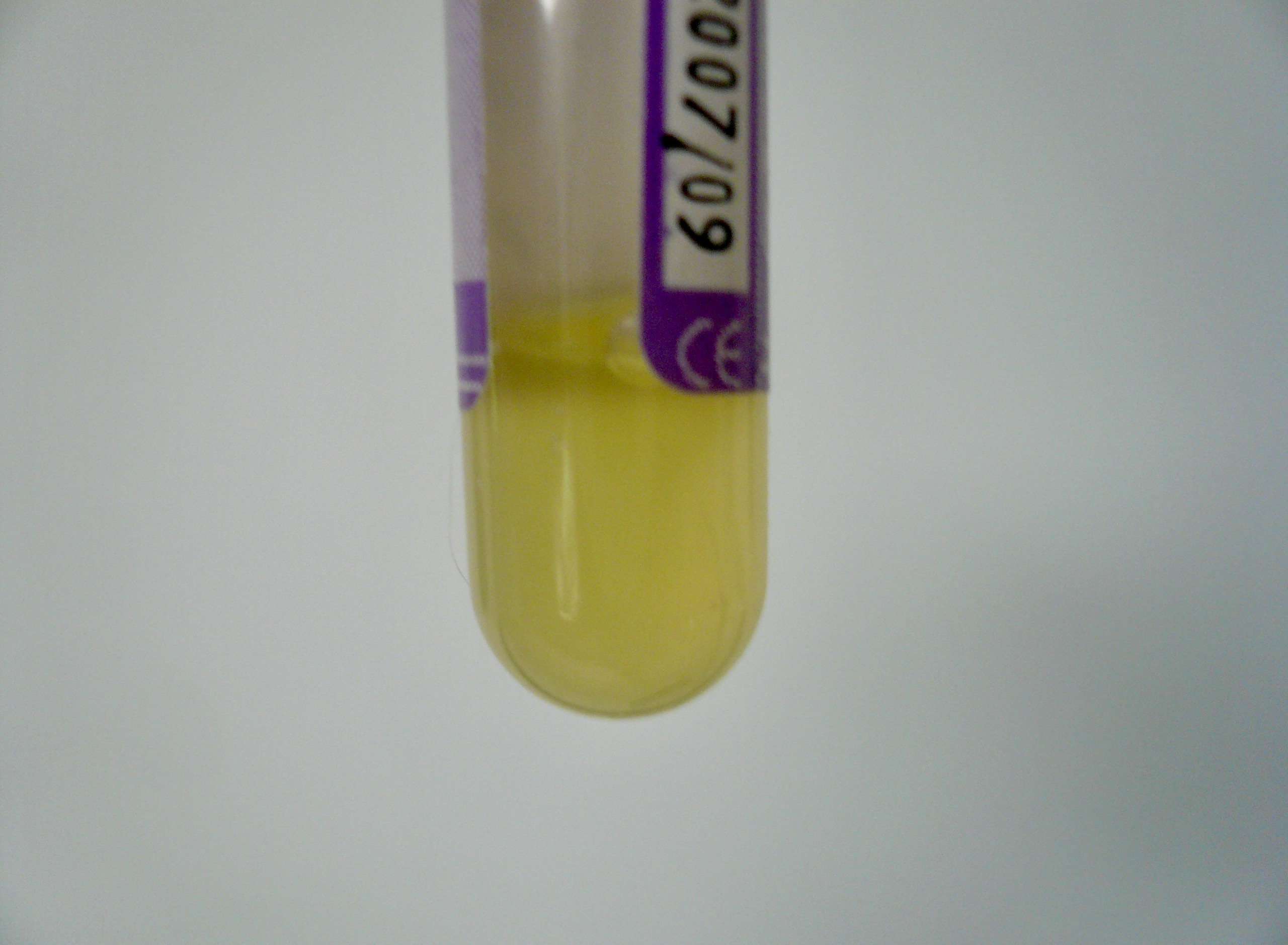
Déjà, à l’œil nu : l’épanchement de la PIF, (qu’il soit dans l’abdomen ou dans la plèvre), se présente classiquement sous la forme d’un liquide « jaune paille », épais et filant (photo ci-dessous). Il s’agit d’un transsudat modifié avec un taux de protéines supérieur à 35 g/l (on peut monter à 99 g/l) et une cellularité de moins de 5000 globules blancs/µl. Si l’épanchement est hémorragique, purulent, nauséabond ou chyleux (= graisseux et lactescent), la PIF est peu probable (bien que des chyles purs aient été décrits chez des chats à PIF).

Liquide d’ascite typique, prélevé chez le chat dont nous avons vu les deux images d’échographie un peu plus haut, au paragraphe « Imagerie » : la couleur est bien jaune, et l’aspect épais et filant nettement visible à gauche de l’image, avec ce liquide qui « colle » au piston de la seringue. Le taux de protéines (60 g/l) et la densité (1042) du liquide étaient tous deux très augmentés. La charge de coronavirus détectée dans ce liquide par RT-PCR était élevée, et fortement compatible avec une PIF.
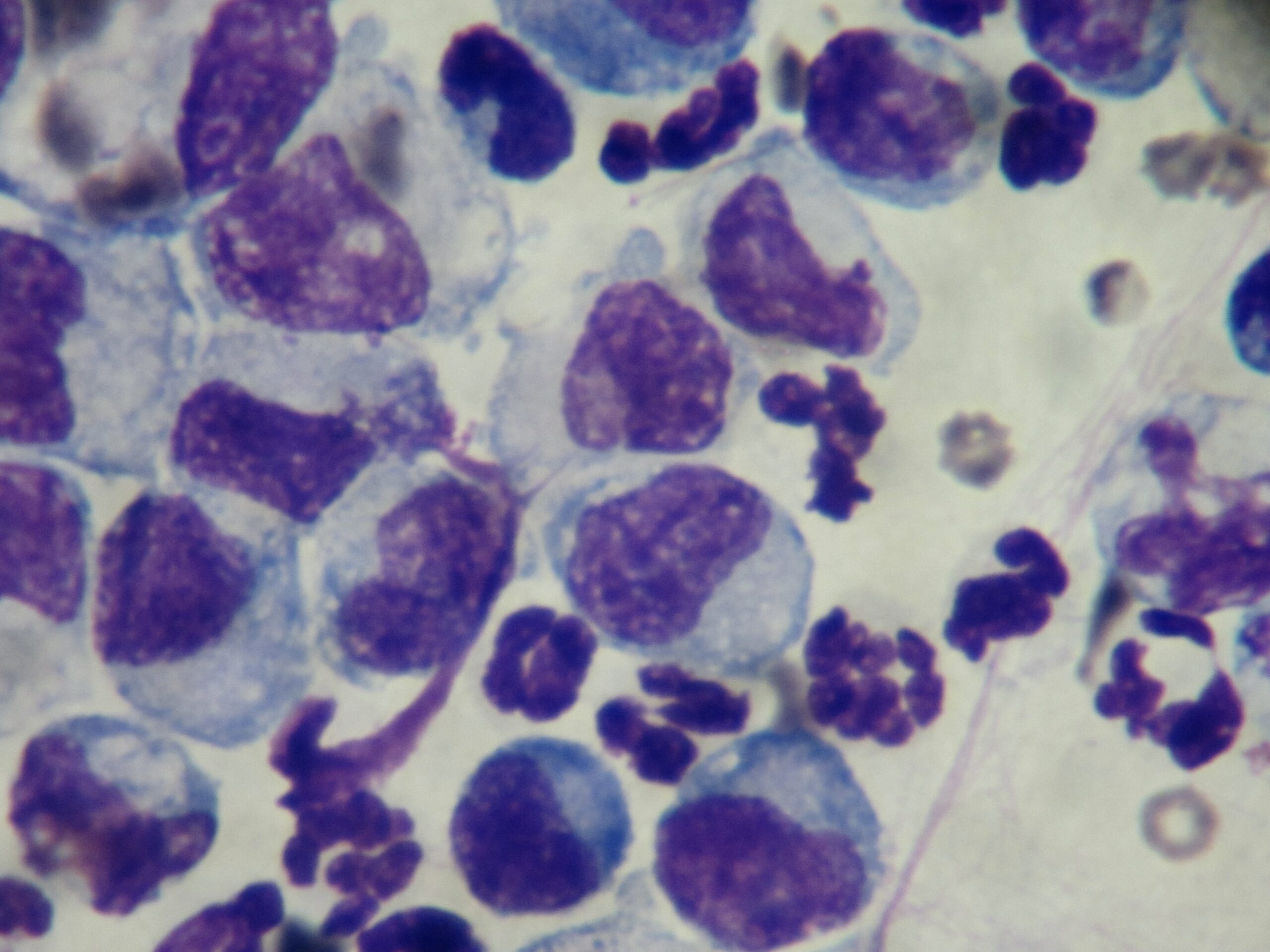
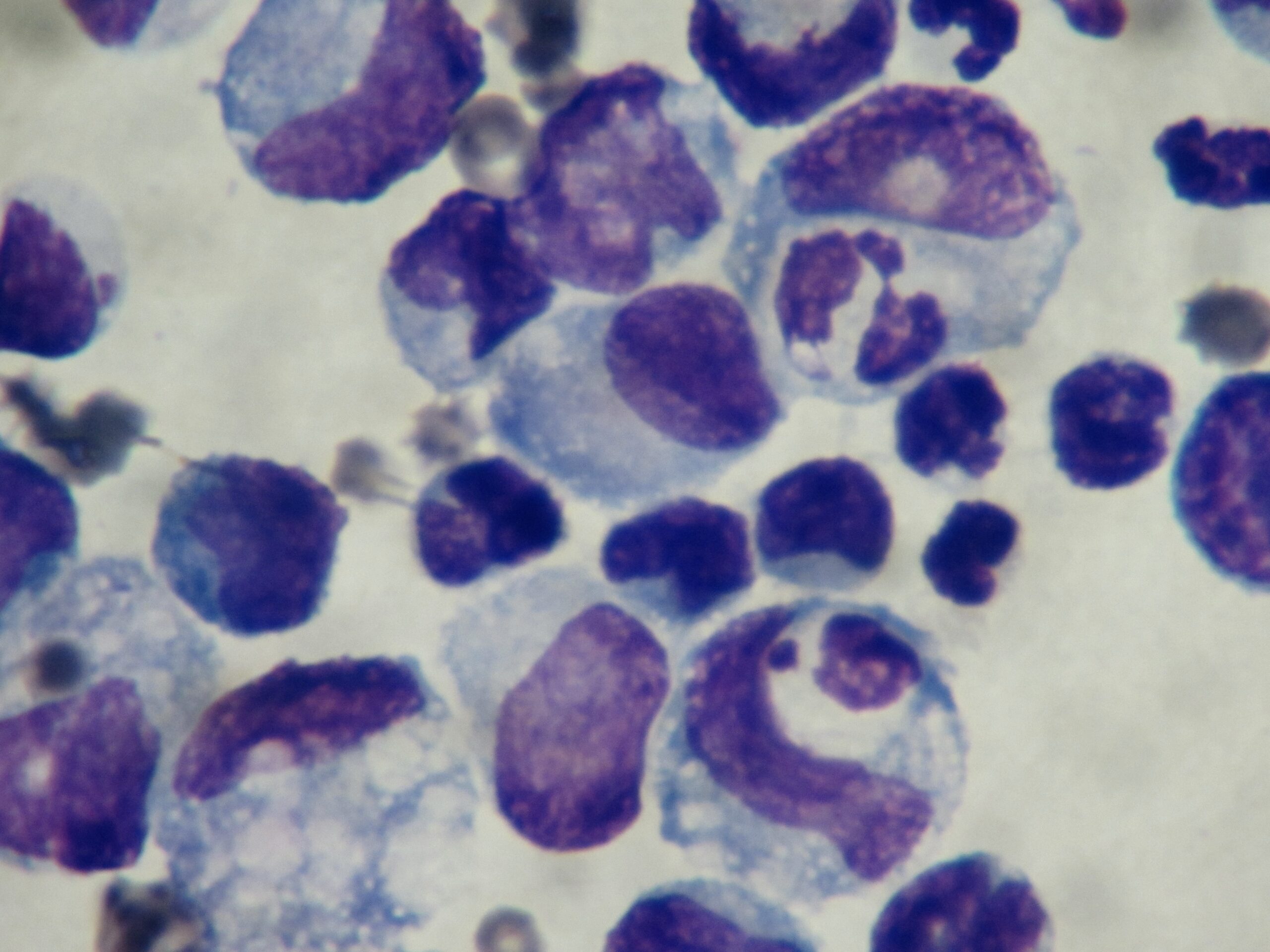
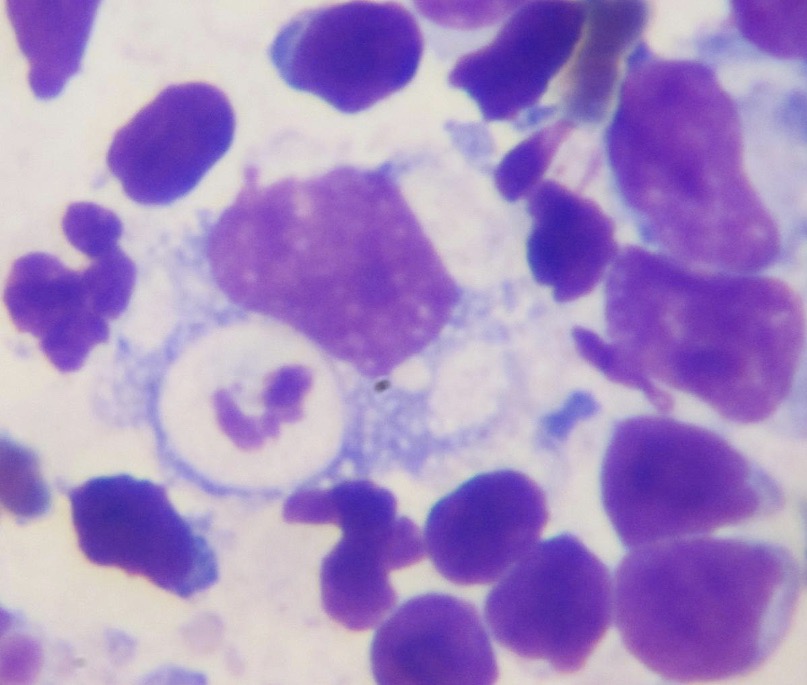
L’examen cytologique du liquide d’épanchement montre des macrophages et des polynucléaires neutrophiles (épanchement pyogranulomateux). Si on y trouve des bactérie phagocytées, de grandes quantités de lymphocytes, ou des cellules tumorales, alors la PIF devient improbable (photos ci-dessous).
Les tests réalisés sur épanchement ont une meilleure valeur diagnostique que les mêmes tests réalisés sur plasma (cf paragraphe précédent : Hématologie et biochimie) : notamment la valeur prédictive du rapport Alb/Glob (< 0,4 vs > 0,8), et le dosage de l’AGP. On parlera de la PCR un peu plus loin.
5 – Cytologie et histologie
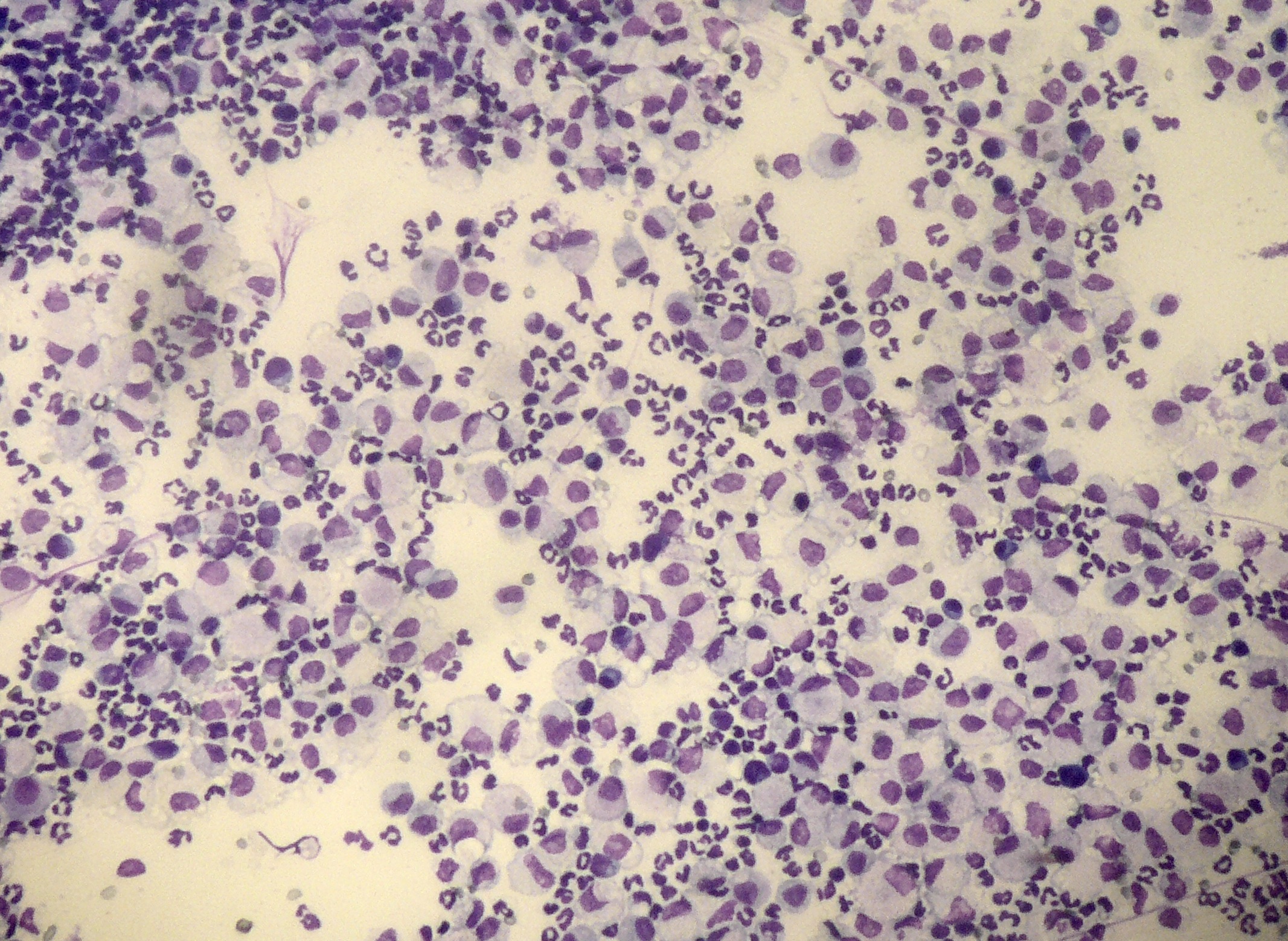
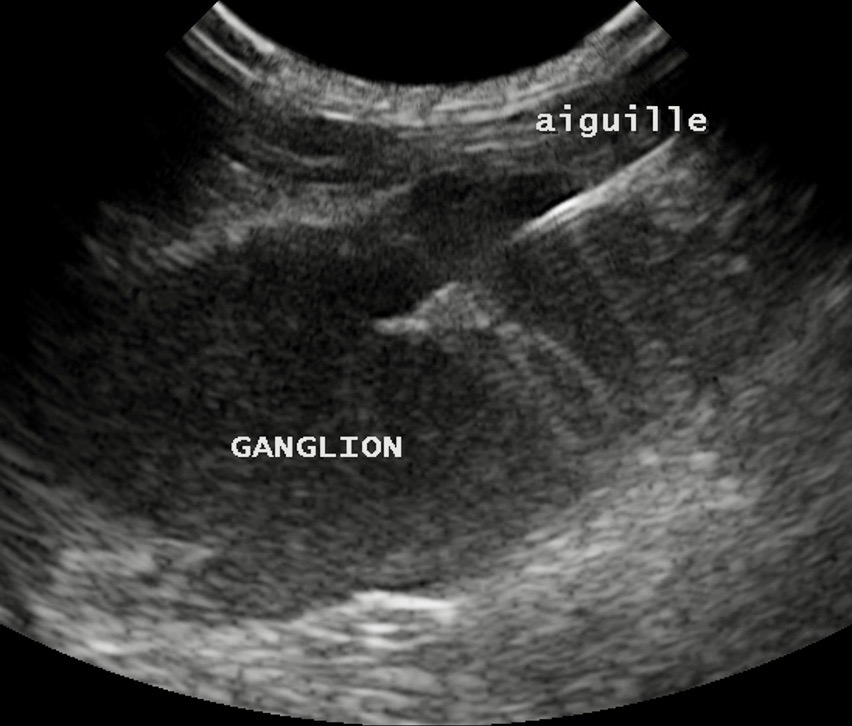
L’examen cytologique présente l’avantage de la simplicité (une ponction à l’aiguille, et un examen au microscope dans la foulée, après étalement et coloration), mais ne donne pas un diagnostic de certitude. Il permet malgré tout de se rendre compte si les cellules collectées sont compatibles avec l’hypothèse de PIF (réaction pyogranulomateuse au milieu des cellules normales de l’organe ponctionné), et d’éliminer d’autres hypothèses (par exemple, un lymphome… surtout si c’est un gros ganglion que l’on a ponctionné). Les publications semblent montrer que ça marche bien pour les cytoponctions de ganglions, (Green, 2023), un peu moins bien pour les cytoponctions de foie, et encore moins pour celles de rate.
Photo de gauche : ponction du très gros ganglion mésentérique présenté plus haut : l’aiguille, en place dans le ganglion pour le prélèvement, est bien visible. Photo de droite : examen microscopique de ce prélèvement, après étalement et coloration : la population cellulaire est variée, ce qui exlut un envahissement tumoral (en particulier un lymphome). Au milieu des cellules ganglionnaires, on observe des polynucléaires neutrophiles et des macrophages, (celui au centre de la photo a avalé un PNN), compatibles notamment avec une PIF. Une PCR réalisée sur le même prélèvement a confirmé le diagnostic de PIF, avec une très forte charge en coronavirus.
Le diagnostic histologique est un peu moins facile à réaliser, puisqu’il s’agit cette fois d’aller prélever un fragment d’organe (foie, reins…), et non plus seulement quelques cellules, comme dans une simple ponction à l’aiguille. Cela peut se faire à l’aide d’un trocart, (c’est un peu plus gros qu’une aiguille, mais le mode de prélèvement reste grosso modo le même), d’une chirurgie (bon, on ouvre rarement le ventre d’un chat suspect de PIF ; ce serait plutôt à l’occasion d’une laparotomie parce qu’on suspectait autre chose, et on tombe sur des lésions bizarres qu’on prélève), ou malheureusement, d’une autopsie. À défaut d’être d’accès facile, l’histologie est parfois considérée comme le meilleur outil de diagnostic pour la PIF : Les inflammations localisées autour des vaisseaux, avec macrophages, polynucléaires neutrophiles, lymphocytes, et plasmocytes, ainsi que les pyogranulomes, sont en effet typiques de la maladie. En cas de doute, la PCR ou l’immunofluorescence réalisées sur les tissus prélevés, confirmeront la PIF – on en parle, pas au paragraphe suivant, mais à celui d’après.
6 – Sérologie
Levons tout de suite une confusion : on nous présente parfois des chats « (séro)positifs pour la PIF », ou ayant « une sérologie PIF positive » : ce n’est pas de PIF qu’il est question chez ces chats, mais de coronavirus, sachant que le test est positif aussi bien pour le « méchant » coronavirus de la PIF, que pour le « gentil » coronavirus intestinal. La séroconversion (= le moment où le test se positive), se produit généralement entre 7 et 28 jours après l’infection. 90% des chats de chatterie et 50% des chats de maison ont eu un jour un « banal » Coronavirus dans l’intestin : tous ces chats ont, à un moment donné, été positifs pour le coronavirus, (et pas pour la PIF !), mais la plupart de ces chats sont en parfaite santé, et ne feront jamais une PIF.
Un test positif ne signe donc pas une PIF, même si des titres très élevés sont tout de même plutôt en faveur d’une PIF : si le plus haut titre du laboratoire est atteint, la probabilité de la PIF est de 94%. Cette probabilité est encore plus forte s’il s’agit d’un chat de maison, plutôt que d’un chat de chatterie, où les taux élevés sont courants et n’ont pas une forte valeur prédictive.
On pourrait se dire qu’au moins, si la sérologie est négative, ça veut dire que le chat n’est pas infecté par quelque FCoV que ce soit, et qu’il ne peut donc pas avoir la PIF. Ben non, même pas ! 10% des chats avec une PIF clinique (notamment en phase terminale), sont séronégatifs. Les chats à épanchement ont souvent peu ou pas d’anticorps car ceux-ci sont dilués dans l’épanchement, ainsi que la plus grande partie des protéines. On considérait classiquement, en revanche, que si un chat sans épanchement était séronégatif, on pouvait pratiquement exclure la PIF… et patatras, voilà qu’une publication décrivant les cas de 7 chats atteints d’une forme neurologique de PIF, sans épanchement, indique que 3 d’entre eux étaient séronégatifs pour le FCoV.
Un mot sur les tests rapides réalisables en clinique, qui ne donnent pas un taux, mais seulement un résultat positif ou négatif : ils sont inutiles, (nous venons de mentionner l’intérêt de savoir si le titre est élevé), et ils donnent en outre de nombreux faux positifs et faux négatifs.
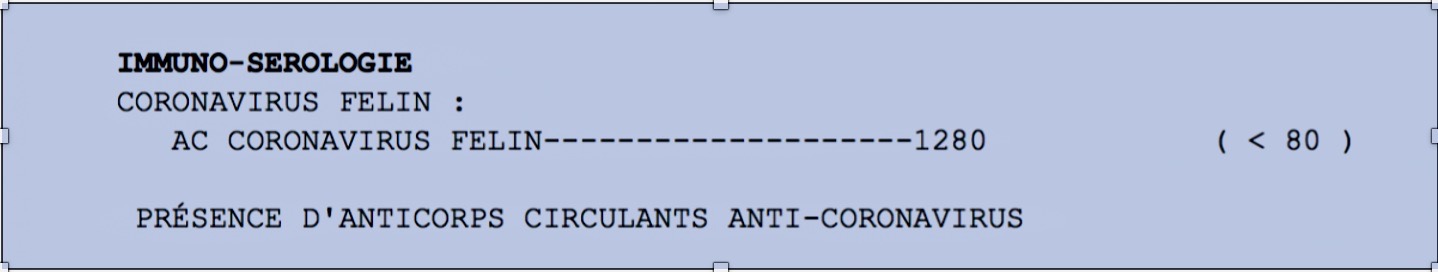
Alors, la sérologie coronavirus est-elle totalement inutiles ? allez, pas tout à fait :
– Un chat sain, qui ne présente pas du tout du tout de symptôme, et qui est séronégatif, est indemne de coronavirus : il n’est donc pas contagieux, ce qui est toujours bon à savoir dans une collectivité ; et comme il n’héberge pas de coronavirus, il ne peut pas faire une PIF.
– Chez un chat qui n’héberge que le FCoV intestinal, le taux d’anticorps est directement corrélé à la quantité de coronavirus présent dans les intestins et excrété dans les selles, et également corrélé à la replication du virus.
Le test est donc intéressant pour créer une chatterie indemne de FCoV, ou avant l’introduction d’un nouveau chat dans une telle chatterie.
Notons que le dosage des anticorps sur un épanchement ou sur du liquide céphalo-rachidien, ne semble pas beaucoup plus intéressant que sur sérum.
7 – Mise en évidence directe du virus : immunomarquages et PCR
Alors, jusque-là, on n’a cherché à savoir si notre chat avait la PIF qu’en utilisant des voies détournées : est-ce que c’est un jeune chat de race qui vit en collectivité ? est-ce qu’il a un épanchement, une uvéite ou une ataxie ? est-ce que ses gammaglobulines sont très augmentées, ainsi que, tant qu’à faire, ses AGP ? Il est certain que quand plusieurs de ces éléments sont présents, (plus une fièvre, plus un état général qui se dégrade…), le risque d’avoir une PIF est élevé… mais on n’en reste pas moins sur des signes indirects. Pour arriver à un diagnostic de (quasi)-certitude, le must sera d’arriver à mettre en évidence le virus dans l’organisme du chat suspect. En sachant que même là, on va retomber sur la difficulté que constitue la proximité entre gentil FCoV intestinal, et méchant virus de la PIF. La mise en évidence du virus dans le chat pourra se faire de deux façons : par immunomarquage au sein même d’une lésion, ou par PCR sur sérum, épanchement, liquide céphalo-rachidien (LCR), ou encore humeur aqueuse.
Les immunomarquages
Le principe des immunomarquages, c’est qu’on va utiliser des anticorps, (des molécules qui défendent l’organisme, on en a parlé dans la partie « Pathogénie »), qui vont aller se fixer sur des antigènes, en l’occurrence les cellules de l’organisme du chat modifiées par la présence du FCoV à l’intérieur. Et le complexe antigène-anticorps ainsi formé sera visualisé par un marquage fluo (on simplifie un peu). Alors, vous nous direz : oui, mais qu’est-ce qui nous dit que le marquage touche vraiment des cellules infectées par le virus de la PIF, et pas par le gentil virus intestinal, pour une fois en excursion loin de chez lui ? Eh bien, et c’est ce qui fait la beauté de la chose, parce que la présence du virus est ici recherchée au sein même de lésions caractéristiques, à savoir les lésions pyogranulomateuses déjà évoquées plus haut (Stranieri & Coll, 2020).
Le top du top, c’est de faire ça sur une biopsie, c’est à dire un morceau de tissu qu’on sera allé chercher au cœur d’une lésion, (dans le foie, la rate, un ganglion mésentérique…), le plus souvent sous contrôle échographique avec un pistolet à biopsie, ou éventuellement par chirurgie. (Dans le pire des cas à l’occasion d’une autopsie, si l’on veut confirmer rétrospectivement une suspicion de PIF). Donc déjà, on vérifie qu’on ait bien des lésions pyogranulomateuses : ce n’est pas spécifique, on l’a vu, ces lésions se rencontrent aussi dans la toxoplasmose, des mycoses profondes, des infections à Pseudomonas ou à mycobactéries… mais déjà, on sait qu’il ne s’agit pas, par exemple, d’une lésion cancéreuse. Après, on fait notre immunomarquage, (pour une biopsie, on parle d’immunohistochimie (IHC)) et si c’est positif, alors là, bingo, on a les lésions caractéristiques et le FCoV à l’intérieur, ce qui nous donne (enfin) un diagnostic de certitude !
On peut parfois hésiter à aller faire une biopsie sur un chat en mauvais état, et on préfèrera alors se contenter de cellules obtenues par cytoponctions (= ponctions à l’aiguille fine), dans un organe présentant des lésions évocatrices de PIF, lésions préalablement repérées à l’échographie. On peut aussi utiliser un liquide d’épanchement : on a vu tout cela plus haut. Evidemment, on n’obtient ainsi que des étalements de cellules, et pas de belles lésions à la structure bien conservée ; mais on n’a pas toujours ce qu’on veut dans la vie, et l’étude des cellules, même en vrac, nous permet tout de même de savoir si nous sommes bien en présence de lésions pyogranulomateuses et pas, comme on l’a dit précédemment, de cellules cancéreuses, auquel cas, on oublie la PIF. Et donc, si le caractère pyogranulomateux est bien confirmé, on fait notre immunomarquage, (ici, on parle d’immunocytochimie (ICC) ou d’immunofluorescence (IF)), et si c’est positif, même chose que pour les biopsies : on a les cellules caractéristiques et le FCoV au milieu, ce qui nous donne… presque un diagnostic de certitude – mais pas loin. Alors, pourquoi presque ? Parce que si c’est positif, on a notre diagnostic de PIF, mais si c’est négatif, il peut tout de même s’agir d’une PIF, mais avec peu de virus dans le prélèvement, parce que quoi qu’on fasse, il y aura toujours moins de cellules infectées dans un épanchement que dans un bon gros morceau de tissu prélevé au cœur d’une lésion.
xxxx
La PCR
- Chercher le virus
On n'a pas toujours tout ce qu'il faut sous la main pour réaliser une immunohisto/cytochimie : une alternative plus fréquente est constituée par la RT-PCR (Sigle pouvant signifier aussi bien Real Time - Polymerase Chain Reaction, que Reverse Transcriptase - Polymerase Chain Reaction). En langage intelligible, la PCR, ou "réaction de polymérisation en chaîne", consiste à dupliquer/amplifier un petit fragment d'ADN de façon exponentielle, jusqu'à en obtenir une quantité suffisamment importante pour le rendre détectable, mesurer sa charge initiale, etc. Et comme la PCR se fait sur ADN et que le FCoV est un virus à ARN, on commence par convertir cet ARN en ADN (dans la nature, c'est dans l'autre sens que ça se passe, l'ADN est transcrit en ARN, donc ici, on fait une transcription inverse/reverse, d'où le préfixe RT), et une fois qu'on a l'ADN, on réalise la PCR classique. Concernant la Real Time PCR, ou PCR en temps réel, ses principaux avantages, par rapport à une PCR conventionnelle, sont une mesure de la charge virale, (analyse quantitative), et de bien meilleures sensibilité et reproductibilité. Les laboratoires auxquels nous adressons nos prélèvements utilisent la PCR en temps réel (voir les exemples de résultats ci-dessous).
Donc, grâce à la RT-PCR, on va pouvoir détecter la présence du FCoV dans le sang, dans un liquide d'épanchement, (deux types de prélèvements faciles à réaliser, même sur un chat en mauvais état), mais aussi dans du liquide céphalo-rachidien en cas de symptômes neurologiques, ou dans l'humeur aqueuse en cas d'atteinte oculaire… et dans tous les cas, de connaître la charge virale. Après, toujours du fait de la proximité génétique du virus gentil et du virus méchant, trouver du FCoV dans le sang ou dans un épanchement ne signifie pas forcément que le chat a la PIF (même si le virus intestinal a moins tendance à circuler que le virus de la PIF). On ne se contentera donc pas de savoir qu'il y a du FCoV dans le sang ou le liquide d'épanchement d'un chat suspect, il faudra aussi réaliser une analyse quantitative pour connaître la charge virale : en effet, la charge virale d'un chat porteur du seul FCoV intestinal, sera plus faible que celle que l'on trouve chez un chat atteint de PIF. Sachant que comme précédemment, un résultat négatif n'exclura pas totalement la possibilité que le chat ait quand même la PIF ! Cela peut se produire s'il y a peu de virus chez ce chat, ou si le virus est inégalement réparti de sorte qu'il n'y en ait pas, (ou seulement très peu), pile dans le fluide qu'on a prélevé. Globalement, la PCR réalisée sur un épanchement sera positive chez, (selon les études), 72 à 100% des chats à PIF, et généralement négative chez les chats indemnes de PIF. Une PCR très positive sur un épanchement ayant des caractéristiques biochimiques et cytologiques évocatrices sera évidemment très très en faveur d'une PIF (Coggins & Coll, 2023).
Outre les fluides, il est également intéressant de réaliser une RT-PCR sur un prélèvement obtenu par cytoponction (aspiration dans un ganglion mésentérique, par exemple). En revanche, rechercher du FCoV par RT-PCR dans les selles ne présente vraiment aucun intérêt, puisque plein de chats qui vont très bien ont du FCoV non muté dans l'intestin ; le seul intérêt éventuel serait de déterminer lesquels, parmi les 15 chats en bonne santé qui squattent ma chambre et mon salon, excrètent du coronavirus intestinal, (sachant, on l'a vu, que l'excrétion peut être intermittente !), afin de savoir où j'en suis, et comment gérer la situation. Bof… On en reparle plus loin, dans la partie "Prévention". En tout cas, définitivement aucun intérêt pour le diagnostic de la PIF.

Résultat d'une RT-PCR réalisée sur le sang d'un chat suspect de PIF : il y a certes du coronavirus, mais en quantité inférieure au seuil de quantification… donc c'est quand même bof bof, il faudrait vraiment avoir des symptômes et des signes biologiques très évocateurs à côté pour conclure à la PIF.

Là, c'est déjà mieux ; (enfin, pour le diagnostic, malheureusement pas pour le minou). Avec cette forte charge virale dans l'épanchement abdominal d'un chat qui présentait des symptômes très évocateurs, le diagnostic de PIF devient hautement probable.

Et là, c'est le résultat du chaton que nous avons vu plus haut, avec son ventre très gonflé par un épanchement présentant toutes les caractéristiques des épanchements dus à la PIF. Si l'on y ajoute cette RT-PCR positive avec une "charge virale de Coronavirus félin détectée fortement compatible avec une Péritonite Infectieuse Féline", on peut dire que pour le coup, on a là un diagnostic de certitude.
- Chercher les mutations
On n'a parlé presque que de ça depuis le début de cet article : le gentil FCoV intestinal et le méchant virus de la PIF se ressemblent (presque) comme deux gouttes d'eau et du coup, pas facile de les distinguer ; ce serait donc vraiment bien d'arriver à trouver un test qui permette de les différencier ! On l'a vu tout au début de cet article, les gènes codant pour la protéine de surface (S), (qui permet notamment au virus de pénétrer dans une cellule), semblent jouer un rôle particulièrement important dans la bascule du FCoV intestinal vers le virus de la PIF. Plusieurs techniques ont donc été développées pour détecter les mutations sur le gène S, la plus fréquemment disponible en laboratoire d'analyses (le test de discrimination allélique) permettant de mettre en évidence deux mutations concernant chacune un seul nucléotide (= un composant de base de l'ADN ou de l'ARN), mutations portant les doux noms de M1058L et S1060A. Bon, tout cela est bien séduisant, mais plusieurs problèmes se posent malgré tout : entre autres, on sait qu'une seule, voire quelques mutations, ne suffisent pas à transformer un FCoV intestinal en virus de la PIF, mais que de nombreuses mutations sont probablement nécessaires : un diagnostic de PIF ne peut donc reposer sur la mise en évidence d'une seule mutation. On sait aussi que d'autres mutations, ainsi que des facteurs liés à l'hôte (le chat), permettent visiblement l'entrée et la replication du FCoV à l'intérieur des monocytes. La sensibilité du test varie aussi beaucoup selon la méthode utilisée (de 40 à 95% !) : c'est ainsi que dans une étude portant sur 34 chats atteints de PIF, le test de discrimination allélique n'a permis de détecter l'une des deux mutations mentionnées ci-dessus que chez 24 chats (sensibilité = 71%)(L Sangl & Coll, 2019). Il n'est, en outre, pas exclu qu'un virus muté soit présent chez un chat non atteint de PIF, dans la mesure où la mutation M1058L pourrait n'être responsable que de la dissémination dans l'organisme d'un innocent FCoV intestinal, et pas forcément d'une PIF… etc. Du coup, sans surprise, la compilation des résultats d'un grand nombre d'études a montré qu'il était très difficile de s'appuyer sur une seule mutation du gène codant pour la protéine S pour confirmer un diagnostic de PIF (S. Tasker & Coll, 2023-2025). La recherche de ce type de mutation présente malgré tout un intérêt : la mise en évidence d'une mutation sur le gène S n'est possible que si une grande quantité d'ARN viral est présente dans le prélèvement analysé ; donc à défaut d'autre chose, détecter l'une de ces mutation indique que le prélèvement contient une forte charge de FCoV… ce qui est très en faveur d'un diagnostic de PIF. Ainsi, même si des articles récents ont montré que la mutation M1058L, notamment, est fortement associée à la PIF, (J. Zhu & Coll 2024, Q. Hong Duong & Coll 2026), le consensus actuel fait encore essentiellement reposer le diagnostic sur la détection d'une forte charge en ARN du coronavirus dans un prélèvement tel que du liquide d'ascite, de l'épanchement pleural ou un échantillon de tissu obtenu par cytoponction… même si cela n'est pas totalement spécifique.
8 - Et le diagnostic thérapeutique ?
Déjà, on va commencer par définir le diagnostic thérapeutique : c'est la démarche qui consiste, quand on soupçonne telle ou telle maladie mais qu'on n'en est pas très sûr, à donner le traitement de la maladie en question et si l'animal guérit, on se dit que ah ben oui, c'était sûrement bien ça.
Alors ça fait toujours bizarre de parler de diagnostic thérapeutique pour une maladie qui, pendant des décennies, n'a pas eu de traitement ; mais enfin, maintenant qu'on en a un efficace (voir le chapitre suivant)… après tout, pourquoi pas. Plus sérieusement, un diagnostic thérapeutique, ça n'a pas très bonne presse : ça fait un peu paresseux, pas très scientifique, (dans le genre : on ne sait pas trop, alors plutôt que de réfléchir, on va traiter et on verra bien), et puis est-ce qu'on ne risque pas de créer des résistances en utilisant des anti-viraux à tout va, sur des chats qui n'ont peut-être même pas la PIF ? Question évidemment légitime.
Il se trouve que la possibilité d'utiliser le diagnostic thérapeutique est abordée dans l'article de référence de S. Taylor & Coll, qui fait le point sur les connaissances en matière de traitement de la PIF en 2025… alors bon, quand même. Il y est écrit que dans certaines situations, il est quasiment impossible d'obtenir un diagnostic de certitude ; par exemple, parce que les tests ne sont pas disponibles, ou trop coûteux, ou que l'état du chat ne permet pas d'attendre plusieurs jours le résultat d'une RT-PCR ou plus long encore, d'une histologie ou d'une immuno-histochimie… le diagnostic thérapeutique peut alors se justifier, mais malgré tout à certaines conditions. D'abord, il faut tout de même qu'on ait des éléments de suspicion assez solides : par exemple un chat fiévreux avec un épanchement jaune paille pour lequel on ne trouve pas d'autre origine, ou bien un chat fiévreux avec une uvéite, et dans ces deux cas, une bonne élévation des globulines en prime. Si on a juste un chat avec un 39°C de fièvre depuis la veille, on oublie. (Ok, on caricature un peu). Ensuite, tant qu'à y être, on fait un "vrai" traitement, à dose normale, pas quatre jours avec des mini-doses comme on verra un peu plus loin dans le traitement des chats porteurs du FCoV intestinal, parce que là, pour le coup, c'est le meilleur moyen de créer des résistances aux médicaments. Enfin, pour que ce soit concluant, il faut qu'on ait une amélioration clinique rapide, c'est à dire une normalisation de la température en 48 heures, un retour à un comportement (quasi) normal en 2 à 5 jours, (10 jours maximum) et après, une disparition progressive des épanchements, des éventuelles manifestations oculaires et neurologiques, et une objectivation de ces améliorations avec les résultats d'analyse ou d'imagerie.
Signalons quand même, (on le verra au chapitre suivant), que le traitement n'est pas disponible en un claquement de doigt, (ça changera peut-être, mais en 2026, au moment où l'on écrit cet article, il doit être préparé au coup par coup, dans certaines pharmacies), et qu'il est loin d'être donné : donc, on ne va pas faire des diagnostics thérapeutiques comme ça, sur tous les chats qui passent !
Le traitement
Jusqu'à un passé récent, il n 'y avait aucun traitement pour la PIF : dans l'ensemble de la littérature scientifique mondiale, on ne trouvait que quelques descriptions tout à fait anecdotiques de survie, généralement brève, chez des chats traités par les corticoïdes à forte dose, les interférons, la ciclosporine… mais concrètement, lorsque l'on diagnostiquait une PIF chez un chat, nous devions malheureusement annoncer à ses propriétaires que leur compagnon allait se dégrader et décéder, le plus souvent rapidement, et sans que l'on puisse rien y faire… sinon abréger ses souffrances.
Et puis après plusieurs décennies à se désespérer à chaque nouveau cas de PIF, plusieurs molécules (analogues de l'adenosine nucléoside ou inhibiteurs de protéase) ont enfin fait la preuve de leur efficacité, à la toute fin des années 2010 !! Mais le sort s'acharnant décidément sur les matous, ces traitements étaient longs, astreignants, (administrés exclusivement en injections, souvent douloureuses), coûteux et par-dessus tout, n'étaient pas autorisés en France. Non pas pour des raisons médicales, effets secondaires ou autres, mais pour de bêtes questions de droits de la part des labos. Ils ne pouvaient donc être importés et utilisés qu'illégalement. Et puis enfin, parce que tout finit par arriver un jour si on y croit vraiment, (enfin, c'est ce qu'il faut se dire), un de ces médicaments, le GS-441524, qui plus est dans une version plus facile à administrer, (par voie orale), a finalement été autorisé chez nous. On fait le point ci-dessous.
Deux petites précisions avant de se lancer : déjà, on ne parlera ici que du GS-441524, et non des autres molécules dont l'efficacité sur la PIF a été reconnue plus ou moins en même temps : Remdesivir, Molnupiravir, GC376, notamment. D'abord parce qu'on ne peut pas (encore ?) les utiliser légalement, ensuite parce qu'elles ne semblent pas donner de meilleurs résultats que le GS-441524, (sinon peut-être en association, mais ce n'est même pas formellement démontré), et enfin parce que si on veut parler de toutes les molécules existantes dans cette page, on ne s'en sortira jamais !
Deuxième précision : les premières études concernant ces traitements remontent à 2019, et certaines publications sont sorties en 2025 ou 2026 : on ne dispose donc pas d'un recul de cinq ou dix ans pour affirmer que tel chat traité est définitivement guéri. Il faudra garder cette réserve à l'esprit, lorsqu'on parlera ci-dessous de guérison ou de rémission prolongée… en sachant que quand une maladie nous a habitués à un taux de mortalité de 100%, voir un chat toujours vivant et sans symptôme six mois ou un an après le traitement, avec normalisation biologique et disparition du FCoV de tous les tissus prélevés… il y a quand même de quoi se montrer optimiste !
1 - Le GS-441524 : enfin un traitement efficace !
En injections (les premières formulations)
La molécule miracle porte donc le doux nom de GS-441524. Il s'agit d'un analogue nucléosidique de l'adénosine, qui possède la propriété d'inhiber la transcription des ARN viraux. A noter que plusieurs autres molécules ont été utilisées avec des résultats à peu près comparables, (on citera, entre autres, le peptide anti-protéase GC 376, ou encore le Remdesevir (GS-5734) dont découle le GS-441524), mais ce dernier étant le seul autorisé en France, nous nous limiterons aux études le concernant.
L'efficacité du GS-441524 à inhiber la multiplication du virus de la PIF a d'abord été vérifiée en cultures cellulaires, puis chez 10 jeunes chats infectés expérimentalement (pffff, ben oui) (BG Murphy & Coll, 2018) : l'amélioration a été rapide, et tous les chats étaient asymptomatiques deux semaines après le début du traitement. Deux chats ont rechuté après 4 et 6 semaines, et ont bien répondu à une reprise du traitement ; lors de la publication de l'article, plus de 8 mois après l'infection, tous les chats étaient en bonne santé, et les seuls effets secondaires avaient consisté en réactions de douleur (miaulements, léchage…) tout de suite après l'injection.
La première étude portant sur le traitement de "vrais" chats malades, dans les conditions naturelles, a été réalisée par Pedersen & Coll, en 2019, avec la forme injectable du GS-441524, encore interdite d'utilisation chez nous, à l'époque. 31 chats (13 mois d'âge moyen) présentant une PIF (humide chez 26 chats, sèche chez 5), ont reçu le traitement, qui consistait en une injection par jour à des doses relativement faibles (2, puis si nécessaire 4 mg/kg/j), pendant au moins 12 semaines. Parmi ces 31 chats, 4 sont décédés ou ont été euthanasiés dans les 5 premiers jours, (on peut penser que la maladie était déjà trop avancée), et un après 26 jours, le traitement n'ayant pas eu d'effet sur lui. Chez les 26 autres chats, la réponse a été spectaculaire : normalisation de la température en 12 à 36 heures, en même temps que l'appétit, le niveau d'activité et le poids remontaient. Les épanchements ont disparu en quelques semaines, les ictères en 2 à 4 semaines. Les symptômes oculaires ont commencé à régresser après 24-48 heures seulement, jusqu'à une normalisation après 1 à 2 semaines. Quant aux ganglions intestinaux, leur taille diminua progressivement, tout au long du traitement. Sur les 26 chats encore en vie à l'issue de ce premier traitement, 8 ont rechuté 3 à 84 jours plus tard. Un seul a dû être euthanasié, les 7 autres revenant en rémission après reprise du traitement à une dose supérieure. Les indicateurs biologiques dont nous avons parlé plus haut (rapport Alb/Glob, charge virale…) se sont également améliorés pendant le traitement. Très peu d'effets secondaires ont été observé excepté - quand même - d'assez nombreuses, et parfois graves, réactions aux points d'injection du produit.
Donc, champagne ! Après des décennies à voir mourir tous nos chats atteints de PIF, tout cela était déjà franchement spectaculaire. Plusieurs autres articles sont venus confirmer ces premiers résultats :
Dans une étude de 2020 (PJ Dickinson & Coll) portant sur 4 chats présentant une forme sèche de PIF avec atteinte neurologique (ataxie, parésie, convulsions…), une chatte (qui présentait aussi des troubles oculaires) n'a pas répondu au traitement et a dû être euthanasiée après 216 jours, tandis que les trois autres étaient toujours vivants et sans symptôme 528, 516, et 354 jours après le début du traitement. Un point intéressant est que chez un de ces chats, la guérison s'est accompagnée de la disparition des anomalies de l'IRM cérébral, visibles avant le début du traitement. Les doses administrées étaient ici de 5 à 10 mg/kg/j pendant au moins 84 jours, donc plus élevées que chez Pedersen, vu la faible diffusion du GS-441524 dans l'œil et le système nerveux central. (20% seulement de la dose de GS-441524 absorbée passerait la barrière hémato-méningée).
Une étude réalisée à Wuhan (Y. Yin & Coll) en 2021 a conclu à la guérison clinique de 23/24 chats… "hautement suspects" de PIF, traités par le GS-441524 à la dose de 2-4 mg/kg/j pendant plus de 8 semaines.
Citons enfin la plus importante étude réalisée à ce jour, puisqu'elle a porté sur 629 chats atteints de PIF, en Iran (Mansari Mood, 2026). 497/629 chats (79%) ont été traités par le GS-441524 administré une fois par jour par voie injectable, les 21% restants étant également traités par voie injectable, mais avec passage à la voie orale, lorsque les injections finissaient par poser problème : quantités à injecter trop importantes, lésions au point d'injection, stress pour le chat… ou le propriétaire. Le dosage de départ était de 6-8 mg/kg/j pour les formes humides avec ascite ; 8 mg/kg/j pour celles avec épanchement pleural associé ou non à une ascite ; 9-10 mg/kg/j pour les formes sèches et les formes oculaires, et 10-12 mg/kg/j pour les formes neurologiques ou mixtes (c'est à dire humide + oculaire et/ou neurologique). En fonction de l'évolution des symptômes, la dose pouvait être augmentée, et était donc souvent légèrement supérieure à la fin du traitement (lui-même d'une durée minimum de 84 jours). A noter qu'un certain nombre de propriétaires ont dû acheter leur GS-441524 sur internet, utilisant parfois des marques différentes tout au long du traitement, avec les doutes que cela implique sur la qualité et le dosage du produit. Ceci étant dit, sur les 629 chats du départ, 592 (94,1%) pouvaient être considérés comme guéris, et avaient vécu entre 300 et 1470 jours après la fin du traitement. (Sachant que l'étude porte sur les années 2020-2024, et que le décompte est donc loin d'être terminé pour beaucoup de ces chats). 584 étaient toujours vivants au moment de la publication de l'article. Plus spécifiquement, parmi les patients présentant des formes de PIF neurologiques et/ou oculaires, ou mixtes, souvent considérées comme plus difficiles à traiter, 239/259 (92,2%) des chats ont été considérés comme guéris. Sur les 37 chats (5,9%) décédés pendant le traitement, 33 l'ont été pendant les 20 premiers jours, et 4 seulement au-delà ; cela rejoint ce qu'on a déjà lu dans d'autres articles, à savoir que si le chat tient bon jusqu'à ce que le traitement soit bien en place, (3-5 jours en général, un peu plus longtemps ici), alors il est très très bien parti. 4 chats (0,63%) sont morts au-delà la phase d'observation (soit plus de 90 jours après la fin du traitement), ce qui nous fait un taux de mortalité total de 6,48%. Enfin, pour 5 chats, le traitement a été arrêté avant les 84 jours règlementaires, essentiellement pour raisons économiques… ce qui ne les a pas empêchés d'être toujours vivants et en forme au moment de l'écriture de l'article. Plusieurs chats ont subi, sans problème, différentes interventions pendant leur traitement : on en reparle plus loin, dans la partie "Prévention" (3 - Prévention chez le chat guéri). A noter que des cristaux urinaires sont apparus pendant le traitement, chez certains chats de cette étude : on en reparle plus loin, dans la partie consacrée aux effets secondaires.
Tout ça, c'était déjà inespéré par rapport à ce qu'on avait connu, mais les injections, ce n'est pas toujours idéal quand même, surtout quand elles sont douloureuses, qu'il faut en faire pendant 84 jours ou plus, et que ce sont les propriétaires qui s'en chargent. Dans une étude portant sur 393 chats atteints de PIF, reposant sur les déclarations de propriétaires, recueillies par téléphone (S. Jones, 2021), des miaulements ont été rapportés dans 82% des cas, des douleurs au point d'injection dans 76%, des réactions de défense ou de l'agressivité dans 63%, et l'apparition de plaies, croûtes, cicatrices, saignements… au point d'injection, dans plus ou moins la moitié des cas.

Parmi les autres enseignements de cette étude, (à la fiabilité limitée car ne reposant donc que sur des déclarations téléphoniques), 88,2% des propriétaires ont noté une nette amélioration de l'état de leur animal dès la première semaine de traitement, avec un "retour à la normale" en moins de 4 semaines. Au moment de l'étude, 380 chats (96.7%) étaient vivants, dont 54% considérés comme guéris, 43.3% encore en observation, et 2,7% en traitement pour une rechute. Alors on pourra toujours dire que les inconvénients liés à l'injection valent bien un chat guéri de la PIF, mais bon… on a quand même vu arriver avec satisfaction un GS-441524 qui se prend par la bouche… et qu'on peut se procurer légalement !
Par voie orale (plus simple… et légal !)
La première description du traitement par voie orale (Addie & Coll, 2020) a concerné un Chat des Forêts Norvégiennes du nom de Skywise, âgé de 2 ans et vivant avec quatre autres chats, dont deux jeunes arrivés à la maison trois mois plus tôt (probablement porteurs de leur stock de FCoV). Skywise avait reçu son rappel de vaccin annuel cinq jours avant le début des symptômes ce qui, avec l'arrivée des jeunes chats, nous fait deux sources de stress consécutives (voir plus haut, la pathogénie de la PIF). A sa première consultation, Skywise était anémié, amaigri, en diarrhée intermittente, et il présentait une uvéite de l'œil droit, (il avait perdu le gauche quand il était chaton, il y en a vraiment qui cumulent…), ainsi qu'une hypertrophie des ganglions mésentériques. Un traitement a été mis en place, et c'est là que ça devient un peu compliqué : en effet, Skywize a reçu 50 jours de GS-441524, mais sans qu'on soit trop sûr de la dose que le fabriquant avait mise dans sa préparation : au moins 8 mg/kg/j, mais sans doute beaucoup plus. (Eh oui, aujourd'hui encore, le GS-441524 se présente sous forme de "préparations", et non de jolis petits comprimés bien calibrés. La différence par rapport à 2020 étant que le produit que l'on peut se procurer légalement en France depuis 2024, est préparé en pharmacie, de façon beaucoup plus rigoureuse !). Skywise a également reçu des corticoïdes par la bouche et en collyre avant le début du GS-441524, et 7 mois d'interféron oméga, après. Toujours est-il qu'après deux semaines, le chat avait repris du poids et courait après les oiseaux. Trois ans plus tard, il était toujours vivant et sans symptôme.
De nombreuses publications ont, par la suite, confirmé l'efficacité du GS-441524 administré per os (= par voie orale) : deux études de la même équipe (D. Krentz & Coll, 2021, Zwicklbauer & Coll, 2023), ont décrit l’évolution sur le long terme de 18 chats atteints de PIF, ayant reçu 84 jours de GS-441524 à la dose de 5 mg/kg/j s'ils ne présentaient pas de symptôme neurologique ou oculaire, et 10 mg/kg/j dans le cas contraire. (En fait, comme ci-dessus pour Skywize, l'analyse ultérieure du médicament administré a montré que le fabricant s'était un peu emmêlé les pinceaux, et que la préparation contenait plus de deux fois la dose de GS-441524 indiquée). L'amélioration a été rapide et spectaculaire dès les premiers jours de traitement, avec prise de poids, normalisation de la température, diminution des épanchements et amélioration des paramètres hématologiques et biochimiques (y compris la SAA : voir la partie consacrée au diagnostic). Plus intéressant encore, le FCoV avait été détecté dans le sang de 15 chats sur 18 avant traitement, mais la charge virale a commencé à diminuer massivement chez tous les chats 2 à 4 jours après le début du traitement, et à J14 et jusqu’à la fin du traitement, (12ème semaine) , plus aucun ARN viral n'était détectable dans le sang des chats. Un an après le début du traitement, 1 chat était malheureusement décédé dans un accident sur la voie publique, 3 avaient disparu dans la nature, (non ramenés aux contrôles par leurs propriétaires), et 14 ne présentaient plus aucun symptôme, excepté l’apparition transitoire, chez 2 d’entre eux, de signes neurologiques (syndrome d’hyperesthésie féline), dont nous avons parlé plus haut, dans le paragraphe consacré aux symptômes neurologiques. Deux ans après le diagnostic, les 14 chats étaient toujours vivants, sans anomalie clinique (y compris neurologique) ni biologique, et sans avoir connu de rechute. A noter que du FCoV a été retrouvé dans les selles de 5 d'entre eux pendant la période de suivi, probablement suite à une réinfection de la part de leurs colocs, et qu’une adénomégalie (= gros ganglion) abdominale persistante a été constatée chez 12 chats ; (résultat que l’on retrouve dans plusieurs études : voir plus haut, Ansari Mood, 2026). Aucun effet secondaire sérieux, de nature à interrompre le traitement, n'a été constaté parmi les 18 chats.
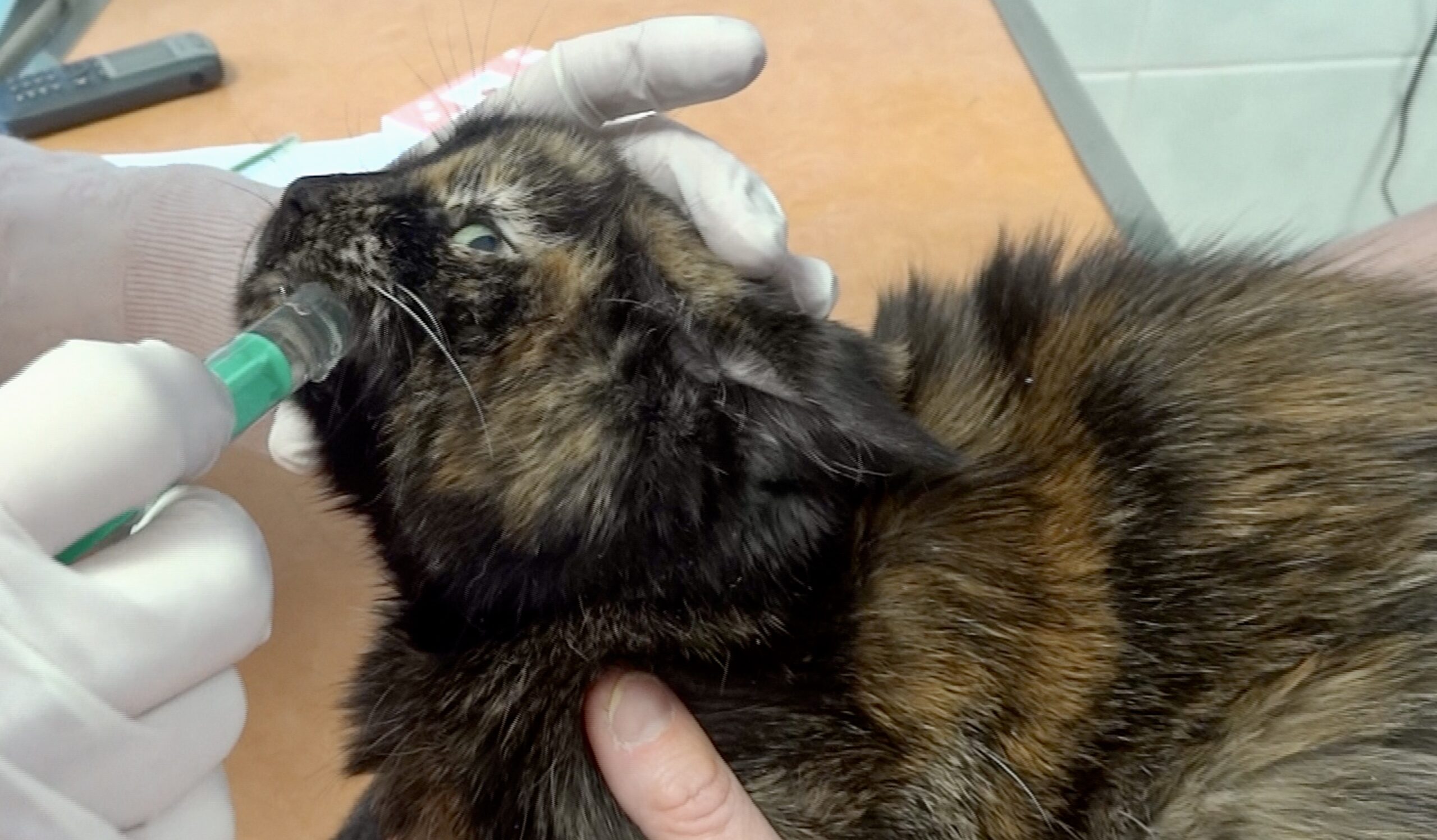
Finalement, quand on a pris l'habitude des injections, on pourrait se dire qu'une petite piqûre, ce n'est pas plus compliqué que l'administration quotidienne d'une pâte ou d'un comprimé à un chat récalcitrant - surtout quand on en est au 80ème jour et à la 80ème administration ! Cela dit, à efficacité comparable, (semble-t-il : on en parle plus loin), les irritations, voire lésions, aux points d'injection d'une part, l'aromatisation des solutions et pâtes orales d'autre part, font aujourd'hui pencher la balance en faveur des formes orales. Et de toute façon, ce sont les seules que l'on peut se procurer légalement en France ! Sur la photo ci-contre : cette minette n'a pas la PIF et ce n'est pas du GS-441524 qu'on lui fait avaler : seulement un peu d'eau pour faire passer un comprimé… et pour montrer que c'est possible sans traumatiser l'animal !
On ne va pas citer tous les articles montrant l'efficacité du GS-441524 administré per os. Mentionnons l'étude rétrospective (et un peu hétérogène) de Katayama & Coll (2021), avec 82% de guérison (116/141) chez des chats présentant une PIF humide et traités par le GS-441524 (per os pour la grande majorité) pendant 84 jours, à la dose… probable de 5 mg/kg/j (voir plus haut les incertitudes concernant le dosage de certaines formulations). Un point intéressant : les chats qui s'en sont sortis avaient en moyenne, au début du traitement, une température plus élevée (39,0°C vs 37,9°C) et un taux de bilirubine plus bas (16,1 µmol/l vs 53,2 µmol/l) que les chats qui n'ont pas survécu. Une autre étude des mêmes auteurs portant cette fois sur 324 chats, (Katayama & Coll, 2023), elle aussi assez hétérogène, notamment en terme de traitement, (la plupart des chats ont tout de même été traités per os), a trouvé un taux de survie de 85% (137/161) chez les chats présentant une PIF "mixte" (symptômes à la fois de PIF humide et de PIF sèche) et de 94% (153/163) chez ceux présentant une PIF sèche. Là aussi, les chances de guérison ont été associées à la température, et surtout au taux de bilirubine avant le début du traitement, avec des chances de survie de 97% pour un taux de bilirubine ≤ 8,6 µmol/l, 89% pour 8,6-17,1 µmol/l, 75% pour 17,1-34,2 µmol/l, 50% pour 34,2-68,4 µmol/l, et 14% quand la bilirubine était > 68,4 µmol/l. Alors ces chiffres correspondent bien sûr aux normes du laboratoire des auteurs, mais l'idée à retenir est que le pronostic est tout de même très lié au taux de bilirubine au début du traitement.
Une étude, (là, pour le coup, très très hétérogène), a compilé les résultats parus dans 11 articles pour un total de 650 chats traités, soit par le GS-441524 seul, soit par une association GS-441524 + interféron omega, Remdesivir, ou GC376 (Gokalsing & Coll, 2025) : les taux de guérison ont semblé plus élevés avec les traitements associant deux molécules (94,8% vs 83,1%), mais l'hétérogénéité des groupes de chats rend toute conclusion impossible. Même chose pour l'administration du GS-441524 par voie orale (87% de guérison) ou injectable (77%). De moins bons résultats ont été obtenus dans les formes neurologiques (67,7%), mais avec des doses de GS-441524 plus faibles que celles utilisées aujourd'hui (voir plus loin, le paragraphe "En pratique"). Ce qu'on retiendra donc de cet article est que globalement, en s'appuyant sur un grand nombre de cas, autour de 85% des chats atteints de PIF ont été guéris par le GS-441524, seul ou en association avec deux autres nouvelles molécules.
Allez, encore une étude bien intéressante, celle-ci prospective et randomisée, c'est à dire qu'on n'a pas choisi d'affecter tel chat à un groupe plutôt qu'à l'autre. AM Zuzzi-Krebitz & Coll (2024) ont comparé les résultats obtenus en traitant par le GS-441524, à la dose de 15 mg/kg/j per os, 40 chats atteints de forme humide de PIF : 20 pendant la durée habituelle de 84 jours, et 20 pendant 42 jours seulement. Résultat : match nul : un décès dans chaque groupe, (dont un après 3 jours de traitement), et 19 chats en rémission complète de chaque côté 168 jours après le début du traitement. Donc, sans doute un résultat à confirmer avec un peu plus de recul, un peu plus de chats, et d'autres formes que des PIF humides, avant de s'arrêter à 42 jours de traitement pour tout le monde, mais c'est quand même bien encourageant. Et au passage… ça nous fait une étude avec 95% de rémission prolongée (38/40 chats) avec le seul GS-441524 per os, et même 97,4% si l'on tient compte du fait que l'un des deux chats décédés est mort au 3ème jour du traitement, avant donc que ce dernier ait eu le temps de faire grand chose.
A noter, parmi les recommandations de 2025 du "FIP Advisory Board" (S. Taylor & Coll) : il existe chez certains chats une mauvaise absorption intestinale du GS-441524 : on le soupçonne en cas d'amélioration insuffisante, ou pas assez rapide, de l'état clinique ou des constantes biologiques (voir ci-dessous, le paragraphe consacré au suivi du traitement). La dose de GS-441524 pourra alors être augmentée. De même, certains chats répondront mieux à une administration fractionnée, (par exemple 10 mg/kg matin et soir, plutôt que 20 mg/kg en une seule fois) : tout cela est à juger au cas par cas, en fonction du suivi du traitement.
Alors, oral, ou injectable ?
Il serait tentant de dire : Les deux, mon colonel. Dans bon nombre d'études, en effet, le traitement est attaqué sous forme injectable, le temps que l'état du chat se stabilise et qu'il soit capable d'avaler des médicaments sans les vomir tout de suite après, puis poursuivi par voie orale. Mais concernant l'efficacité pure, on ne peut pas dire à ce stade si le GS-441524 est plus efficace par voie orale, par voie injectable, ou s'il n'y a pas de différence : en effet, dans les publications où les deux formulations étaient utilisées en parallèle, soit le nombre de chats traités par l'une ou par l'autre était insuffisant pour constater une différence statistiquement significative, soit les protocoles de traitement étaient vraiment trop hétérogènes ; (plusieurs antiviraux utilisés chez certains chats et pas chez d'autres, par exemple).
Il est donc urgent d'attendre pour se prononcer, et comme de toute façon, la forme injectable n'est pas accessible légalement et qu'elle peut provoquer de sévères lésions au point d'injection… on privilégiera pour l'instant les formes orales. Petit détail qui n'en est pas vraiment un, vu le coût d'un traitement par le GS-441524 : les préparations orales sont actuellement un peu moins chères que les formes injectables.
Et donc, concrètement ?
Bon, tout cela fait beaucoup d'informations mais concrètement, quel traitement recevra votre chat s'il nous est présenté avec un gros ventre plein d'épanchement, des signes neurologiques, une uvéite… et que nous posons un diagnostic de PIF ?
Première chose à savoir, dont on a déjà bien parlé, au demeurant : vu la nouveauté du produit, de son autorisation en France, et l'urgence d'en disposer chez les chats atteints de PIF, le médicament qui vous sera délivré ne se présentera pas, pour l'instant du moins, sous forme de comprimés ou de solutés buvables produits industriellement, mais de préparations magistrales, à savoir, selon la définition du site santé.gouv.fr, de médicaments "réalisés pour un patient déterminé et selon une prescription médicale, en raison de l’absence de spécialité disponible ou adaptée". Le médicament est donc actuellement préparé en pharmacie, sur ordonnance du vétérinaire, à partir du principe actif, le GS-441524.


Quelques exemples de préparations magistrales de GS-441524, en pâte ou en solution orale aromatisées. Nous en avons mis plusieurs, vu que nous n'avons pas d'actions chez les uns ou chez les autres !
Quelques pharmacies spécialisées dans les préparations magistrales, (et pouvant apporter des garanties quant à leur fournisseur et à la qualité du principe actif), sont actuellement en mesure de délivrer le GS-441524. (On insiste bien sur les garanties et la préparation en pharmacie : il n'est pas question d'aller acheter n'importe quoi sur internet !). Il existe, à ce stade, deux présentations disponibles en France : une pâte orale et une suspension buvable, toutes deux aromatisées pour faciliter leur prise par les chats (photos ci-dessus). Il peut y avoir des variations d'un préparateur à l'autre, mais la pâte orale est généralement dosée à 3,75 mg ou à 7,5 mg pour 0,05 ml de la préparation. Elle peut être administrée directement dans la bouche du minou, ou mélangée à un peu de nourriture humide ; on dit bien "un peu", car le chat doit être à jeun 30 à 60 mn avant et après la prise du médicament. La dose habituellement recommandée est de 15 mg/kg/j, en une ou deux prises, pour les formes humides, ou les formes sèches sans signe neurologique ni oculaire, et de 20-22,5 mg/kg/j, là aussi en une ou deux prises, pour les formes neurologiques ou oculaires, le tout pendant 84 jours… mais tout cela à moduler selon les recommandations du préparateur, et surtout la prescription de votre vétérinaire. Le chat devra être pesé régulièrement pendant le traitement, parce qu'indépendamment de l'importance du poids dans le suivi, si le minou était tout maigre en début de traitement et qu'il regrossit, ou si au contraire il maigrit, la dose du médicament devra être ajustée à son nouveau poids. Des schémas sont généralement fournis avec le médicament pour savoir comment utiliser le flacon doseur.
La suspension buvable est habituellement dosée à 50 mg/ml. Elle aussi peut être administrée directement dans la bouche du chat, ou mélangée à un peu d'aliment humide (une seringue et des conseils pour une administration correcte sont fournis avec le flacon). Les autres informations et recommandations, (notamment le jeûne de 30-60 mn avant et après chaque prise), sont les mêmes que pour la pâte orale.
Ci-contre : GATSBY, Scottish fold de 13 ans, présenté pour abattement, anorexie, perte de poids rapide, et ascite importante. Photographié ici par ses maîtres après 55 jours de traitement par le GS-441524 en suspension ou pâte orale… il n'a pas l'air d'aller si mal que ça !

Deux points à préciser :
- On l'a vu, il s'agit de préparations magistrales. Comme le rappelle l'Agence Nationale du Médicament Vétérinaire (ANMV), celles-ci "n’étant pas soumises à autorisation préalable, aucune évaluation de la qualité, de l’innocuité ou de l’efficacité n’a été réalisée par l’ANMV. Celle-ci n'a donc pas effectué d'évaluation spécifique sur la forme galénique utilisée. Les préparations magistrales ne sont en effet pas évaluées par l'ANMV car elles sont réalisées sur mesure pour un patient spécifique, contrairement aux spécialités pharmaceutiques avec AMM (= Autorisation de Mise sur le Marché), qui sont soumises à une évaluation rigoureuse pour un usage à grande échelle". Bon, après, quand on a un traitement efficace dans 80-90% des cas (voire plus), pour traiter une maladie mortelle dans 100% des cas sans traitement… on ne va peut-être pas trop chipoter, d'autant que jusqu'ici, il n'y a pas eu d'effets secondaires sérieux rapportés avec les formes orales, et seulement de façon exceptionnelle avec les formes injectables (voir le paragraphe suivant)..
- Tous les éléments ci-dessus sont donnés à titre indicatif : en effet, le traitement, (dose, durée…), qui vous sera prescrit par votre vétérinaire dépendra de l'état du minou, de ses symptômes, des résultats de ses analyses, mais aussi de l'évolution des connaissances : cet article a été écrit début 2026, le GS-441524 n'est disponible en France que depuis courant 2024… autant dire que de nouvelles formulations (comprimés…) et voies d'administration, de nouveaux dosages, des effets secondaires toujours possibles, voire de nouvelles molécules, verront probablement le jour dans un futur proche… alors que cet article ne sera peut-être pas réactualisé tous les 15 jours ! Donc, suivre avant tout la prescription de votre vétérinaire.
Des effets secondaires ?
Puisqu'on en parlait…
Alors, comme d'habitude, on ne s'intéressera qu'au GS-441524, seul traitement de la PIF autorisé chez nous, du moins pour l'instant : on oublie les Remdesivir, Molnupiravir et autres EIDD-1931, et on ne reviendra pas sur les irritations ou lésions cutanées causées par la forme injectable du GS-441524 : on en a parlé plus haut. Le document le plus "up to date", (du moins au moment de l'écriture de cet article), consacré au traitement de la PIF, (On parle de la mise au point de S. Taylor & Coll de juillet 2025, dont on trouvera les coordonnées complètes dans les références), décrit deux effets secondaires :
Une augmentation de l'activité des ALAT (une enzyme présente dans les cellules du foie), chez moins de 30% des chats traités. Certains prescrivent des hépatoprotecteurs lorsque ça arrive, mais leur utilité n'a pas été démontrée, et les ALAT reviennent à la normale à la fin du traitement. Même chose pour deux catégories de cellules sanguines, les polynucléaires éosinophiles et les lymphocytes, qui augmentent modérément pendant le traitement de GS-441524, et reviennent à la normale quand celui-ci se termine, sans qu'aucun traitement n'ait été nécessaire. Bon, jusque-là, pas de quoi fouetter un chat.
Un peu (beaucoup) plus embêtant : des calculs urinaires ont été exceptionnellement décrits chez des chats recevant du GS-441524. A ce jour, (début 2026), il semble qu'une seule étude, concernant deux chats (M. Allinder & Coll, 2024), ait rapporté cet effet secondaire, mais avec quand même présence de calculs dans les reins, les uretères et la vessie qui ont entraîné une insuffisance rénale et, malgré la mise en œuvre de soins lourds (exérèse chirurgicale des calculs vésicaux, pose d'une dérivation urétérale (SUB)…), le décès des deux patients. Dans les deux cas, les calculs étaient constitués à 98% de GS-441524, mais dans les deux cas également, il s'agissait d'un traitement acheté sur internet, sans aucune garantie concernant sa composition et en particulier sa concentration en principe actif.
Dans l'étude iranienne déjà citée (M. Ansari Mood, 2026), portant sur 629 chats traités par le GS-441524, essentiellement par voie injectable, des cristaux urinaires, absents au début de l'étude, ont été mis en évidence dans la vessie chez 11,25% des chats au 56ème jour de traitement, et 4,5% au 83ème jour. (Entre temps, certaines mesures, dont un changement d'alimentation, avaient été prises). Les chats en question présentaient des signes cliniques liés à la présence des cristaux. Il ne semble pas que ces derniers aient été analysés. Mais comme dans l'étude de Allinder & Coll, un certain nombre de propriétaires avaient dû acheter leur GS-441524 sur internet, changeant parfois de marque en cours de traitement, avec les doutes que cela implique sur la qualité et le dosage du produit.
Que retenir de tout cela ? D'abord qu'il s'agit d'effets secondaires graves, ayant tout de même conduit au décès des deux chats dans l'article d'Allinder & Coll, mais d'une part, causés par des médicaments d'origine et de qualité incertaines, et d'autre part très exceptionnels, car non rapportés dans les multiples études mentionnées tout au long de cet article, qui regroupent en tout des centaines (des milliers ?) de chats traités par le GS-441524. L'étude iranienne doit être prise en considération, mais il ne semble pas démontré que les cristaux étaient composés de GS-441524 et de toute façon, ils n'ont pas été à l'origine de symptômes graves - si on les compare à ceux de la PIF !
Donc pas de panique, ce n'est pas parce que deux chats dans le monde (et même s'il y en a quelques autres ces prochaines années…), sont décédés à cause de calculs de GS-441524, qu'il faut arrêter de traiter, et laisser à nouveau tous les chats mourir de PIF. Mais maintenant qu'on sait que ça existe, autant, bien sûr, être vigilant de ce côté-là. Normalement, une échographie abdominale est réalisée au moment du diagnostic pour rechercher une ascite, identifier une masse ou mettre en évidence de gros ganglions… et l'ensemble de l'abdomen est, bien sûr, inspecté au passage. Si des calculs sont présents dans l'appareil urinaire, ou des cristaux dans la vessie, ils doivent donc être repérés à ce moment-là, et l'échographie sera alors complétée par une analyse d'urines. La fonction rénale est également vérifiée dans le bilan sanguin réalisé lors du diagnostic, ou avant la mise en place du traitement. Et les mêmes examens seront renouvelés lors des contrôles prévus en cours de traitement donc normalement, calculs et cristaux doivent être repérés avant que la situation ne dérape vraiment, et le traitement ajusté en conséquence.
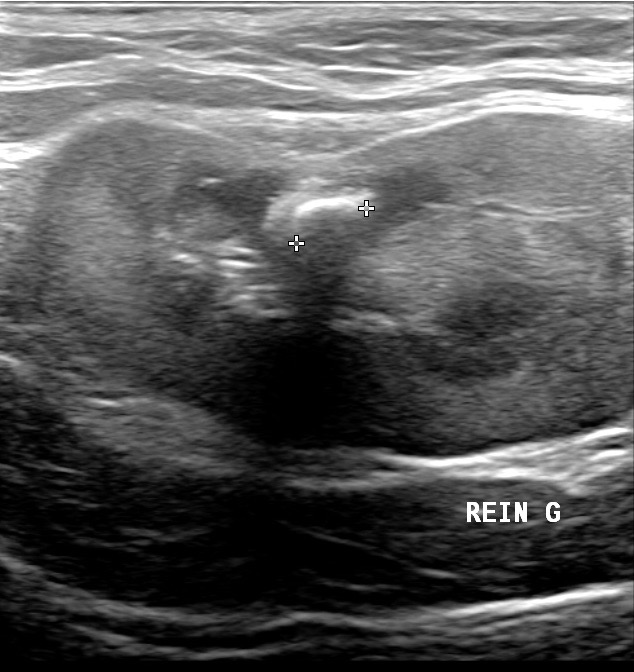
Un calcul de 5 mm dans le rein gauche d'un chat atteint de PIF (celui dont on a vu l'uvéite un peu plus haut) : il ne s'agit pas d'un calcul de GS-441524, car du fait de son très mauvais état général, le chat n'a malheureusement pas été traité. Mais s'il l'avait été, la découverte de ce calcul aurait, bien sûr, été importante avant la mise en place du traitement.
Les traitements adjuvants, pour compléter
Alors là, pour une fois, on va faire court parce que ça tombe sous le sens : outre le traitement de la cause (le virus), on va évidemment soulager le chat et si certains organes sont déjà bien touchés, essayer de limiter les dégâts et de sauver ce qui peut être sauvé. Déjà, ou va soutenir l'état général si le chat n'est vraiment pas bien : hospitaliser pour perfuser, s'il est déshydraté ou en insuffisance rénale, rénutrir si nécessaire, etc. On luttera contre la douleur si le chat a mal, on lui injectera des antiémétiques s'il vomit… Après, il y aura des traitements plus spécifiques en fonction des symptômes : collyres anti-inflammatoires, mydriatiques (pour dilater la pupille) en cas d'uvéite, avant de se retrouver avec un glaucome, des adhérences (synéchies) et au bout du compte, la perte de l'œil. On administrera des anti-convulsivants à un chat présentant une forme nerveuse avec des crises convulsives, etc. Encore une fois, tout cela tombe un peu sous le sens. Et puis ce n'est pas vraiment un traitement adjuvant au sens strict, mais en cas d'épanchement pleural, ou parfois même d'épanchement abdominal très important, l'un ou l'autre à l'origine de difficultés respiratoires, il pourra être nécessaire pour le confort du chat - ou même pour sa survie ! - d'aspirer le maximum de liquide, voire de mettre en place un dispositif de drainage.
2 - Comment savoir si ça marche ? Le suivi du traitement
Mesurer la (re)prise de poids est un moyen simple de contrôler l'efficacité du traitement. Sans compter que des pesées régulières (une fois par semaine) sont nécessaires pour ajuster la dose des médicaments (le GS-441524 surtout, mais aussi d'éventuels traitements adjuvants), au nouveau poids du chat.
Les symptômes généraux, et la fièvre en particulier, s'améliorent généralement dès les premiers jours : la température se normalise en 48 heures, et le chat retrouve un comportement (quasi) normal en 2 à 5 jours (10 jours maximum). On peut lire que les épanchements, lorsqu'il y en a, disparaissent en deux semaines… mais ça peut quand même prendre un peu plus de temps ! La taille des ganglions abdominaux diminue progressivement, mais reste souvent supérieure à la normale (Zwicklbauer & Coll, 2023) ; dans l'étude d'Ansari Mood déjà citée, elle était supérieure aux valeurs usuelles chez près de la moitié des chats en fin de traitement.
D'un point de vue sanguin, la bilirubine, dont on a vu plus haut l'intérêt pronostique en début de traitement, se normalise rapidement en cas de traitement efficace, suivie par une remontée de l'hématocrite (le taux de globules rouges dans le sang). La normalisation de l'hyperglobulinémie, et par conséquent du rapport Alb/Glob, peut prendre plus de temps.
Un exemple de suivi : une jeune chatte Sacrée de Birmanie nous a été présentée à l'âge de 5 mois et demi avec une hyperthermie (39,5°C), des muqueuses pâles et ictériques et à l'échographie, plusieurs gros ganglions sphériques au milieu de l'abdomen (en revanche, pas trace d'épanchement). Les tests FeLV et FIV étaient négatifs, mais la RT-PCR sur sang est revenue positive pour le coronavirus félin, avec une charge compatible avec une PIF - en l'occurrence, donc, une PIF sèche.
D'un point de vue clinique, l'amélioration sous traitement par le GS-441524 a été rapide avec retour des comportements de jeu et disparition de l'ictère. Une prise de poids de 150 g a été constatée dès la première semaine et en fin de traitement, le poids de la chatte était passé de 2,3 kg à J0 à 3,5 kg à J80. A l'échographie de contrôle à un mois, les ganglions mésentériques avaient repris une forme et une taille normales.
Les résultats de biochimie étaient très modifiés à J0, avec en particulier des protéines totales > 110 g/l, (l'analyseur ne dosait pas au-delà), des globulines > 100 g/l (idem), et une albumine = 22 g/l. Nous n'avons malheureusement pas de tracé d'électrophorèse pour servir de point de départ, mais ces chiffres sont à comparer aux résultats et aux valeurs de référence qui apparaissent sous l'électrophorèse ci-contre, réalisée après 82 jours de traitement par le GS-441524. (Respectivement 66 g/l, 31,9 g/l et 34,1 g/l). Le tracé de l'électrophorèse, quasiment normalisé, peut être comparé à celui d'un chat, le jour de son diagnostic de PIF, un peu plus haut dans cet article (Chapitre Diagnostic, paragraphe 3 - Hématologie et biochimie). Côté hématologie, on partait à J0 d'un hématocrite de 9,1% (valeurs de référence = 24-45 !) et d'un taux d'hémoglobine de 3,1 g/dl (8-15) pour arriver, à J82, à un hématocrite de 28,7% et une hémoglobine de 9,8%.
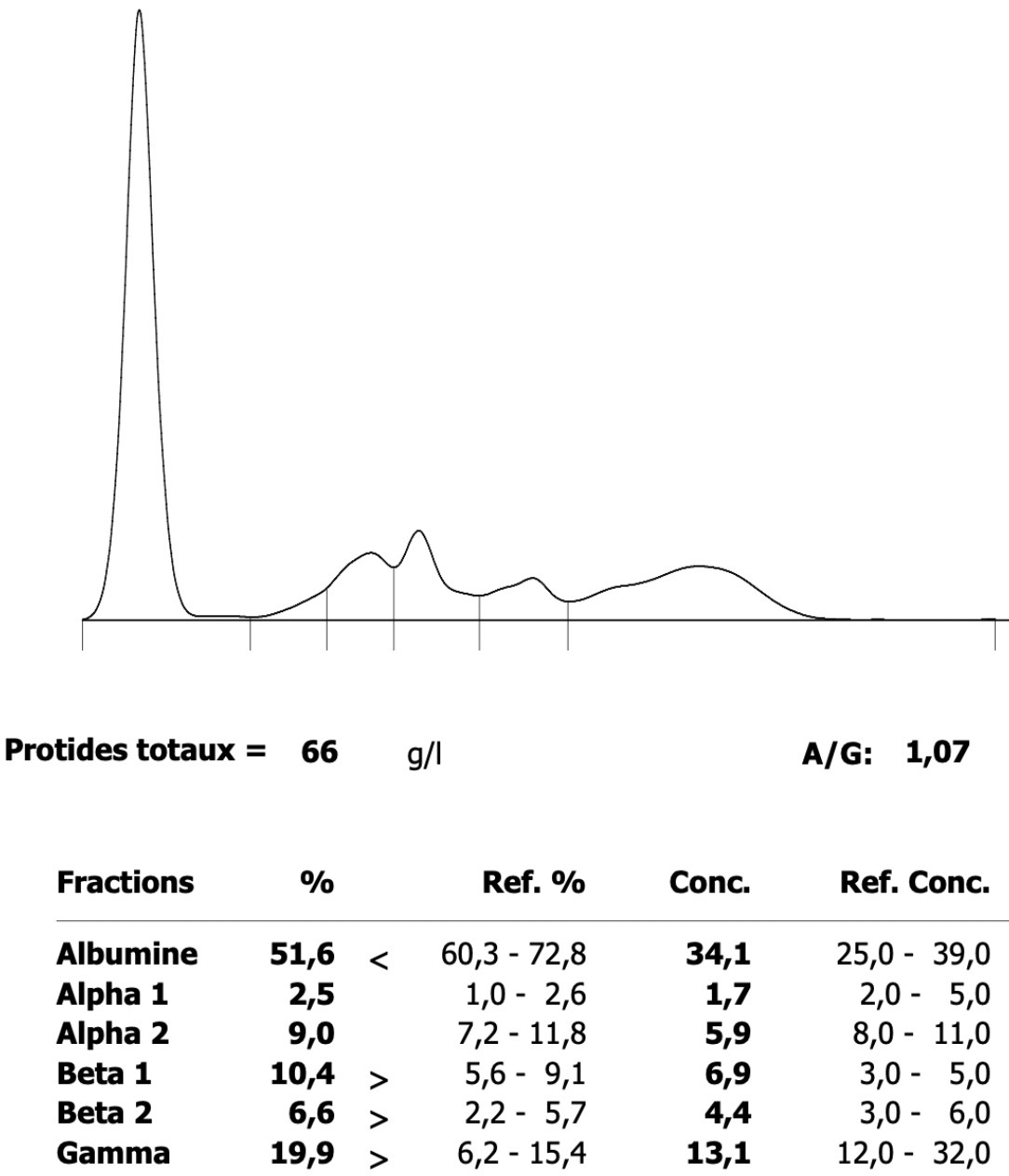
Ces résultats permettent d'objectiver l'évolution favorable sous traitement, de pouvoir affirmer la guérison ou du moins (tant qu'on n'a pas le recul suffisant), la rémission, de décider de l'arrêt ou non du traitement à la fin du protocole, et d'anticiper une éventuelle rechute (par exemple si l'on observe une remontée des globulines lors d'un contrôle programmé, ou à l'occasion d'un épisode de fièvre, de fatigue…)
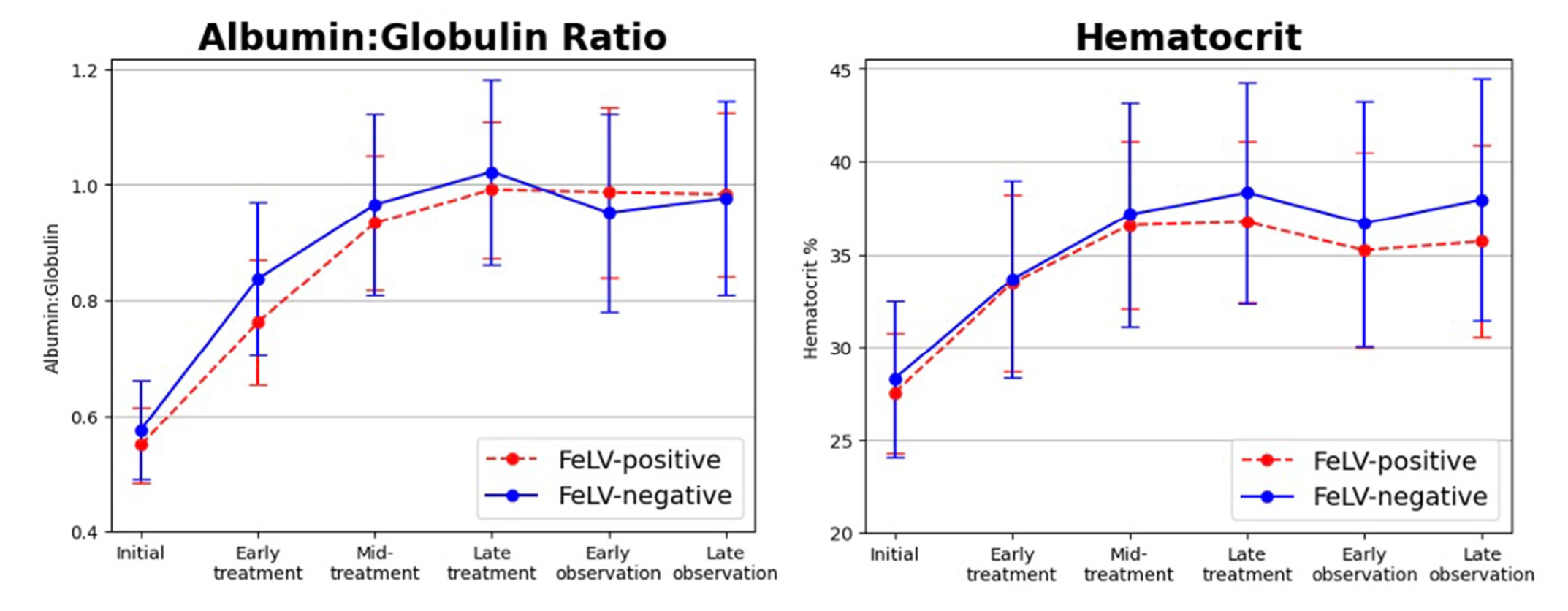
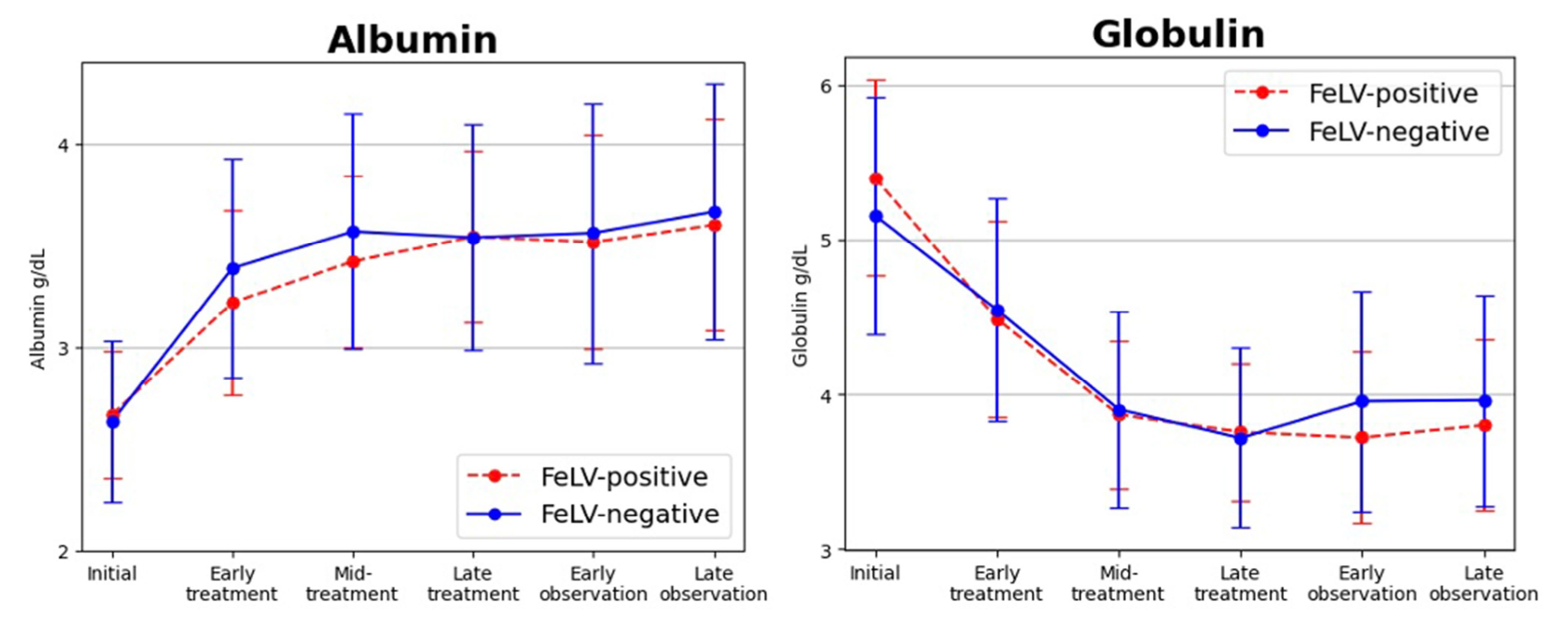
Les quatre graphiques ci-dessus, dont on reparlera plus loin, (paragraphe 5 : Quand le FeLV s'en mêle), montrent l'augmentation rapide de l'hématocrite, du taux d'albumine et du rapport Alb/Glob, ainsi que la baisse du taux de globuline, dès le début du traitement par le GS-441524. (Source : LaVigne & Coll, 2025).
On a vu l'intérêt de l'AGP dans le diagnostic de la PIF : sa normalisation rapide est d'un bon pronostic ; quand tout se passe bien, sa concentration commence à diminuer 48 heures après le début de l'administration du GS-441524 par voie orale, avec une normalisation au bout de 28 jours. Deux dosages d'AGP dans les valeurs usuelles à une ou deux semaines d'intervalle, sont un bon indicateur de guérison (ou de rémission durable) et peuvent être utiles pour une éventuelle décision d'arrêter le traitement à 42 jours au lieu de 84, comme on l'a vu plus haut… mais tout cela, bien sûr, avec prudence et seulement pour les PIF humides : en 2026, on manque encore de recul par rapport à ces traitements "courts". Le SAA est également un bon indicateur de l'efficacité du GS-441524 , avec un retour à la normale après une semaine de traitement.
Ce qui ne sert à rien :
- la sérologie (le dosage des anticorps anti-FCoV), qui peut rester positive après un traitement efficace.
- La persistance d'une adénomégalie abdominale et particulièrement mésentérique (= les ganglions le long de l'intestin ; on en a vu des exemples plus haut), chez un chat qui va bien après traitement, et en dehors de toute rechute.
- Certains signes neurologiques, (notamment le syndrome d'hyperesthésie féline dont on a parlé plus haut, avec léchage obsessionnel, etc), qui peuvent apparaître pendant un traitement par ailleurs efficace, ou persister en fin de traitement, sans que cela signe une rechute… mais parfois, si ! (Les choses ne sont décidément jamais simples).
3 - Faut-il traiter les chats asymptomatiques ?
Alors, attention, sujet polémique !!! Certaines publications, (DD Addie & Coll, 2023), ont montré qu'un court traitement à base de GS-441524 à faible dose (4 jours à 4 mg/kg/j par voie orale), permettait de stopper l'excrétion par les selles du FCoV, chez des chats vivant en collectivité. Par la suite, aucun de ces chats ne développa une PIF au cours des 6 mois à 3,5 ans suivants, contrairement à ce qui se passe habituellement dans des populations (à peu près) comparables. (Etude réalisée sur 147 chats, dont 109 excrétaient le FCoV, 25 ne l'excrétaient pas, et 13 étaient traités pour PIF). En outre, certains de ces chats présentant, parfois depuis des années, une diarrhée chronique due à l'infection par le FCoV intestinal, ont vu leurs symptômes digestifs disparaître. Les auteurs concluent que quand on a plusieurs chats à la maison et qu'il y a du FCoV qui circule, une petite cure de GS-441524 pourrait diminuer/supprimer le risque que l'un d'eux nous sorte une PIF dans les mois ou les années qui suivent et que même, chez un chat souffrant d'une maladie inflammatoire chronique de l'intestin, ce pourrait être une bonne idée d'utiliser ces quatre jours de GS-441524 comme une sorte de diagnostic thérapeutique, avant de se lancer dans des explorations plus invasives comme endoscopie et biopsies digestives : si ça guérit avec 4 jours de GS-441524, on peut en conclure que la diarrhée chronique était due au FCoV, et voilà !
Alors, tout cela est bien tentant, mais les courts traitements de GS-441524 à faible dose, ce n'est définitivement pas du tout du tout une bonne idée (et c'est le groupe de spécialistes européens de la PIF qui le dit dans sa mise à jour 2025) : d'abord parce que ce genre de protocole est le meilleur moyen de faire émerger des virus résistants aux traitements, surtout avec des créatures aussi imprévisibles que les coronavirus ! Une bonne gestion des anti-microbiens consiste d'ailleurs à n'utiliser les anti-viraux que lorsqu'ils sont nécessaires, c'est à dire en cas de risque vital (donc, dans le cas présent, quand on a un diagnostic ou, vraiment, une très forte suspicion de PIF). Ensuite, le FCoV est tellement répandu qu'à la moindre (ré)introduction de chat, on risque de se retrouver à nouveau avec du FCoV qui circule, et le mini-traitement n'aura servi à rien. Et enfin, aux dernières nouvelles, il ne serait même plus vraiment sûr que le GS-441524 empêche à tous les coups l'excrétion du virus.
4 - Quand le FeLV s'en mêle : des résultats surprenants !
Quitte à ce que l'homogénéité du plan de l'article en souffre un peu, on a fait du traitement des chats atteints de PIF ET infectés par le FeLV, (certains n'ont vraiment pas de chance), un paragraphe à part, parce que les résultats qui suivent sont étonnants et viennent renforcer l'intérêt des traitements anti-viraux de la PIF, en particulier du GR-441524. Pour mémoire, le FeLV (pour Feline Leukemia Virus, ou virus leucémogène félin), est un rétrovirus contagieux de chat à chat, (transmission par morsure, léchage, gamelles communes, litières communes, lactation, transfusion sanguine…), responsable entre autres d'un déficit immunitaire, (le chat infecté attrape un peu tout ce qui passe), d'anémies, de cancers, (lymphomes, leucémies…), etc. Sachant que l'incubation peut être longue, et que certains chats, chez qui la réponse immunitaire est suffisante pour contenir le virus, (on parle d'infection régressive) peuvent ne présenter aucun symptôme, et avoir des tests de diagnostic (antigénique et PCR) négatifs… aussi longtemps du moins que leur système immunitaire tient bon. (On simplifie un peu mais en gros, c'est ça). D'un point de vue traitement, on peut traiter certains symptômes, les infections (coryza ou autre) qui ont profité du déficit immunitaire pour s'installer… mais globalement, ce n'est quand même pas bien réjouissant quand on trouve le FeLV chez un chat. Alors quand le FeLV est, en plus, associé à une PIF qu'il a probablement contribué à déclencher… vous imaginez !
Une étude publiée en septembre 2025 (LaVigne & Coll) a été réalisée dans un refuge spécialisé dans l'adoption de chats infectés par le FeLV. 170 chats atteints de PIF, dont 104 positifs pour le FeLV (test Snap Idexx), et 66 négatifs, ont reçu un traitement de 84 jours par le GS-441524 (par voie injectable au départ, puis relais par voie orale), suivi d'une période d'observation, également de 84 jours (tableau ci-dessous). Le pourcentage de chats encore vivants dans les deux groupes ne différait significativement ni à l'issue de la phase de traitement (79% / 76%), ni à la fin de celle d'observation (74% / 74%). Comme dans d'autres études citées plus haut, si l'on exclut de ces statistiques les chats décédés au cours des 7 premiers jours de traitement, (dont on peut supposer que l'organisme était déjà trop atteint par la maladie), on arrive à un taux de survie de 86%. Les courbes montrant l'amélioration parallèle, FeLV ou pas, des taux d'hémoglobine et du rapport Alb/Glob, sont reproduites un peu plus haut dans ce chapitre (paragraphe 2, consacré au contrôle du traitement). Comme le FeLV reste le FeLV, les chats atteints par ce virus ont tout de même vécu globalement moins longtemps, mais avec une médiane de survie de 524 jours quand même (valeurs limites : 1 - 1585). En comparaison, pour les chats du groupe négatif pour le FeLV, la médiane de survie n'était toujours pas atteinte après 4 ans de suivi. (Pour mémoire, la médiane de survie = le délai au bout duquel la moitié d'une population est décédée… quelle qu'en soit la cause : PIF, voiture, Pit bull, mort aux rats… dans le cas présent, cela signifie qu'au bout de 4 ans, plus de la moitié des chats non porteurs du FeLV, traités pour une PIF par le GR-441524, étaient toujours vivants).
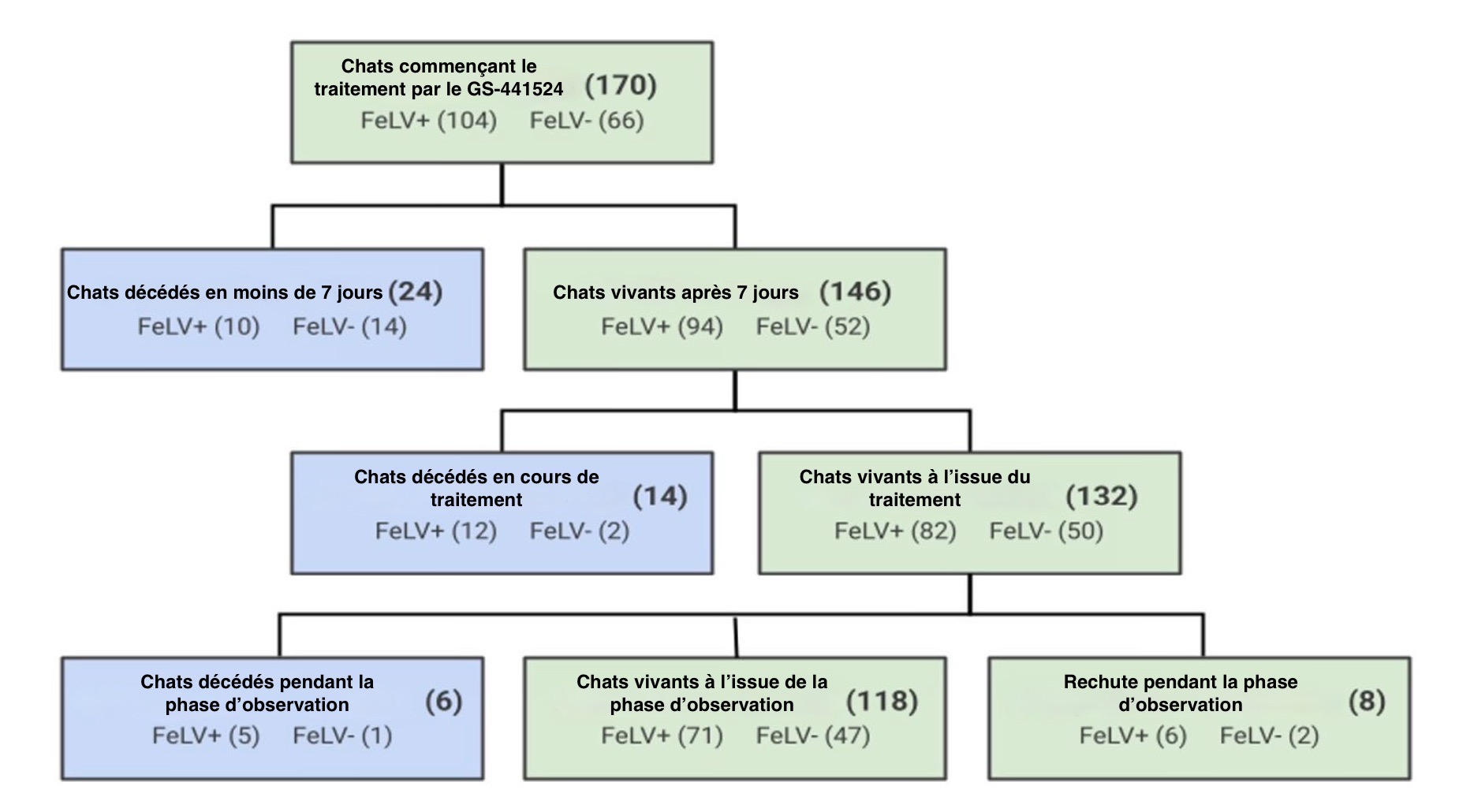
D'après LaVigne & Coll, 2025 : Evolution sous traitement par le GS-441524, de 170 chats ayant contracté la PIF, dont 104 également infectés par le FeLV, et 66 n'ayant "que" la PIF. Les cases bleues correspondent aux chats décédés (naturellement ou par euthanasie) pendant les périodes de traitement ou d'observation, et les cases vertes, à ceux qui s'en sont sortis.
Bon, quelles conséquences peut-on tirer de tout ça ? 1) La PIF, on l'a vu plus haut, est souvent déclenchée chez des chats porteurs d'un FCoV intestinal qui se tenait tranquille jusque là, par un événement extérieur, (abandon, chirurgie…), mais particulièrement par une maladie intercurrente ; et dans ce domaine, l'infection par le FeLV, ça se pose un peu là ! Eh bien cette étude nous montre que quand on diagnostique une PIF et qu'on fait un bilan avant de mettre en place le traitement par le GS-441524, s'il s'avère que le chat est positif pour le FeLV, il ne faut pas se dire que pffff, ça ne sert à rien de traiter la PIF, le chat va mourir et on n'a qu'à l'euthanasier tout de suite. Parce que certes, c'est quand même mieux si le chat est négatif pour le FeLV, il se peut qu'il décède dès les premières semaines de traitement, mais dans la présente étude, 50% des FeLV+ ont vécu au moins 524 jours, et il y en a un qui a dépassé les 4 ans. 2) On retrouve ici les très bons résultats après traitement publiés dans les études récentes : à savoir que dans le groupe des chats indemnes de FeLV, si l'on exclut les chats décédés pendant la première semaine de traitement, (dont on peut penser que l'organisme était tellement atteint que tuer le virus avec le GS-441524 ne servait plus à rien), on obtient plus de 92% de chats encore vivants un an après la mise en route du traitement. Et 3) Dans les premières publications de la fin des années 2010 et du tout début des années 2020, les doses de GS-441524 administrées tournaient généralement autour de 2 à 4 mg/kg/j. Elles sont beaucoup plus importantes au milieu des années 2020 : dans le présent article, la posologie de départ (par voie injectable) du GS-441524 chez les chats négatifs pour le FeLV, était de 10 mg/kg et par jour pour les formes sèches, 10 mg/kg matin et soir pour les formes humides, neurologiques et oculaires, et 12 à 30 mg/kg matin et soir chez les chats les plus sévèrement atteints. Ces doses étaient légèrement supérieures dans le groupe FeLV+, et augmentées en cas d'absence de réponse au début du traitement, ou en cas de rechute.
5 - Et la "PIF" du furet ?
Alors d'accord, c'est vrai, ce n'est pas du tout le sujet du jour, et puis d'abord ce n'est pas exactement de péritonite infectieuse féline qu'il s'agit, puisque les furets ne sont pas des félins. Mais si on en parle ici, c'est parce que cette coronavirose systémique du furet (Ferret Systemic Coronaviral Disease pour les Anglo-saxons) ressemble comme deux gouttes d'eau à la forme sèche de la PIF chez le chat, et que le GS-441524, déjà utilisé avec succès chez des furets infectés par le SARS-CoV-2 responsable de la COVID-19, a permis, comme chez le chat, une amélioration très rapide et durable des symptômes chez des furets atteints de CSF. Dans une étude portant sur 7 furets (EC Caride & Coll, décembre 2025), les durées de vie après le début du traitement se sont étalées de 9 mois à plus de 3 ans. Trois furets sont décédés au cours de l'étude, mais sans présenter de lésions évocatrices de CSF, et sans mise en évidence du coronavirus - donc, peut-être morts d'autre chose et en tout cas, le traitement avait chassé le virus. Dans une autre étude portant sur 3 furets atteints de CSF (J Puffal & Coll, 2024), ces derniers ont également répondu très rapidement à l'administration du GS-441524, et étaient toujours vivants et en bonne santé 7 à 12 mois après le début du traitement. Vous pourrez télécharger des vidéos assez spectaculaires de la réponse au traitement de l'un de ces trois furets, en suivant ce lien. Rappelons que jusque là, le traitement de la coronavirose systémique du furet reposait sur de fortes doses de corticoïdes et une couverture antibiotique, qui n'empêchaient pas une dégradation lente (sur plusieurs mois), et systématiquement fatale pour la petite bête.
Et en prévention ?
Comme on ne peut pas compter sur la vaccination (non disponible en France, de toute façon ; on en parle à la fin de cette partie), la seule prévention de la PIF consiste à empêcher l'infection par le FCoV… ce qui n'est pas chose facile ! Envisageons successivement le cas où nous aurions un gentil petit chat naïf qui croise la route de chats excréteurs de FCoV, puis inversement, le cas où nous serions nous-mêmes propriétaires d'une petite colonie de chats infectés, au sein de laquelle nous aimerions bien stopper la circulation du virus… à défaut de s'en débarrasser complètement ! Et on terminera avec les mesures à prendre pour protéger notre Félix, tout juste guéri d'une PIF.
1 - Mon chat a été en contact avec un chat infecté
Si mon chat a été en contact avec un chat malade de la PIF, il n'y a pas trop de souci à se faire : on l'a vu plus haut, les chats malades n'excrètent pas directement le virus de la PIF (sauf cas particulier : voir ci-dessous l'épidémie de PIF à Chypre), et ils excrètent même très peu de FCoV non muté.
Qu'en est-il, maintenant, si mon chat a été en contact avec un congénère porteur du FCoV intestinal ? On l'a vu, la transmission est essentiellement fécale/orale, même si de très rares cas de transmission par la salive ont été décrits. Pour que notre chat attrape le virus, il faut donc que les deux matous aient farfouillé dans la même litière et léchouillé leurs crottes respectives. S'ils se sont juste croisés au fond du jardin, frotté le flanc ou reniflé le museau (de pas trop près) pendant 10 secondes… ça devrait aller.
Si, en revanche, notre chat a été en contact prolongé avec un chat infecté par le FCoV, ou a vécu en compagnie d'un chat qui a fini par mourir de la PIF, il y a de fortes chances qu'il ait contracté le FCoV et soit séropositif. On l'a vu plus haut, cela ne veut pas dire qu'il développera une PIF, y compris s'il est fortement séropositif : pour cela, il faut encore que son virus intestinal mute pour se transformer en virus de la PIF. Dans une étude portant sur 50 chats ayant présenté des taux d'anticorps élevés lors de trois dosages successifs, 4 seulement ont développé une PIF et en sont morts (c'était longtemps avant la découverte du traitement).
Une fois rentré à la maison, si notre chat contaminé vit seul (ou on va dire, au pire, avec deux autres chats), et qu'il fait ses besoins à l'extérieur, il y a de bonnes chances qu'en l'absence de recontaminations successives, il finisse par éliminer l'infection et se négative après quelques mois ou quelques années ; si cela se produit, il ne développera évidemment pas la PIF. Notons qu'un faible pourcentage de chats semble résistant à l'infection et reste séronégatif, même dans une maison où tous les chats sont porteurs. Ces chats ne développeront évidemment pas la PIF.
On l'a vu, le FCoV ne résiste pas très longtemps dans le milieu extérieur : au mieux, il peut rester infectieux 7 semaines dans un environnement sec. Il sera donc prudent d'attendre trois mois avant de faire rentrer notre chat dans une maison où a vécu un chat infecté.
2 - J'ai plein de chats, à la maison ! (ou un élevage, ou un refuge…)
OK, alors là, ça va devenir compliqué parce qu'on en a parlé plusieurs fois, la charge virale en FCoV et, de ce fait, le risque que celui-ci finisse par muter en virus de la PIF, augmente au gré des infections, ré-infections, ré-ré-infections, etc.
Alors, on se répète un peu, mais quand on a un seul chat à la maison, voire deux, voire trois, qui font leurs besoins dehors et les recouvrent soigneusement tout de suite après, même s'il y en a un qui a du FCoV dans l'intestin, le risque qu'il le transmette aux autres est assez réduit et avec un peu de chance, il finira par l'éliminer tout seul, et puis voilà.
Photo ci-contre : On se trouve un petit coin à l'ombre, on y fait son petit caca, et on le recouvre soigneusement. Résultat : 15% seulement des chats de maison vivant seuls sont séropositifs pour le FCoV.

C'est évidemment beaucoup plus compliqué lorsque l'on a cinq, dix ou quinze chats ; que l'on soit un amoureux des chats et qu'on en ait plein sa chambre et son salon, ou éleveur, ou gestionnaire d'un refuge… A fortiori si les chats n'ont pas accès à l'extérieur, ou qu'ils préfèrent faire leurs besoins dans le bac à litière. (Il y en a, comme ça, qui rentrent de dehors pour faire leur crotte dans le bac, puis qui repartent se promener dehors, et on n'a plus qu'à nettoyer. Grrrrr…). Bref, là, il est évident que si, à chaque fois qu'un chat fait sa crotte, neuf autres passent derrière pour la renifler, il suffira qu'il y en ait un qui soit porteur du coronavirus pour contaminer tout le monde en pas longtemps. Une étude allemande (U. Klein-Richers & Coll, 2020) portant sur 170 chats répartis dans 37 élevages a montré que 76,5% (!) des chats excrétaient du FCoV, et aucun élevage n'était indemne.
Donc, les conseils qu'on trouve dans la littérature scientifique pour ces maisons ou établissements multi-chats :
- Pas plus de trois chats par pièce (ou par secteur de la maison), avec si possible un accès à l'extérieur pour chaque tribu. Cela va sans dire mais au moment de la répartition, il est conseillé de mettre ensemble des chats qui s'entendent bien !
- Si l'accès à l'extérieur est impossible, prévoir un bac à litière de plus que le nombre de chats, (s'il y a trois chats dans la pièce, on leur met quatre bacs), positionnés à distance les uns des autres, et aussi à distance des gamelles et de l'eau. (Au passage : un bac de plus que le nombre de chats, c'est aussi ce qui est conseillé en comportement, notamment dans les problèmes de malpropreté ou de cohabitation entre chats).
- Les selles sont retirées deux fois par jour, et le bac à litière nettoyé à fond au moins une fois par semaine.
- Une litière très agglomérante à base de bentonite (ou terre à foulon) pourrait être utile pour réduire la dissémination du virus.
Tout cela demande évidemment une organisation certaine ! (Photo ci-contre : là, il y aura effectivement du boulot ! Détail d'un dessin d'Albert Dubout, dans : Les chats, Ed. Hoëbeke)
Il est, bien sûr, intéressant d'identifier les porteurs/excréteurs de FCoV, et de les séparer des chats indemnes. On peut, pour cela, utiliser la sérologie (sur prise de sang), des taux d'anticorps anti-FCoV élevés étant généralement corrélés à une forte charge en virus dans les selles, et donc à son excrétion… mais les choses n'étant jamais aussi simples qu'on le voudrait, on a trouvé (par PCR) du FCoV dans les selles de chats séronégatifs, et inversement, des chats séropositifs sans ARN de FCoV dans les selles. (Logique, vu que l'excrétion du virus peut être intermittente).

Autre possibilité, rechercher le virus par PCR dans les selles des chats à dépister, mais vu le caractère intermittent de l'excrétion que l'on vient de mentionner, on réalisera trois tests à une à quatre semaines d'intervalle. Donc rien de sûr à 100%, mais un dépistage par l'une ou l'autre technique sera toujours mieux que rien. Il est bien évident que quand on se bagarre déjà pour contrôler le FCoV qui circule chez ses dix chats, on n'autorisera pas un nouveau félin à rejoindre le reste de la troupe sans l'avoir préalablement testé, et lui avoir imposé une quarantaine ! (Compter deux mois, pour la quarantaine). Même chose en élevage, pour les chats extérieurs utilisés pour des saillies - bon, il sera peut-être difficile d'imposer deux mois de quarantaine au super-étalon qui vient de l'autre bout du pays, mais on peut au moins demander un test.
On a parlé, dans la partie consacrée au traitement, de l'utilisation du GS-441524 à faible dose et pour une courte durée, chez les chats porteurs non malades, histoire d'assainir son effectif : ça a l'air de marcher, mais ça reste très controversé, et actuellement déconseillé, du fait du risque d'induire des résistances chez un coronavirus qui n'a déjà pas besoin de ça pour muter !
On sait que le stress (au sens large : maladie intercurrente, chirurgie, arrivée dans un refuge…), en altérant le système immunitaire, prédispose un chat porteur du FCoV à développer la maladie : une publication de 2022 (Healey & Coll) décrit par exemple le cas de 7 chats admis dans un refuge après l'incendie de leur maison : trois déclarèrent une PIF une dizaine de jours après leur admission, et un quatrième (adopté entretemps), décéda six semaines plus tard, avec des symptômes très évocateurs de PIF. Alors il va sans dire que c'est toujours bien de réduire le niveau de stress de son chat, mais ce sera particulièrement vrai dans un élevage ou un refuge où, par nature, le FCoV circule facilement, et où les problèmes de cohabitation, le stress de la perte ou de l'abandon dans le cas des refuges… peuvent favoriser la mutation du virus intestinal. Donc, toutes les mesures visant à réduire le stress de la vie en collectivité (comme regrouper les chats par affinités…), seront évidemment bonnes à prendre.
Un point délicat, surtout en élevage, si on a un FCoV qui circule : quid des chattes reproductrices porteuses/excrétrices du coronavirus ? Une solution proposée par certains auteurs repose sur le fait que les chatons nés de chattes infectées sont protégés par les anticorps maternels jusqu'à l'âge de 5-6 semaines.

Dessin d'Albert Dubout, dans : Les chats, Ed. Hoëbeke
Par ailleurs, certaines chattes arrêtent d'excréter le virus après quelques semaines si elles ne sont pas ré-exposées. Dans une maison avec plusieurs chats excréteurs de FCoV, il est donc proposé d'isoler les chattes 2 à 3 semaines avant la mise-bas et pendant la lactation, puis de sevrer à les chatons à l'âge de 4 à 6 semaines pour les exfiltrer vers une autre maison, si possible sans chat, jusqu'à ce que leur statut vis à vis du FCoV soit définitivement éclairci. Bon, tout cela n'est tout de même pas très pratique à mettre en œuvre, sans compter qu'un tel isolement n'est pas idéal pour le développement comportemental et la socialisation des chatons !
Un mot sur le cas particulier des refuges : la prévention y est difficile car même en isolant les chats dans des cages individuelles, le FCoV est facilement transporté par les vêtements, les chaussures, voire la poussière - a fortiori en cas de surpopulation. Les chats sauvages introduits dans les refuges sont majoritairement négatifs, (cf la vie à l'extérieur et l'enfouissement des selles), mais la plupart se positivent en quelques semaines : dans une étude portant sur 2207 chats répartis dans 14 refuges au Royaume-Uni (Cave & Coll, 2004), les chats ayant passé plus de 60 jours en refuge avaient plus de 5 fois plus de chances d'être séropositifs que ceux qui étaient arrivés depuis moins de 60 jours.
3 - La prévention chez le chat guéri
Il y a quelques années, la question ne se posait pas, puisque tout le monde mourait. Aujourd'hui, on ne va pas s'en plaindre, mais comme la plupart des chats s'en sortent… que doit-on faire ou ne pas faire une fois qu'ils sont guéris ? On manque évidemment de recul dans ce domaine, et les réponses aux questions ci-dessous reposent en grande partie sur des avis ou observations personnelles d'experts… mais dans un premier temps, ce sera toujours mieux que rien. A noter que même si on donne quelques pistes, ces questions seront à discuter avec votre vétérinaire qui connaît votre chat, la situation sanitaire dans le secteur, (les virus qui circulent), etc.
D'abord, un chat guéri de la PIF peut-il ré-attraper la PIF ? Une petite précision avant de répondre, (ou pas, d'ailleurs), à cette question : il ne faudrait pas confondre rechute et ré-infection. Une rechute est possible après traitement, on en a vu plein d'exemples, mais il ne s'agit pas alors d'une nouvelle PIF, c'est juste l'ancienne qui, pour une raison ou pour une autre, n'a pas été totalement éradiquée de l'organisme du chat, et qui ressort. Ici, ce qui nous occupe, c'est de savoir si un chat guéri guéri peut attraper la PIF une seconde fois, ou s'il est protégé. Alors on a peut-être mal cherché, mais on n'a rien trouvé sur le sujet dans la littérature. Il faut dire qu'il n'y a pas longtemps qu'on sait traiter la PIF, que comme on l'a vu plus haut, il ne s'agit quand même pas d'une maladie bien fréquente, et que tous les chats qui ont du FCoV intestinal ne font pas une PIF, loin de là. Alors même s'il existe une prédisposition génétique, ce ne serait vraiment pas de bol pour un chat d'avoir déjà fait deux PIF successives depuis le peu de temps que le traitement existe ! En revanche, ce que l'on sait, c'est que les chats guéris de la PIF par le GS-441524, peuvent se recontaminer rapidement avec le FCoV intestinal de leurs collègues : on l'a vu plus haut, par exemple dans l'étude de Zwicklbauer (2023), avec 5 chats sur 14 déjà ré-infectés pendant la période de suivi après traitement : il ne manquerait plus alors qu'une petite mutation pour voir resurgir un FIPV mais encore une fois, d'abord ce ne serait vraiment pas de chance, et a priori, cela n'a pas (encore) été décrit.
Peut-on vacciner ou stériliser un(e) chat(te) en rémission après un traitement par le GS-441524 ? Sachant qu'on a parlé plus haut du rôle du stress (au sens large, ce qui inclut évidemment une chirurgie) dans le déclenchement d'une PIF chez un chat porteur du FCoV intestinal, et que nous-mêmes avons eu le cas d'une jeune chatte tout juste sortie d'un élevage, qui a déclenché une PIF dans les jours suivant sa stérilisation. Des séries de cas non publiées semblent cependant indiquer qu'il est possible de vacciner ou stériliser des chats après (voire pendant) un traitement par le GS-441524 ; avec, bien sûr, des manipulations aussi douces que possible, et une prise en charge de la douleur - mais cela devrait toujours être le cas, PIF ou pas PIF ! Dans la vaste étude d'Ansari Mood (2026), 95 chats ont subi une intervention en cours de traitement par le GS-441524, sans problème particulier, semble-t-il : il s'agissait essentiellement (dans 91 cas) de stérilisations, (castrations, ovario-hystérectomies) et de soins dentaires, mais 4 chats ont dû être opérés en urgence pour des fractures ou une intussusception intestinale. Dans les 91 cas où l'intervention pouvait être programmée, celle-ci a été réalisée dans les 20 derniers jours du traitement, ce dernier étant poursuivi au moins 14 jours après l'intervention. En conclusion, il est toujours possible de réaliser une intervention de routine pendant un traitement pour la PIF… mais sauf cas particulier, (comme une chatte qui risque de se faire saillir par tous les matous du quartier, un chat qui se bagarre et urine partout, ou qui va être adopté…), ce sera quand même mieux d'attendre un peu ! La dernière mise à jour sur le traitement de la PIF (S. Taylor & Coll, 2025) recommande d'attendre un mois après la fin du traitement. A noter que tout ce qui précède est également valable pour un séjour en pension, un toilettage, ou autres situations/interventions équivalentes.
Concernant la vaccination : dans l'étude iranienne de 2026, les chats n'ont jamais été vaccinés pendant le traitement ni pendant les trois mois suivants, et l'auteur conseillait même de décaler les vaccinations de routine jusqu'à six mois. La mise à jour de Taylor & Coll recommande d'attendre un mois après la fin du traitement. Après… à voir selon le contexte ce qui est nécessaire ou pas. Si Princesse vit seule dans son appartement du cinquième étage, on la laissera peut-être se remettre de sa PIF avant de se précipiter pour lui faire son rappel de vaccin. (Même s'il n'est jamais totalement exclu qu'on puisse lui ramener un virus sous la semelle des chaussures mais bon, c'est une question d'évaluation des risques). En revanche, s'il y a une grosse colonie de chats qui traîne dans le quartier, qu'ils sont tous en diarrhée et passent leur temps à éternuer, et qu'il est impossible de garder Attila à l'intérieur depuis qu'il se sent mieux avec son GS-441524… on ne va quand même pas trop traîner pour lui faire son rappel ! A noter qu'on ne connaît pas, à l'heure actuelle, l'efficacité d'un vaccin administré pendant un traitement antiviral.
Côté anti-parasitaires, tout le monde les prescrit sans arrière-pensée : de nombreux chats ont été traités sans problème (Taylor & Coll).
Autre question un peu dans le même genre, peut-on faire reproduire une chatte (ou, d'ailleurs, un chat), guéris de la PIF ? Là, il n'y a pas que l'effet sur le système immunitaire de la chatte gestante qui intervient : il existe une composante génétique significative au risque de développer une PIF après une infection par le FCoV (S. Taylor, 2025). On sait par exemple que le risque d'attraper la PIF est plus important pour les chats issus de la même portée qu'un chaton qui a eu la PIF, que pour les autres chats qui vivent dans le même environnement. Il est donc recommandé de retirer de la reproduction les parents (mâle et femelle) et frères et sœurs de chats ayant développé une PIF… et bien sûr, ces chats eux-mêmes !
4 - La vaccination
Alors on en dit un mot pour la culture générale et parce que vous pourriez en entendre parler, mais de toute façon, le vaccin n'est pas disponible en France, ce qui est déjà une bonne raison pour ne pas l'utiliser !
Il se fait par voie nasale, et provoque ainsi une immunité locale au point d'entrée du FCoV (l'oropharynx). On utilise un mutant du FCoV qui se multiplie à faible température (celle de l'appareil respiratoire supérieur), mais pas à la température du reste du corps.
Son efficacité est contestée et surtout, il est inefficace chez les chats déjà séropositifs pour le FCoV. Or, dans une collectivité de chats, (là où il serait intéressant de vacciner, car ce sont rarement les chats vivant seuls qui déclenchent une PIF), en général, il y a pas mal de séropositifs, y compris parmi les chatons de 16 semaines (l'âge minimum pour vacciner) ; du coup… ça ne sert pas à grand chose. Ajoutons qu'on n'est pas trop sûr de sa durée d'efficacité mais qu'elle ne serait pas bien longue, et que la plupart des chats vaccinés deviennent séropositifs ce qui fait qu'après, on ne sait plus trop où on en est. Allez, essayons d'être un peu positif, dans une étude en double-aveugle réalisée sur une population de chats séronégatifs, il y a eu une faible, mais significative, diminution du nombre de chats développant une PIF parmi les animaux vaccinés.
Enfin, à défaut de servir à grand chose, au moins le vaccin est sûr : c'est déjà ça, on ne risque pas de donner la PIF à un chat en le vaccinant, ni de provoquer une aggravation des symptômes (par l'intermédiaire d'une augmentation du taux d'anticorps) si, par hasard, il avait déjà la PIF. (Ce qui serait ballot !)
Sans surprise après tout ça, le vaccin n'est pas recommandé par le groupe d'experts européens sur la PIF (S. Tasker & Coll, 2023).
Voir Chypre et mourir
Bon, l'expression d'origine, c'est "Voir Naples et mourir", qui a dérivé au fil du temps vers "Voir Venise et mourir", ce qui signifierait, (tout le monde n'est pas d'accord là-dessus), que la baie de Naples est tellement belle qu'une fois qu'on l'a vue, on peut mourir tranquille. Et les Vénitiens n'ont naturellement pas voulu être en reste. Le hic, c'est que quand on s'appelle Minette ou Garfield, et qu'on accompagne sont maître qui a voulu vérifier si Chypre, c'est aussi beau que le reste… eh bien on meurt pour de bon ! et en l'occurrence, de la PIF. Explications :
1 - Le Coronavirus chypriote
En janvier 2023, une véritable épidémie de PIF est partie de Nicosie, capitale de Chypre, pour s'étendre à l'ensemble de l'île dès le mois de mars. On reparlera de la maladie elle-même dans le paragraphe suivant consacré à l'épidémiologie, mais concernant le virus - sans trop entrer dans les détails, ce qui nous amènerait très très très loin - il résulte de la recombinaison d'un sous-type de notre FCoV classique avec une souche hypervirulente du coronavirus canin pCCoV, cette dernière étant capable d'infecter de nombreux organes du chien : intestin, poumons, rate, foie, reins, ganglions, cerveau et même les lymphocytes B et T dont nous avons parlé plus haut, ce qui est tout de même un comble ! (Rappelons que le virus canin CCoV se cantonne normalement au tractus digestif du chien, ne provoque que des symptômes digestifs bénins voire pas de symptômes du tout, et s'élimine tout seul). Le nouveau virus ainsi obtenu a été baptisé FCoV-23. Il se caractérise, dans la plupart des cas, par l'insertion dans le gène codant pour la protéine S du FCoV, (on le rappelle : celle qui permet au virus de rentrer dans une nouvelle cellule), d'une séquence identique à 96,5% provenant du pCCoV canin hypervirulent. Malgré tout, le génome du FCoV-23 est resté globalement suffisamment proche du génome original du FCoV (identique à plus de 99,17%), pour permettre sa transmission directe de chat à chat. Pour faire court, on a donc un virus aussi méchant que celui de la PIF, qui se transmet aussi facilement que le FCoV.
Ceux qui veulent en savoir plus, les passionnés du site de clivage de la furine à l'interface S1-S2, les aficionados du CCoV-HuPn-2018, se reporteront utilement à l'article de Charalampos Attipa paru dans la revue Nature en juillet 2025, mais il faut être prévenu que la lecture en est… exigeante ! En attendant, la morale de cette histoire, c'est qu'après l'expérience de la Covid-19, (qui n'a, on l'a vu plus haut, aucun rapport avec les coronavirus du chat et du chien), on ne peut vraiment jamais être tranquille avec les coronavirus, et on reste toujours à la merci d'une mutation ou d'une recombinaison dont sortirait un virus aussi agressif que celui qui décime les chats chypriotes depuis 2023.
2 - La circulation du virus
Donc, l'histoire a commencé en janvier 2023, avec la description de premiers cas de PIF à Nicosie. En février, le nombre de cas atteignait un pic autour de la capitale et en mars, toute l'île était touchée, avec une prévalence particulièrement élevée dans la région de Famagouste - ce qui laisse supposer une atteinte équivalente (et logique) de la partie turque de l'île, pour laquelle on ne semble pas disposer d'informations. Le nombre de cas confirmés a ensuite diminué de juin à août 2023, avant l'arrivée d'une seconde vague (tout de même moins forte que la première) entre septembre 2023 et mars 2024, puis d'une troisième en juin 2024.
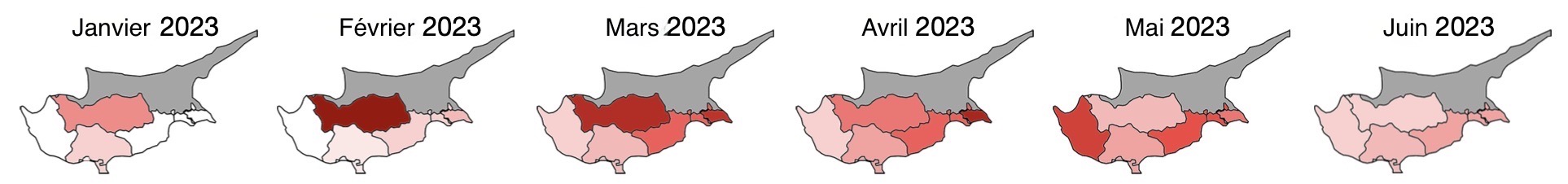
Evolution du nombre de cas confirmés de PIF à Chypre, province par province, entre janvier et juin 2023 : plus c'est foncé, plus il y a de cas ! Après, ça s'est calmé, mais avec tout de même deux nouvelles vagues en septembre 2023 - mars 2024, puis en juin 2024. On voit que tout est parti de Nicosie, (au centre de la carte), et que c'est là que le nombre de cas a été maximal. La région de Famagouste, (la petite pointe complètement à l'est de la partie grecque (= sud) de l'île), a été bien touchée également. D'après : C. Attipa & Coll, Nature, 2025 : voir dans la liste des références.
Le nombre de diagnostics de PIF confirmés est ainsi passé de 3 (en 2021) et 4 (en 2022), à 186 en 2023 et 215 de janvier 2023 à juin 2024, ce qui représente une multiplication par 50 du nombre de cas. Alors ces chiffres peuvent paraître faibles, et on serait tenté de se dire qu'il n'y a pas de quoi en faire tout un plat. Le problème, c'est que Chypre a été surnommée "l'île aux chats", (aujourd'hui, certains journaux l'appellent "l'île aux chats morts"), parce qu'elle hébergerait dans les un million de chats errants, (à la louche, bien sûr), et qu'évidemment, tous ceux-là ne sont ni diagnostiqués, ni comptabilisés dans les statistiques. La Pancyprian Veterinary Association évalue à 10 000 le nombre de chats chypriotes présentant des symptômes de PIF, à avoir été présentés chez un vétérinaire entre janvier et juillet 2023… tandis que traîne dans la plupart des journaux "généralistes" le chiffre de 300 000 décès (soit un tiers de la population féline totale (estimée) de l'île. En outre, au mois de mai 2025, 5 cas confirmés d'infection par le FCoV-23 ont été diagnostiqués au Royaume Uni, dont 4 en provenance de Chypre, et un de Grèce. Une occasion de signaler que la présence du virus recombiné est suspectée, (mais non confirmée à ce jour), en Grèce, en Turquie et au Liban… entre autres ; et que le nombre de cas au Royaume Uni pourrait bien être sous-estimé.

Un chat errant sur une jetée du port de Larnaca. Heureusement pour lui, c'était quelques années avant l'apparition du virus mutant !
Mais alors, qu'est-ce qu'il a de particulier, ce FCoV-23 pour se transmettre et circuler comme ça ? on l'a vu plus haut : dans un monde normal, un chat infecté par le "gentil" FCoV ne développera pas une PIF, sauf dans les rares cas où le virus mute pour devenir le méchant agent de la PIF. Mais celui-ci ne passera pas d'un chat à l'autre, sa présence résultera toujours d'une mutation chez un FCoV déjà présent chez l'animal et ensuite, ce virus muté ne sortira plus jamais de son chat. Rien de tout cela avec le virus chypriote : le virus muté se transmet directement d'un chat à l'autre par l'intermédiaire des selles, porteuses d'une forte charge virale, et la PIF se développe rapidement chez le chat nouvellement infecté, indépendamment de son âge ; ce qui montre que contrairement au virus classique de la PIF, qui s'attaque surtout aux jeunes chats sans défense ou presque, le FCoV-23 se moque pas mal de l'immunité qu'ont pu développer un chat adulte ou âgé.
3 - Symptômes, et tentatives de traitement
Après la transmission, les symptômes. Ils sont similaires à ceux de la PIF classique… mais quand même pas complètement identiques. En particulier, la variété des organes infectés et la charge virale dans chacun de ces organes, (pantropisme), semble encore plus élevée dans l'infection par le FCoV-23 que dans notre PIF à nous. La forme la plus fréquente est la PIF humide (63,7% des cas), suivie par une forme neurologique, plus fréquente avec le FCoV-23 (26% des cas) que dans la PIF classique (14%), probablement à cause d'un neurotropisme supérieur chez le FCoV-23, ou peut-être du fait d'une vigilance accrue des praticiens vis à vis de ces symptômes. Vient ensuite une forme sèche (10,2% des cas).
Le 3 août 2023, face à l'hécatombe, (10 000 ou 300 000 chats morts selon les sources, dans un cas comme dans l'autre, ça fait beaucoup), les autorités chypriotes ont autorisé l'utilisation des antiviraux pour humains stockés lors de la pandémie de Covid, en particulier le GS-441524 et le molnupiravir. Ces traitements se sont montrés efficaces lorsqu'ils ont été employés chez les chats infectés par le FCoV-23… sauf que 1) une confirmation par PCR du diagnostic de PIF était nécessaire pour avoir accès au produit, et le test n'a, bien sûr, pas pu être réalisé chez tous les chats présentant des symptômes évocateurs ; 2) le prix du traitement, on l'a vu, est élevé ; et 3) les milliers (ou dizaines ? ou centaines ? de milliers) de chats errants infectés par le virus recombiné, n'avaient évidemment aucune chance de recevoir du GS-441524 ou du molnupiravir. La mise à disposition des antiviraux n'avait donc aucune chance de stopper l'épidémie.
La conclusion de tout cela, c'est que si on envisage d'aller s'installer à Chypre, ou du moins y passer une longue période, il sera vivement conseillé de laisser Minette et Garfield à la maison, ou à défaut en pension chez la belle-famille. Et que si un gentil petit chaton vous suit en poussant des miaulements désespérés quelque part du côté de Paphos ou de Larnaca… On en éprouvera peut-être de la culpabilité pour le restant de ses jours, mais il faudra savoir se convaincre que le cacher dans son bagage cabine pour le ramener en France ne serait pas du tout du tout du tout une bonne idée !
Quelques références
On a fait une petite sélection, parce que pour vous donner une idée, dans l'article de synthèse de Tasker & Coll (2023) dont les coordonnées figurent ci-dessous, on trouve… 444 références ! Et il y a plein d'autres publications qui sont sorties depuis. Donc, juste quelques articles parmi ceux qui nous ont semblé les plus utiles :
DD Addie, F Bellini, J Covell-Ritchie & Coll : Stopping Feline Coronavirus shedding prevented Feline Infectious Peritonitis. Viruses 2023, 15(4), 818
DD Addie, J Covell-Ritchie, O Jarrett & Coll : Rapid Resolution of Non-Effusive Feline Infectious Peritonitis Uveitis with an Oral Adenosine Nucleoside Analogue and Feline Interferon Omega. Viruses 2020, 12(11), 1216.
M. Allinder, B. Tynan, C. Martin & Coll : Uroliths composed of antiviral compound GS-441524 in 2 cats undergoing treatment for feline infectious peritonitis. J Vet Intern Med, 2024 Jan-Feb 38(1) : 370-374
M. Ansari Mood : Analysis of risk factors, clinical data, treatment outcomes for cats with feline infectious peritonitis using GS-441524 (2020–2024). Sci Rep 16, 1037 (2026).
C Attipa, AS Warr, D Epaminondas & Coll : Feline Infectious Peritonitis epizootic caused by a recombinant coronavirus. Nature, 2025 Sep ; 645(8079):228-234
SJ Coggins, JM Norris, R Malik & Coll : Outcome of treatment of cats with feline infectious peritonitis using parenteral remdesivir, with or without transition to oral GS-441524. J. Vet. Intern. Med. 2023, 37 : 1772–1783
J Green, H Syme, S Tayler : Thirty-two cats with effusive or non-effusive feline infectious peritonitis treated with a combination of remdesivir and GS-441524. J. Vet. Intern. Med. 2023. 37,5 : 1784-1793.
K Hazuchova, S Held, R Neiger & Coll : Usefulness of acute phase proteins in differentiating between feline infectious peritonitis and other diseases in cats with body cavity effusions. J. Feline Med. Surg. 2017, 19, 809–816.
M Katayama, Y Uemura : Prognostic Prediction for Therapeutic Effects of Mutian on 324 Client-Owned Cats with Feline Infectious Peritonitis Based on Clinical Laboratory Indicators and Physical Signs. Vet. Sci. 2023, 10(2), 136
D Krentz, K Zenger, M Alberer & Coll : Curing Cats with Feline Infectious Peritonitis with an Oral Multi-Component Drug Containing GS-441524. Viruses 2021, 13 (11), 2228.
EK LaVigne, NE Levy, AR Bardzinski & Coll : Spectrum of care approach to animal shelter management of feline infectious peritonitis complicated by feline leukemia virus. Front. Vet. Sci., 2025 12
RS Mueller, G Wess, BS Schulz : Retrospective analysis of pleural effusion in cats. J. Feline Med. Surg. 2019, 21, 1102-1110.
NC Pedersen, M Perron, M Bannasch & Coll : Efficacy and safety of the nucleoside analog GS-441524 for treatment of cats with naturally occurring feline infectious peritonitis. J Feline Med Surg. 2019 Feb 13;21(4):271–281.
LD Pesteanu-Somogyi, C Razai, BM Pressler & Coll : Prevalence of feline infectious peritonitis in specific cat breeds. J. Feline Med. Surg. 2006, 8, 1–5.
J Puffal, AJ Neece, F Scaletti : Treatment of three ferrets diagnosed with Ferret Systemic Coronaviral Disease using the nucleoside analogue GS-441524. Animals, 2024 Mar 16;14(6):916.
F Riemer, AA Kuehner, S Ritz & Coll : Clinical and laboratory features of cats with feline infectious peritonitis - a retrospective study of 231 confirmed cases (2000-2010). J Feline Med Surg. 2016, 18(4) : 348–356.
L Sangl, K Matiasek, S Felten & Coll : Detection of feline coronavirus mutations in paraffin-embedded tissues in cats with feline infectious peritonitis and controls. J Feline Med Surg. 2018, 21(2) : 133-142.
S Tasker, DD Addie, H Egberink & Coll : Feline Infectious Peritonitis : European Advisory Board on Cat Diseases Guidelines. Viruses, 2023, 15(9) : 1847.
S Taylor, S. Tasker, E. Barker & Coll : Feline Infectious Peritonitis : an update on treatment of FIP using antiviral drugs in 2025 : Growing experience, but more to learn. https://catvets.com/wp-content/uploads/2025/09/FelineVMA_FIP_Guide_2025.pdf
G Tir : Mise à jour des connaissances sur les coronavirus félins : de 1963 à nos jours. Thèse de Médecine vétérinaire et santé animale. 2025. dumas-05292934
Y Yin, T Li, T Wang & Coll : A retrospective study of clinical and laboratory features and treatment on cats highly suspected of feline infectious peritonitis in Wuhan, China. Sci. Rep. 2021, 11, 5208.
J Zhu, S Deng, D Mou & Coll : Analysis of spike and accessory 3c genes mutations of less virulent and FIP-associated feline coronaviruses in Beijing, China. Virology : 589 (2024) 109919
AM Zuzzi-Krebitz, K Buchta, M Bergmann & Coll : Short treatment of 42 days with oral GS-441524 results in equal efficacy as the recommended 84 days treatment in cats suffering from Feline Infectious Peritonitis with effusion - A prospective randomized controlled study. Viruses, 2024 Jul 16;16(7):1144
K Zwicklbauer, D Krentz D, M Bergmann & Coll : Long-term follow-up of cats in complete remission after treatment of feline infectious peritonitis with oral GS-441524. J Feline Med Surg, 2023, 25(8) : 1098612X231183250